Los resultados del estudio FREEDOM, fundamento de las guías de práctica clínica, concluyen que la cirugía de revascularización coronaria es superior a la intervención coronaria percutánea en pacientes diabéticos multivaso. El objetivo de este trabajo fue evaluar qué porcentaje de pacientes de la vida real serían incluibles en dicho estudio y sus implicaciones pronósticas.
MétodosSe siguió a 617 diabéticos multivaso, a los que se les había realizado una coronariografía entre 2012 y 2014. Se clasificaron según el cumplimiento de criterios para participar en dicho estudio y se analizó su impacto en la mortalidad y en los eventos cardiovasculares mayores.
ResultadosEl 51,2% de los pacientes no cumplía los criterios de inclusión, tenían más edad (69,3 frente a 66,1 años; p < 0,001), mayor riesgo EuroSCORE II (7,8 frente a 2,26%; p < 0,001), recibían menos cirugía de revascularización coronaria (6 frente a 15%; p < 0,001), más tratamiento conservador (7,6 frente a 2,3%; p = 0,003) y menos revascularización completa (26,9 frente al 43,1%; p < 0,001). La mortalidad fue mayor en los no incluibles (OR = 4,42; IC95%, 2,75-7,15; p < 0,001) tanto a 30 días (OR = 9,54; IC95%, 2,2-41,2; p < 0,001) como a 35 meses (OR = 5,34; IC95%, 3,02-9,45; p < 0,001). En el análisis multivariable la mortalidad se asoció independientemente al no cumplimiento de los criterios de inclusión (HR = 2,77; IC95%, 1,77-4,37; p = 0,001), la revascularización incompleta (HR = 2,46; IC95%, 1,46-4,13; p = 0,001), la situación clínica (HR = 1,34; IC95%, 1,15-1,67; p = 0,001) y la edad (HR = 1,04; IC95%, 1,02-1,06; p < 0,001).
ConclusionesMás de la mitad de los diabéticos multivaso de la vida real no serían incluibles en un gran ensayo clínico, presentando 4 veces más riesgo de muerte en el seguimiento.
The results of the FREEDOM study, the basis of clinical practice guidelines, conclude that coronary artery bypass grafting is superior to percutaneous coronary intervention in diabetic patients with multivessel coronary artery disease. The aim of this study was to evaluate the percentage of real-life patients that would be suitable for inclusion in the study and the prognostic implications.
MethodsAn evaluation was performed on 617 diabetic patients with multivessel coronary artery disease who underwent coronary angiography between 2012 and 2014. Patients were classified according to the criteria for participation in the FREEDOM study, with the impact on mortality and major cardiovascular events being analysed.
ResultsOf all patients, 51.2% did not meet the inclusion criteria. They were older (69.3 vs 66.1 years; P<.001), with a higher EuroSCORE II (7.8 vs 2.26%; P<.001), underwent coronary artery bypass grafting less (6 vs 15%; P<.001), had more conservative treatment (7.6 vs 2.3%; P=.003), and less complete revascularisation (26.9 vs 43.1%; P=.001). Mortality was higher in non-eligible patients (OR, 4.42; 95%CI, 2.75-7.15; P<.001) both at 30 days (OR, 9.54; 95%CI, 2.2-41.2; P< .001), and at 35 months (OR, 5.34; 95%CI, 3.02-9.45; P<.001). The multivariate analysis showed mortality to be independently associated with not meeting inclusion criteria (HR, 2.77; 95%CI, 1.77-4.37; P=.001), incomplete revascularisation (HR, 2.46; 95%CI, 1.46-4.13; P=.001), clinical status (HR, 1.34; 95%CI, 1.15-1.67; P=.001), and age (HR, 1.04; 95%CI, 1.02-1.06; P<.001).
ConclusionsOver half of real-life MVD patients would not be suitable for inclusion in a large clinical trial as they had four times more risk of death in follow-up.
La prevalencia de la diabetes mellitus en el mundo aumenta continuamente y es un importante problema de salud pública. Según la OMS, la prevalencia en 2014 fue del 8,5% y en 2012 causó más de 1,5 millones de defunciones1. Esta situación empeora en España ya que afecta a casi el 14% de la población mayor de 18 años (más de 5,3 millones de personas)2.
La diabetes se asocia a una morbimortalidad muy aumentada de origen principalmente cardiovascular3; se estima que está asociada a alrededor del 50% de las muertes y a más del 75% de las causas de hospitalización4,5, aunque en descenso por la mejora del control desde atención primaria y especializada6. Los pacientes presentan una afección coronaria más compleja, extensa y difusa con mayor daño multivaso en comparación con los pacientes no diabéticos5, lo que hace más controvertido su tratamiento óptimo.
Diversos estudios clásicos7 sentaron la indicación de cirugía de revascularización coronaria (CABG) como la primera opción de tratamiento en pacientes diabéticos con enfermedad coronaria multivaso (MVD), pero con la mejora y la simplificación de las técnicas de intervención coronaria percutánea (ICP) y la aparición del stent farmacoactivo surgió la necesidad de responder nuevamente a esta pregunta recurrente. Para darle respuesta surge el estudio FREEDOM8,9, base científica de las últimas guías de práctica clínica10, que concluye nuevamente la superioridad de la CABG frente a la ICP con stent Taxus pese al bajo porcentaje de pacientes con enfermedad coronaria inestable, y con amplios criterios de exclusión. Ante la falta de evidencia actual sobre este tema, diferentes registros publicados en los últimos años han mostrado que no solo los stents de nueva generación son superiores al stent Taxus11–13, sino que cada vez se hacen más ICP y más complejas en los hospitales encuestados, y se deriva a CABG apenas a un tercio de los pacientes14,15, principalmente aquellos en situación aguda.
A pesar de que el ensayo clínico es el tipo de estudio epidemiológico que permite establecer relaciones causales de mayor rigor epidemiológico, sus resultados no siempre son reproducibles en la población general por razones muy diversas: estructurales, organizativas, por las características epidemiológicas de los enfermos tratados y por las diferencias entre los sistemas sanitarios16,17. Los pacientes llamados «del mundo real», cada vez de mayor edad, con más comorbilidad y en peor situación clínica, son diferentes de los pacientes «ideales» incluidos en los ensayos clínicos. Esto limita la aplicabilidad práctica de sus resultados en la toma de decisiones clínicas18,19. Es necesario describir estas diferencias para establecer directrices y guías de práctica clínica.
Nuestro objetivo fue describir cuántos pacientes MVD de la vida real hubieran sido elegibles para participar en un ensayo clínico (estudio FREEDOM), conocer la estrategia de revascularización miocárdica empleada y evaluar su mortalidad y eventos cardiovasculares mayores en el seguimiento.
MétodosSe realizó un estudio retrospectivo a partir de historias clínicas electrónicas y bases de datos de nuestro centro de todos los pacientes con MVD que se sometieron a coronariografía entre el 1 de enero de 2012 y el 31 de diciembre de 2014. Se excluyó a aquellos que padecían afección grave de tronco común izquierdo (TCI), CABG previa y valvulopatía significativa y se clasificaron en función de si eran susceptibles o no de ser incluidos en el ensayo y qué estrategia de revascularización se eligió.
Dado el porcentaje de eventos de estudios previos, se calculó un tamaño muestral para mostrar diferencias del 7% de eventos entre los 2 grupos de 604 pacientes, incluidas las pérdidas de seguimiento (intervalo de confianza del 95% [IC95%] y una potencia del 80%).
El protocolo de estudio recibió la aprobación del comité ético del hospital y todos los datos se trataron de forma anónima.
DefinicionesSe definió como diabético todo aquel paciente que en el momento de la coronariografía diagnóstica estaba en tratamiento hipoglucemiante según la historia clínica o presentaba historia previa de diabetes mellitus.
Se definió como MVD la detección de lesiones de más del 70% en≥2 vasos epicárdicos y≥2 territorios arteriales coronarios separados, susceptible de revascularización tanto por ICP como por CABG. Todos los pacientes tenían indicación para revascularización basada en las guías de revascularización miocárdica vigentes en el momento y el criterio del cardiólogo hemodinamista cuando el tratamiento fue percutáneo, y por decisión colegiada cuando el tratamiento fue quirúrgico.
Se consideró una definición de revascularización completa anatómica si se trataron todos los vasos epicárdicos de calibre≥2mm con lesiones≥70%, independientemente de si tenían viabilidad o isquemia.
Se agrupó a los pacientes en función de si eran susceptibles o no de inclusión para el estudio de referencia, y se los clasificó como «susceptible» o «no susceptible». Se asignó al grupo no susceptible los pacientes que: a) hubieran presentado infarto agudo de miocardio con elevación del segmento ST en las 72h previas a la coronariografía; b) se hubieran sometido a ICP en los 6 meses anteriores; c) presentaran insuficiencia cardiaca grave con clase funcional iii o iv de la New York Heart Association; d) hubieran presentado un ictus en los 6 meses previos o que tuvieran un déficit neurológico residual>Rankin 1; e) tuvieran historia previa de sangrado significativo en los 6 meses previos; f) el vaso diana presentara reestenosis de stent en caso de ICP previa; g) presentaran demencia conocida o una dependencia al menos moderada según la escala Barthel, y h) presentaran enfermedad extracardiaca que limitara la supervivencia por debajo de 5 años, como enfermedad pulmonar obstructiva crónica grave, hepatitis activa, fallo hepático grave o enfermedad renal grave.
Se excluyó de ambos grupos a los pacientes previamente sometidos a cirugía cardiaca (valvular o CABG); también a los que padecían valvulopatía significativa susceptible de intervención o presentaban afección grave (> 50%) de TCI por ser entidades que aportarían demasiada heterogeneidad a la muestra del grupo no susceptible, limitando con ello la interpretación de los resultados por ser una afección para la que las guías recomiendan más frecuentemente el tratamiento quirúrgico.
La indicación de coronariografía se sentó en función del cuadro que motivó el ingreso: síndrome coronario agudo con elevación del segmento ST y síndrome coronario agudo sin elevación del segmento ST, y se utilizó la cuarta definición universal de infarto, angina estable y otros (insuficiencia cardiaca descompensada, shock cardiogénico, parada cardiorrespiratoria, arritmias ventriculares).
La función de eyección del ventrículo izquierdo se clasificó como> 40% o≤40%, medida por ecocardiografía al ingreso.
El grado de afección renal se clasificó según la clasificación de insuficiencia renal. Se midió el filtrado glomerular por el método Chronic Kidney Disease Epidemiology Collaboration en ml/min/1,73m3 y se definió como reducido cuando el filtrado glomerular era≤45 (estadio 3B).
Se definió como evento cardiaco adverso mayor (MACE) el evento combinado de muerte, infarto no letal y nueva revascularización, y evento cardiovascular adverso mayor (MACCE), el evento combinado de muerte, infarto no mortal, nueva revascularización e ictus. Dichos datos se obtuvieron retrospectivamente a través del sistema de información clínica hospitalario del Sistema Andaluz de Salud Diraya y el acceso a la Historia de Salud Única de cada paciente.
Análisis estadísticoLas variables cuantitativas se expresaron como media±desviación estándar. La comparación entre medias se realizó mediante el test de la t de Student y se calculó el IC95% para las diferencias entre medias. Las variables cualitativas se expresaron mediante porcentajes y su comparación, mediante el test de χ2con IC95%. Para el análisis de supervivencia se realizaron tablas de mortalidad y curvas de Kaplan-Meier. En el análisis de supervivencia multivariable se empleó el método de riesgos proporcionales de Cox, indicando los IC95% para las hazard ratio (HR) de las covariables. La significación estadística se alcanzó con p < 0,05. Todos los análisis estadísticos se realizaron mediante el software SPSS versión 20.0 para Mac.
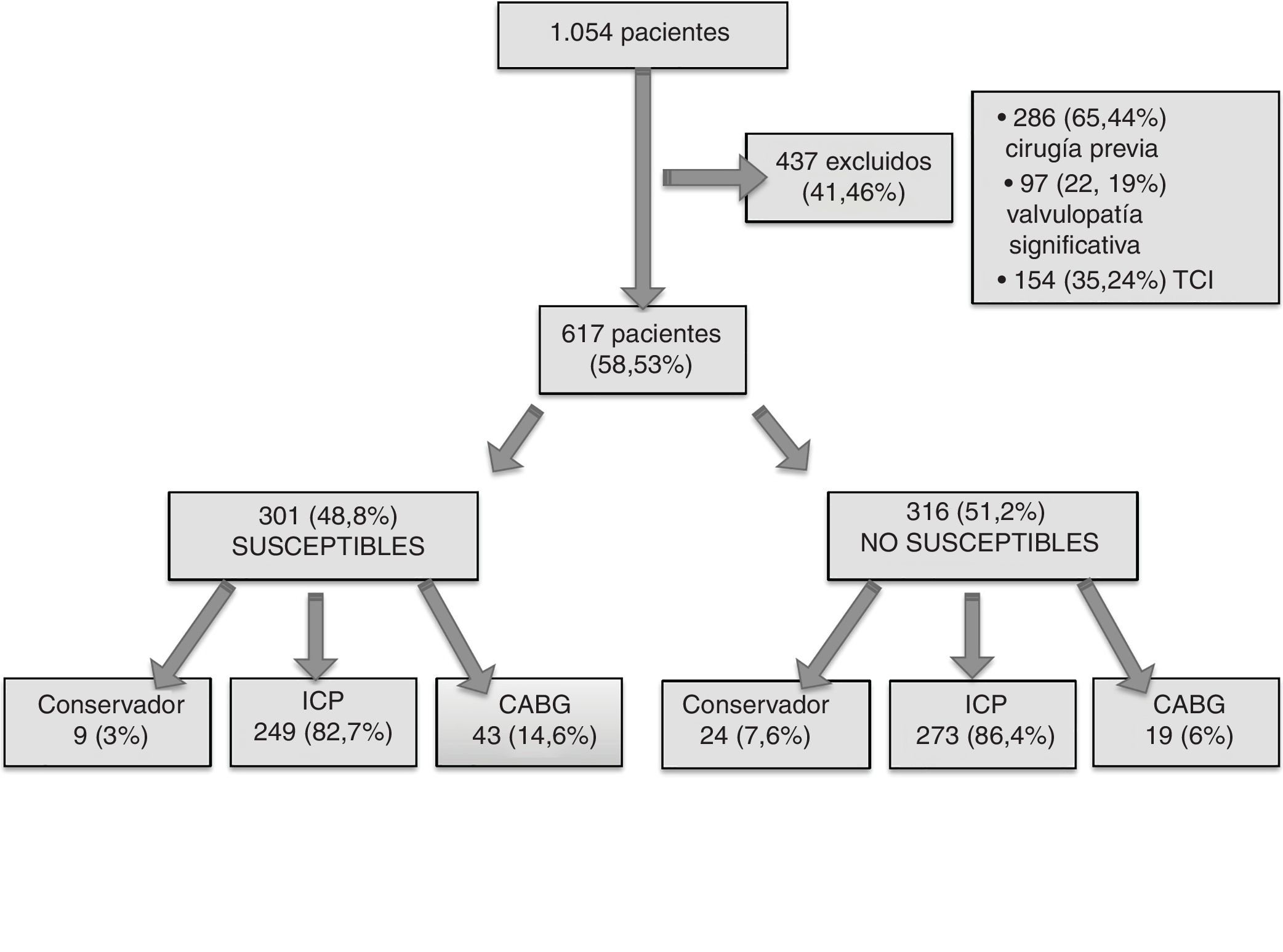
ResultadosDe enero de 2012 a diciembre de 2014 se realizaron 1.011 coronariografías en MVD. Se excluyó del análisis a 394 pacientes (39%) por haberse sometido previamente a cirugía cardiaca (n = 154; 15,24%), presentar valvulopatía significativa susceptible de intervención (n = 117; 11,57%) o presentar afección de TCI (n = 123; 12,16%) (fig. 1).
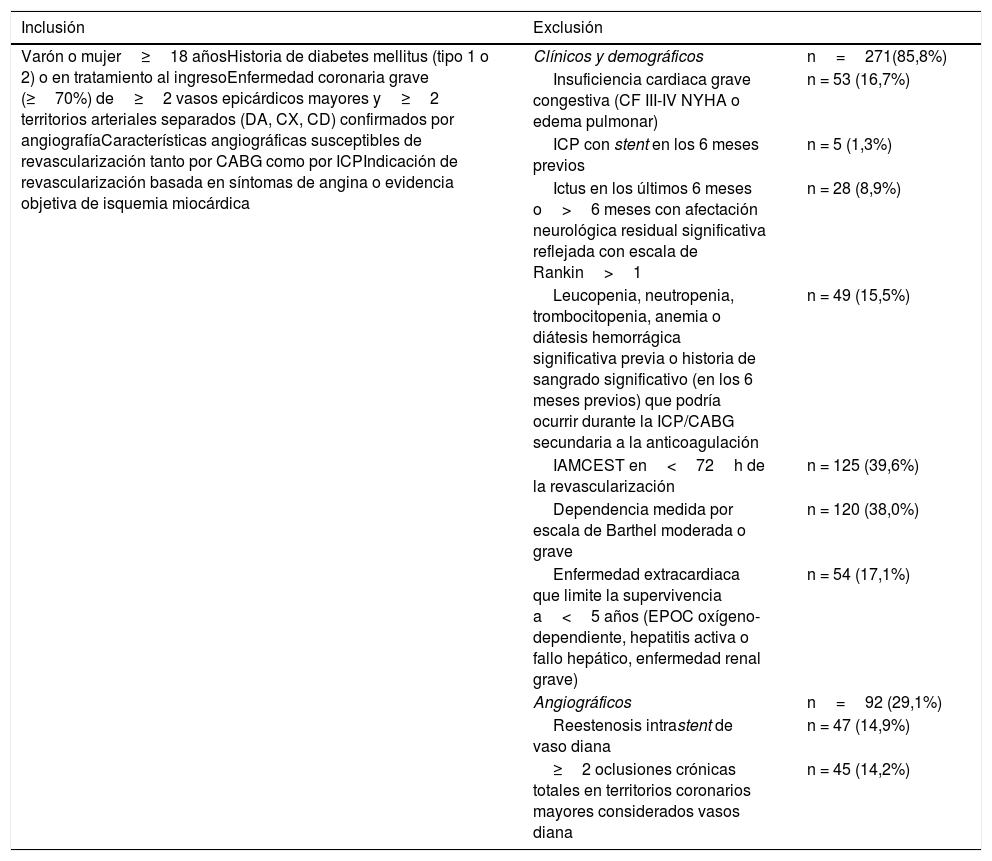
Se estudió a 617 pacientes (58,8% del total), en los que se analizó la estrategia terapéutica seguida (quirúrgica, percutánea o tratamiento médico conservador). De estos pacientes, 301 (48,8%) cumplieron los criterios clínicos de inclusión; el resto se clasificó en el grupo no susceptible, el 85,8% (n = 271) por motivos clínicos y demográficos y el 29,1% (n = 92) por motivos angiográficos; el 43,15% (n =170) no cumplía ninguno de los 2 criterios (tabla 1).
Criterios de inclusión y exclusión
| Inclusión | Exclusión | |
|---|---|---|
| Varón o mujer≥18 añosHistoria de diabetes mellitus (tipo 1 o 2) o en tratamiento al ingresoEnfermedad coronaria grave (≥70%) de≥2 vasos epicárdicos mayores y≥2 territorios arteriales separados (DA, CX, CD) confirmados por angiografíaCaracterísticas angiográficas susceptibles de revascularización tanto por CABG como por ICPIndicación de revascularización basada en síntomas de angina o evidencia objetiva de isquemia miocárdica | Clínicos y demográficos | n=271(85,8%) |
| Insuficiencia cardiaca grave congestiva (CF III-IV NYHA o edema pulmonar) | n = 53 (16,7%) | |
| ICP con stent en los 6 meses previos | n = 5 (1,3%) | |
| Ictus en los últimos 6 meses o>6 meses con afectación neurológica residual significativa reflejada con escala de Rankin>1 | n = 28 (8,9%) | |
| Leucopenia, neutropenia, trombocitopenia, anemia o diátesis hemorrágica significativa previa o historia de sangrado significativo (en los 6 meses previos) que podría ocurrir durante la ICP/CABG secundaria a la anticoagulación | n = 49 (15,5%) | |
| IAMCEST en<72h de la revascularización | n = 125 (39,6%) | |
| Dependencia medida por escala de Barthel moderada o grave | n = 120 (38,0%) | |
| Enfermedad extracardiaca que limite la supervivencia a<5 años (EPOC oxígeno-dependiente, hepatitis activa o fallo hepático, enfermedad renal grave) | n = 54 (17,1%) | |
| Angiográficos | n=92 (29,1%) | |
| Reestenosis intrastent de vaso diana | n = 47 (14,9%) | |
| ≥2 oclusiones crónicas totales en territorios coronarios mayores considerados vasos diana | n = 45 (14,2%) |
CABG: cirugía de revascularización coronaria; CD: arteria coronaria derecha; CF: clase funcional; CX: arteria circunfleja; DA: arteria descendente anterior; EPOC: enfermedad pulmonar obstructiva crónica; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; NYHA: New York Heart Association.
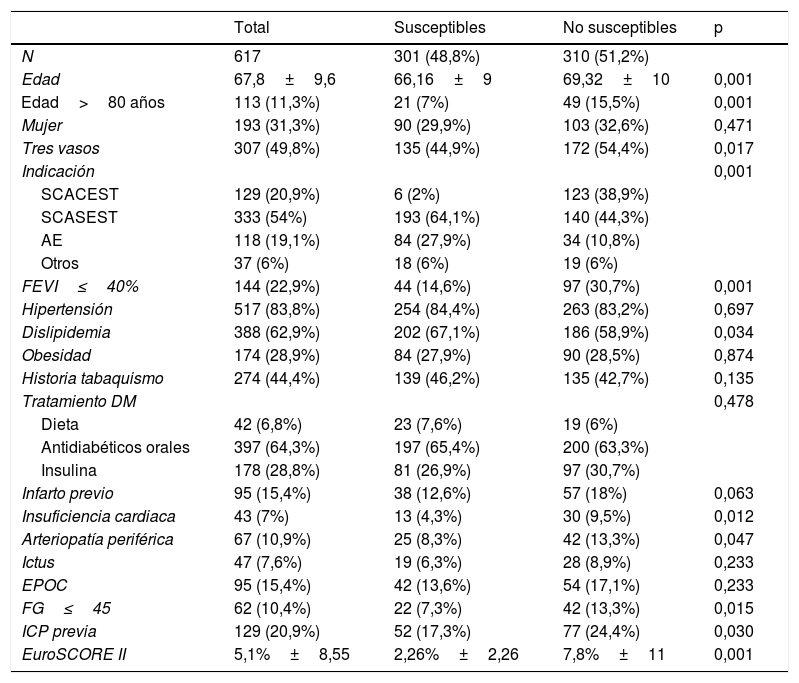
Las características basales del total de los pacientes y de los subgrupos susceptible y no susceptible se muestran en la tabla 2.
Características basales de los pacientes y en función del cumplimiento de criterios
| Total | Susceptibles | No susceptibles | p | |
|---|---|---|---|---|
| N | 617 | 301 (48,8%) | 310 (51,2%) | |
| Edad | 67,8±9,6 | 66,16±9 | 69,32±10 | 0,001 |
| Edad>80 años | 113 (11,3%) | 21 (7%) | 49 (15,5%) | 0,001 |
| Mujer | 193 (31,3%) | 90 (29,9%) | 103 (32,6%) | 0,471 |
| Tres vasos | 307 (49,8%) | 135 (44,9%) | 172 (54,4%) | 0,017 |
| Indicación | 0,001 | |||
| SCACEST | 129 (20,9%) | 6 (2%) | 123 (38,9%) | |
| SCASEST | 333 (54%) | 193 (64,1%) | 140 (44,3%) | |
| AE | 118 (19,1%) | 84 (27,9%) | 34 (10,8%) | |
| Otros | 37 (6%) | 18 (6%) | 19 (6%) | |
| FEVI≤40% | 144 (22,9%) | 44 (14,6%) | 97 (30,7%) | 0,001 |
| Hipertensión | 517 (83,8%) | 254 (84,4%) | 263 (83,2%) | 0,697 |
| Dislipidemia | 388 (62,9%) | 202 (67,1%) | 186 (58,9%) | 0,034 |
| Obesidad | 174 (28,9%) | 84 (27,9%) | 90 (28,5%) | 0,874 |
| Historia tabaquismo | 274 (44,4%) | 139 (46,2%) | 135 (42,7%) | 0,135 |
| Tratamiento DM | 0,478 | |||
| Dieta | 42 (6,8%) | 23 (7,6%) | 19 (6%) | |
| Antidiabéticos orales | 397 (64,3%) | 197 (65,4%) | 200 (63,3%) | |
| Insulina | 178 (28,8%) | 81 (26,9%) | 97 (30,7%) | |
| Infarto previo | 95 (15,4%) | 38 (12,6%) | 57 (18%) | 0,063 |
| Insuficiencia cardiaca | 43 (7%) | 13 (4,3%) | 30 (9,5%) | 0,012 |
| Arteriopatía periférica | 67 (10,9%) | 25 (8,3%) | 42 (13,3%) | 0,047 |
| Ictus | 47 (7,6%) | 19 (6,3%) | 28 (8,9%) | 0,233 |
| EPOC | 95 (15,4%) | 42 (13,6%) | 54 (17,1%) | 0,233 |
| FG≤45 | 62 (10,4%) | 22 (7,3%) | 42 (13,3%) | 0,015 |
| ICP previa | 129 (20,9%) | 52 (17,3%) | 77 (24,4%) | 0,030 |
| EuroSCORE II | 5,1%±8,55 | 2,26%±2,26 | 7,8%±11 | 0,001 |
AE: angina estable; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; FG: filtrado glomerular; ICP: intervención coronaria percutánea; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
Los pacientes no susceptibles eran de mayor edad (69±10 frente a 66±9 años; p < 0,001) y tenían un perfil clínico más desfavorable (mayor frecuencia de historia de infarto e intervencionismo coronario previo, arteriopatía periférica, insuficiencia renal, insuficiencia cardiaca, disfunción ventricular y riesgo quirúrgico más alto medido por EuroSCORE II). La indicación de la coronariografía fue también diferente: más SCA (74,9 frente a 66,1%) y menos angina estable (10,8 frente a 27,9%). Al analizar la anatomía coronaria, el grupo no susceptible presentó un mayor porcentaje de daño de 3 vasos (54,4 frente a 44,9%; p = 0,017) comparado con el grupo susceptible.
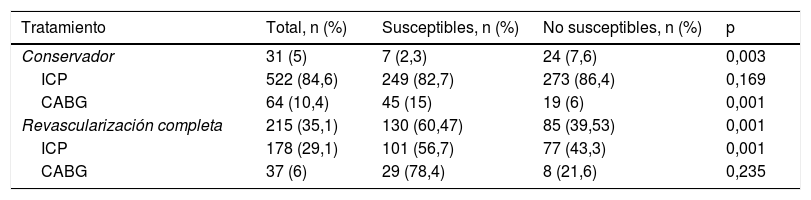
Se revascularizó al 84,6% de los pacientes de forma percutánea, al 10,4% de forma quirúrgica y un 5% recibió tratamiento médico conservador (tabla 3). El grupo no susceptible recibió menos frecuentemente CABG (6 frente a 15%; p < 0,001) y un mayor tratamiento conservador (7,6 frente a 2,3%; p = 0,003).
Distribución de los pacientes en función de su estrategia de tratamiento y si la revascularización fue completa/incompleta
| Tratamiento | Total, n (%) | Susceptibles, n (%) | No susceptibles, n (%) | p |
|---|---|---|---|---|
| Conservador | 31 (5) | 7 (2,3) | 24 (7,6) | 0,003 |
| ICP | 522 (84,6) | 249 (82,7) | 273 (86,4) | 0,169 |
| CABG | 64 (10,4) | 45 (15) | 19 (6) | 0,001 |
| Revascularización completa | 215 (35,1) | 130 (60,47) | 85 (39,53) | 0,001 |
| ICP | 178 (29,1) | 101 (56,7) | 77 (43,3) | 0,001 |
| CABG | 37 (6) | 29 (78,4) | 8 (21,6) | 0,235 |
CABG: cirugía de revascularización coronaria; ICP: intervención coronaria percutánea.
De los pacientes sometidos a ICP, se trataron 2,51±1,27 lesiones en 1,77±0,65 vasos por paciente, sin diferencias entre grupos (p = 0,149); se emplearon stents liberadores de fármacos de nueva generación (everolimus, sirolimus, zotarolimus y biolimus) en el 84,5% de los casos y stents convencionales en el 15,6%. El grupo no susceptible recibió menos porcentaje de stents liberadores de fármacos (79,9 frente a 89,5%; p = 0,032).
A todos los pacientes revascularizados quirúrgicamente se les hizo al menos un injerto arterial, con una media de 2,73±0,66 injertos. Se realizó cirugía sin bomba extracorpórea en el 95% de los casos.
La revascularización fue completa en el 35,1% de los pacientes; dicho porcentaje fue menor en el grupo no susceptible (39,53 frente a 60,47%; p < 0,001) tanto cuando se sometieron a ICP (43,3 frente a 56,7%; p = 0,001) como a CABG (21,6 frente a 78,4%; p=0,262), como se muestra en la tabla 3.
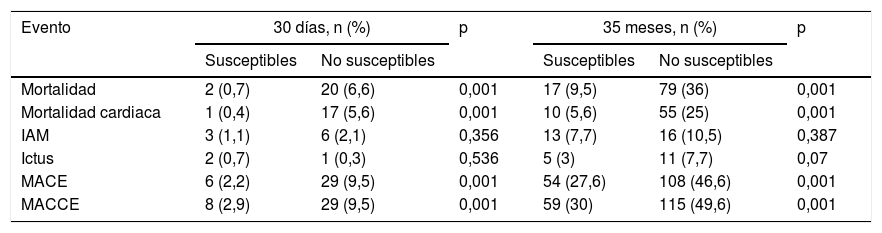
El 94% de los pacientes completaron un seguimiento medio de 35±15 meses. La incidencia de mortalidad, mortalidad cardiaca, infarto no mortal, ictus y eventos combinados MACE y MACCE a 30 días y 35 meses fue significativamente mayor en el grupo no susceptible (tabla 4).
Eventos mayores en el seguimiento a 30 días y 35 meses en susceptibles y no susceptibles
| Evento | 30 días, n (%) | p | 35 meses, n (%) | p | ||
|---|---|---|---|---|---|---|
| Susceptibles | No susceptibles | Susceptibles | No susceptibles | |||
| Mortalidad | 2 (0,7) | 20 (6,6) | 0,001 | 17 (9,5) | 79 (36) | 0,001 |
| Mortalidad cardiaca | 1 (0,4) | 17 (5,6) | 0,001 | 10 (5,6) | 55 (25) | 0,001 |
| IAM | 3 (1,1) | 6 (2,1) | 0,356 | 13 (7,7) | 16 (10,5) | 0,387 |
| Ictus | 2 (0,7) | 1 (0,3) | 0,536 | 5 (3) | 11 (7,7) | 0,07 |
| MACE | 6 (2,2) | 29 (9,5) | 0,001 | 54 (27,6) | 108 (46,6) | 0,001 |
| MACCE | 8 (2,9) | 29 (9,5) | 0,001 | 59 (30) | 115 (49,6) | 0,001 |
IAM: infarto agudo de miocardio; MACCE: evento mayor combinado de muerte, infarto no mortal, necesidad de nueva revascularización e ictus; MACE: evento mayor combinado de muerte, infarto no mortal y necesidad de nueva revascularización.
La mortalidad por cualquier causa en un seguimiento medio de 35 meses fue 4,42 veces más frecuente en el grupo no susceptible (IC95%, 2,75-7,15; p < 0,001), hubo también 4,64 veces más mortalidad de causa cardiaca (IC95%, 2,53-8,51; p < 0,001), 2,24 más riesgo de MACE (IC95%, 1,56-3,2; p < 0,001) y 2,24 veces más riesgo de MACCE (IC95%, 1,59-3,18; p < 0,001).
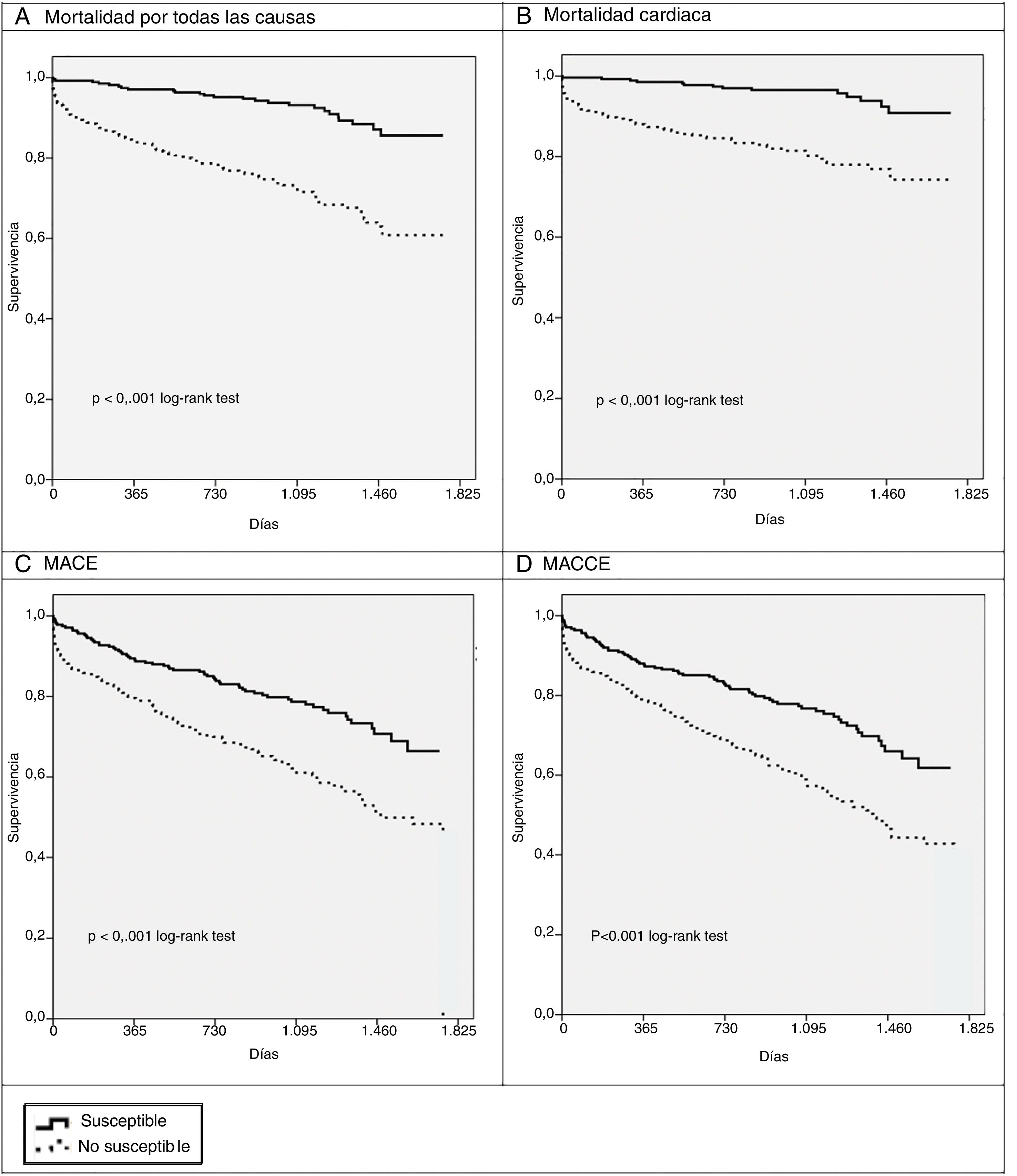
En el análisis de supervivencia, los pacientes del grupo no susceptible presentaron una mayor mortalidad por cualquier causa (HR = 3,916; IC95%, 2,519-6,088; p < 0,001) y por causa cardiaca (HR = 4,45; IC95%, 2,487-7,950; p < 0,001) durante el seguimiento, así como una mayor incidencia de MACE (HR = 1,97; IC95%, 1,46-2,66; p < 0,001) y MACCE (HR = 1,93; IC95%, 1,46-2,56; p < 0,001), como se muestra en la figura 2.
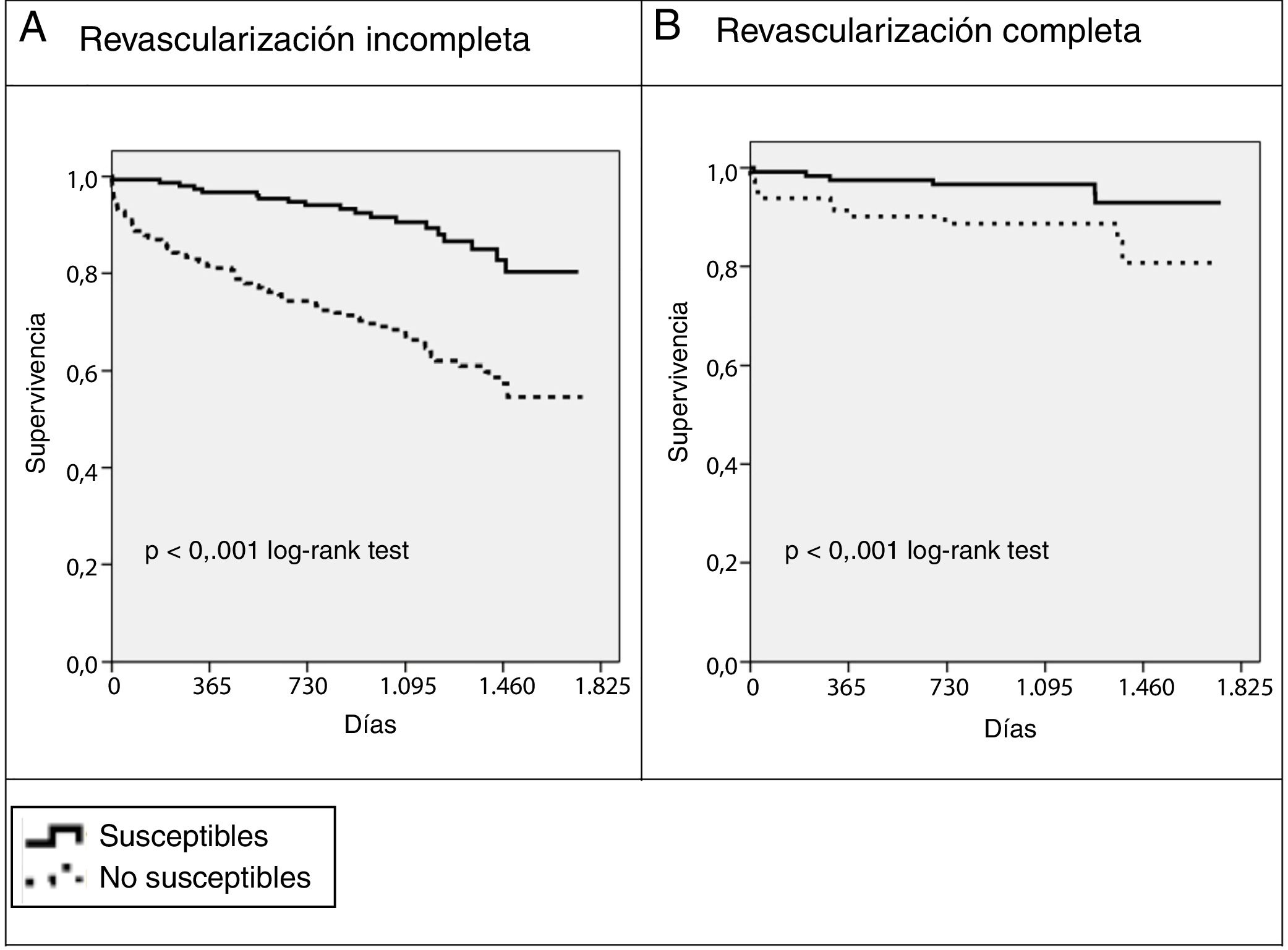
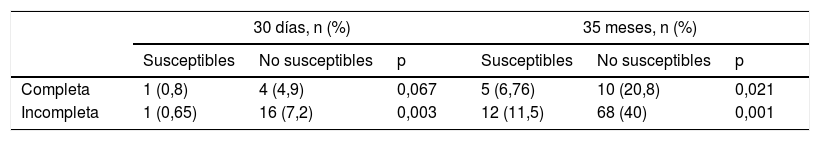
La revascularización completa se asoció a una menor mortalidad a corto y largo plazo de forma global (HR = 0,3; IC95%, 0,18-0,5; p > 0,001) y en los 2 subgrupos (HR = 0,36; IC95%, 0,22-0,61; p < 0,001). Cuando la revascularización fue completa, se redujeron las diferencias entre susceptibles y no susceptibles tanto en mortalidad por cualquier causa (HR = 2,96; IC95%, 1,09-8,0; p = 0,033) como por causa cardiaca (HR = 4,81; IC95%, 0,97-23,86; p = 0,054) (fig. 3 y tabla 5).
Mortalidad a 30 días y 35 meses estratificada en función de revascularización completa/incompleta
| 30 días, n (%) | 35 meses, n (%) | |||||
|---|---|---|---|---|---|---|
| Susceptibles | No susceptibles | p | Susceptibles | No susceptibles | p | |
| Completa | 1 (0,8) | 4 (4,9) | 0,067 | 5 (6,76) | 10 (20,8) | 0,021 |
| Incompleta | 1 (0,65) | 16 (7,2) | 0,003 | 12 (11,5) | 68 (40) | 0,001 |
En el análisis multivariable, la mortalidad se asoció independientemente con el no cumplimiento de criterios (HR = 2,77; IC95%, 1,77-4,37; p = 0,001), la revascularización incompleta (HR = 2,46; IC95%, 1,46-4,13; p = 0,001), la situación clínica (HR = 1,34; IC95%, 1,15-1,67, p = 0,001) y la edad (HR = 1,04; IC95%, 1,02-1,06; p < 0,001).
DiscusiónEste trabajo destaca varios aspectos: a) más de la mitad de los pacientes con MVD en los que se plantea tomar una decisión sobre la mejor estrategia de revascularización no serían incluibles en el estudio FREEDOM, fundamento de las guías de práctica clínica en este campo; b) su pronóstico es mucho peor, más del cuádruple de probabilidad de presentar eventos durante un periodo de tiempo similar, y c) realizar una revascularización coronaria completa podría mejorar el pronóstico de todos los pacientes.
Existen numerosas barreras que impiden reproducir los resultados de los ensayos clínicos en el mundo real por razones muy diversas, por lo que cobra importancia la necesidad de registros tanto en el campo de la cardiología general20 como en el de la revascularización coronaria en particular21; la calidad de los existentes es muy discutible, lo cual limita la información aportada22.
La evidencia científica actual apoya la CABG como la mejor estrategia de revascularización miocárdica en MVD10. Sin embargo, se sabía que un elevado porcentaje de los pacientes con enfermedad coronaria a los que se atiende no serían incluibles en los grandes ensayos clínicos17,23 y, al igual que en nuestra serie, son de mayor edad y con un perfil de riesgo más elevado. No obstante, se desconoce el número de pacientes no incluibles en ensayos clínicos en aquellos con MVD de la época contemporánea, que como se muestra en el presente manuscrito, es también muy elevado (el 70% de todos los MVD y el 51% si se excluye la CABG previa o la valvulopatía grave con indicación quirúrgica por la misma y enfermedad del TCI), congruente con lo documentado por el Registro British Columbia de Canadá15, en el que de 6.830 pacientes que presentan SCA solo 4.661 hubieran cumplido criterios de inclusión. Aunque el conjunto de características que definen al grupo no susceptible son factores de mal pronóstico, en el presente trabajo se optó por excluir a los pacientes que presentaban enfermedad de TCI, valvulopatía significativa con indicación quirúrgica y cirugía cardiaca previa para minimizar la heterogeneidad de los resultados y posibles factores de confusión. La afección de TCI se asocia a más morbimortalidad por la gran cantidad de miocardio en riesgo, y su diagnóstico24 y tratamiento son controvertidos a la luz de los resultados de los ensayos clínicos10, y más aún en los diabéticos, escasamente representados25,26. En presencia de valvulopatía significativa, la revascularización percutánea no está indicada para reducir eventos perioperatorios cardiacos27. Finalmente, se excluyó a los pacientes sometidos previamente a cirugía cardiaca, pues son un cajón de sastre con indicaciones más dudosas, la relación de causalidad síntomas-hallazgos es compleja y las herramientas de medición del riesgo son siempre mayores por razones múltiples28,29.
Con el incremento de la prevalencia de diabetes y la esperanza de vida de la población y la tendencia al tratamiento invasivo, ha aumentado el número de pacientes con peor perfil en las salas de hemodinámica, lo que ha llevado a optar principalmente por el tratamiento percutáneo de sus lesiones, dado su alto riesgo quirúrgico o su fragilidad. Aunque la indicación quirúrgica en el presente trabajo sea menor de lo esperado, es razonable pensar que se deba a una derivación muy seleccionada de pacientes (aquellos con perfil clínico más favorable, principalmente con enfermedad de 3 vasos y todos ellos con afección de la descendente anterior). Cuando se compara con el resto del territorio nacional, aunque no se dispone de datos específicos sobre diabéticos, se observa que el número de ICP multivaso en 2017 ascendió a 13.31330, mientras que la CABG fue de 5.02931 (más del doble) con ratios ICP/CABG distintos por comunidades autónomas32, por lo que en muchos casos la individualización del tratamiento no viene regida por criterios médicos, sino de disponibilidad del medio donde se trata a los enfermos33,34.
Esta tendencia también se ha observado en el registro estadounidense NCDR Action Registry-GWTG14 con pacientes agudos, en el que hubo una diferencia amplia entre centros a la hora de derivar a los pacientes a CABG frente a ICP (0-78 frente a 22-100%; p< 0,0001), influidos principalmente por las comorbilidades y la gravedad de las lesiones coronarias, al igual que en el Registro British Columbia15 de pacientes agudos, en el que el 60% de los pacientes fueron sometidos a ICP. Es, por tanto, habitual en la práctica clínica no aplicar taxativamente el modelo de riesgo derivado de los resultados de los ensayos clínicos, que no contempla adecuadamente el nivel de complejidad de los pacientes. Desde mediados de 2013, herramientas como las escalas Syntax35, la Syntax residual36 y la Syntax II37 se han aproximado a la estimación teórica del riesgo en estos pacientes, aunque la población de DMV estaba escasamente representada, apenas un 30% de los pacientes, e incluía en el análisis a personas con enfermedad de TCI. En nuestro estudio no se tuvieron en cuenta dichas escalas, dado que su uso aún no estaba extendido en el periodo histórico del presente trabajo.
Otra de las conclusiones que extrae este trabajo, aunque con escasa potencia, es cómo a los pacientes de peor perfil (no susceptibles) se les realiza menos revascularización completa, a veces fundamentado en este mismo hecho, lo que contribuye a su peor pronóstico pese a la evidencia actual38; las diferencias se redujeron al comparar grupos y estrategias terapéuticas cuando la revascularización fue completa.
Es en este contexto del mundo real donde la eficacia (lo demostrado en ensayos multicéntricos con pacientes seleccionados) no se traduce necesariamente en efectividad, lo que evidencia la necesidad de registros bien diseñados y estudios con «pacientes no seleccionados» que completen la información científica disponible.
LimitacionesSe trata de un registro unicéntrico retrospectivo a partir de las bases de datos locales que recoge pacientes derivados a coronariografía procedentes de diferentes puntos geográficos, incluidos pacientes extranjeros, lo que propicia cierta pérdida de seguimiento.
Los datos de los pacientes sometidos a CABG no corresponden al total de los pacientes operados por el servicio de cirugía cardiaca, dado que se excluyó a aquellos diagnosticados de enfermedad coronaria de 2 o más vasos en otros centros sin cirugía, lo cual limitó el tamaño muestral y la potencia del trabajo.
ConclusionesEn la vida real, más de la mitad de los pacientes no hubieran sido elegibles para participar en un ensayo clínico como el estudio FREEDOM. Dado su perfil, el pronóstico de dichos pacientes es peor, con una mayor mortalidad y con más eventos cardiovasculares mayores, independientemente de si la revascularización fue completa o no. Dichas características llevan a los cardiólogos y miembros del equipo multidisciplinar a recomendar de forma individualizada qué estrategia de revascularización es la más idónea para cada paciente, con la que obtener los mejores resultados para el paciente según su situación determinada.
- -
La diabetes se asocia a una morbimortalidad aumentada de origen cardiovascular con más afección coronaria multivaso.
- -
Diversos estudios sentaron la indicación de CABG como la primera opción en MVD, aunque determinados subgrupos mostraron eventos similares en poblaciones seleccionadas.
- -
El estudio FREEDOM concluye que la CABG es superior a la PCI en la reducción de muerte e infarto agudo de miocardio, base de las últimas guías de revascularización.
- -
Los pacientes del mundo real no están bien representados en los ensayos clínicos, por lo que en la práctica diaria no siempre se tratan según las guías de actuación clínica.
- -
Más de la mitad de los MVD no serían incluibles en un gran ensayo clínico, ya que presentan un peor pronóstico.
- -
En nuestro medio se opta principalmente por la ICP como estrategia de revascularización, pese a las guías de práctica clínica.
- -
Los pacientes con un peor perfil reciben menos revascularización completa, pese a estar relacionada con un mejor pronóstico, independiente del riesgo.
- -
Surge la necesidad de registros nacionales auditados como herramienta de conocimiento y control de resultados de los diferentes centros.
Los autores declaran no tener ningún conflicto de intereses.