Si bien la utilización de anticoagulantes orales directos (ACOD) en pacientes con fibrilación auricular (FA) y prótesis valvular biológica como alternativa a los antagonistas de la vitamina K (AVK) está recogida en las guías, en la práctica real son escasos los estudios que recogen estos pacientes, más aún en nuestro país, dadas las restricciones que existen a su prescripción.
MétodosSe analizó a los pacientes intervenidos de forma consecutiva en nuestro hospital de sustitución valvular aórtica por prótesis biológica con indicación de anticoagulantes orales por FA durante los años 2013-2018. Comparamos características clínicas basales, así como tasas de eventos cerebrovasculares, hemorragias mayores y menores, y mortalidad de los tratados con ACOD frente a los tratados con AVK.
ResultadosIncluimos 132 pacientes tratados con AVK (62,6%) y 79 con ACOD (37,4%; apixabán 20%, edoxabán 10%, rivaroxabán 6% y dabigatrán 3%). No hubo diferencias significativas en sus características clínicas basales en cuanto a edad, sexo, función renal o escalas de riesgo embólico. El seguimiento medio fue de 32,85±15 meses. La tasa de incidencia de ictus isquémico/accidente isquémico transitorio (AIT) fue de 1,5/100 pacientes/año en el grupo ACOD frente a 1,32 en AVK. La tasa de incidencia de sangrado mayor fue de 2,02/100 pacientes/año en el grupo ACOD frente a 3,7 en AVK. Los pacientes con AVK presentaron 6 ictus hemorrágicos frente a ninguno en el grupo de pacientes con ACOD.
ConclusionesLa utilización de ACOD en pacientes con prótesis cardiaca biológica e indicación de ACO permanente por FA parece una alternativa eficaz y segura al uso de AVK.
Although the usage of direct oral anticoagulants (DOAC) in patients with atrial fibrillation (AF) and bioprosthesis is already accepted in recent guidelines as an alternative to vitamin K antagonists (VKA), real world data in this scenario remain scarce, even more in our country.
MethodsA retrospective single-center study that included all consecutive patients who underwent aortic valve replacement with bioprosthetic heart valve from 2013 to 2018, with oral anticoagulation initiated because of AF. The rates of occurrence of thromboembolic events (ischemic stroke, transient ischemic attack), major and minor although clinically relevant bleed, intracranial hemorrhage and death were assessed in patients on DOAC vs VKA.
ResultsA total of 132 patients on VKA (62.6%) and 79 on DOACs (37.4%; apixaban 20%, edoxaban 10%, rivaroxaban 6% and dabigatran 3%) were included in the study. There were no significant differences in baseline clinical characteristics (age, sex, renal function or embolic risk scales). Mean follow-up was 32.85±15 months. The incidence-rates of cerebrovascular/thromboembolic events were 1.5/100 persons-year in the DOAC group 1.32 in the VKA group. The incidence-rates of major bleed 2.02/100 persons-year in DOACs group vs 3.7 in VKA group. Patients in the VKA group experienced 6 intracranial hemorrhages vs none in the DOAC group.
ConclusionsAccording to our data from clinical practice, DOAC in patients with AF and a bioprosthetic heart valve seem to be a safe and effective alternative to VKA.
Actualmente, los anticoagulantes orales directos (ACOD) se consideran fármacos de primera elección en los pacientes con fibrilación auricular (FA) no valvular1,2. Sin embargo, el término «no valvular» ha resultado controvertido, con diferentes definiciones adoptadas en los ensayos clínicos de los distintos ACOD, e incluso en las guías de práctica clínica3. Los últimos consensos establecen como FA valvular la que se da en pacientes con estenosis mitral moderada-grave o prótesis valvular mecánica, con indicación de anticoagulación permanente con antagonistas de la vitamina K (AVK). La FA no valvular, por tanto, incluye el resto de casos, representados en diversos grados en los ensayos clínicos de los diferentes ACOD, algunos de los cuales incluyeron pacientes con reparaciones valvulares, valvuloplastias y bioprótesis, si bien en escaso número. En función de esto, las últimas guías de manejo clínico consideran aceptable el uso de ACOD en pacientes con prótesis valvular biológica, aunque en la práctica real son escasos los estudios que recogen estos pacientes4. Esta situación es aún más marcada en nuestro país a causa de las restricciones que existen a su prescripción.
El objetivo del presente estudio es evaluar la seguridad y la eficacia del tratamiento con ACOD en una cohorte de pacientes portadores de sustitución valvular aórtica por bioprótesis, con necesidad de anticoagulación oral (ACO) por FA, y comparar su evolución clínica con la de los pacientes tratados con AVK.
MétodosPacientesSe diseñó un registro observacional de carácter retrospectivo, en el que se incluyó a todos los pacientes intervenidos de sustitución valvular aórtica por prótesis biológica con indicación de ACO por FA en nuestro hospital en los años 2013-2018. Se obtuvo consentimiento informado de los mismos y aprobación por el comité ético del centro. El único criterio de exclusión aplicado fue el fallecimiento durante el ingreso. Los datos relativos a las características clínicas basales y detalles quirúrgicos se recogieron de forma prospectiva en una base de datos quirúrgica. Los datos del seguimiento se obtuvieron de la revisión de las notas de consulta ambulatoria o ingresos hospitalarios. En pacientes procedentes de otras regiones, se completó con contacto telefónico en los casos que no continuaron las revisiones en nuestro centro. La elección del régimen de ACO estuvo siempre sujeta al criterio del médico responsable del paciente.
DefinicionesA efectos de nuestro estudio, accidente cerebrovascular se define como déficit neurológico de al menos 24h de duración, sin datos de hemorragia en las pruebas de neuroimagen, y accidente isquémico transitorio (AIT) como aquel de <24h de duración, ambos diagnosticados por el servicio de neurología. Se define sangrado mayor como sangrado mortal o sintomático en un órgano crítico, o sangrado que supone un descenso de los niveles de hemoglobina >2g/dl o necesidad de transfusión. Se ha considerado sangrado menor clínicamente relevante aquel que, no cumpliendo criterios de sangrado mayor, ha requerido intervención médica, interrupción temporal de la ACO o alteración de la actividad básica diaria5.
Análisis estadísticoEl análisis estadístico se realizó con SPSS versión 15.0 (SPSS Inc., EE. UU.). Las variables continuas se presentan como media ± desviación estándar. Las comparaciones entre grupos se realizaron con la prueba de la t de Student o la U de Mann-Whitney. Las variables categóricas se analizaron con la prueba Chi-cuadrado. El estudio de supervivencia se realizó según el método de Kaplan-Meier, utilizando el test de log-rank para la comparación de grupos. Todos los análisis fueron bilaterales, y se consideraron estadísticamente significativos aquellos con p<0,05. Se consideró como tiempo 0 el inicio de la ACO, o bien el momento de su reintroducción tras la cirugía en los pacientes anticoagulados previamente por FA anterior a la indicación quirúrgica.
ResultadosCaracterísticas basalesPresentaron indicación de ACO por FA concomitante 220 pacientes intervenidos de sustitución valvular aórtica por bioprótesis en nuestro centro entre 2013 y 2018. De ellos, 9 se excluyeron del estudio, 7 por rechazar la ACO y los 2 restantes por trasladarse a otras provincias, perdiéndose el seguimiento más allá de los primeros 6 meses.
Incluimos así 211 pacientes (edad media 76,6±7,8 años), 117 varones (56%); 58 de ellos presentaban FA anticoagulada antes de la intervención (27,5%); en el resto de casos apareció a lo largo del seguimiento (tiempo medio al inicio 12,1±1,8 meses tras la intervención). La cirugía consistió en el reemplazo valvular aórtico aislado en 137 casos (64,9%), la mayoría por estenosis aórtica grave. En 3 casos el motivo fue la degeneración de la válvula protésica previa, y en 10 casos la regurgitación aórtica. Este reemplazo valvular aórtico se asoció en 4 casos a implante de tubo valvulado, en 48 casos a pontaje aortocoronario (22,9%) y en 22 a intervención (reparación o sustitución) sobre la válvula mitral (10,4%).
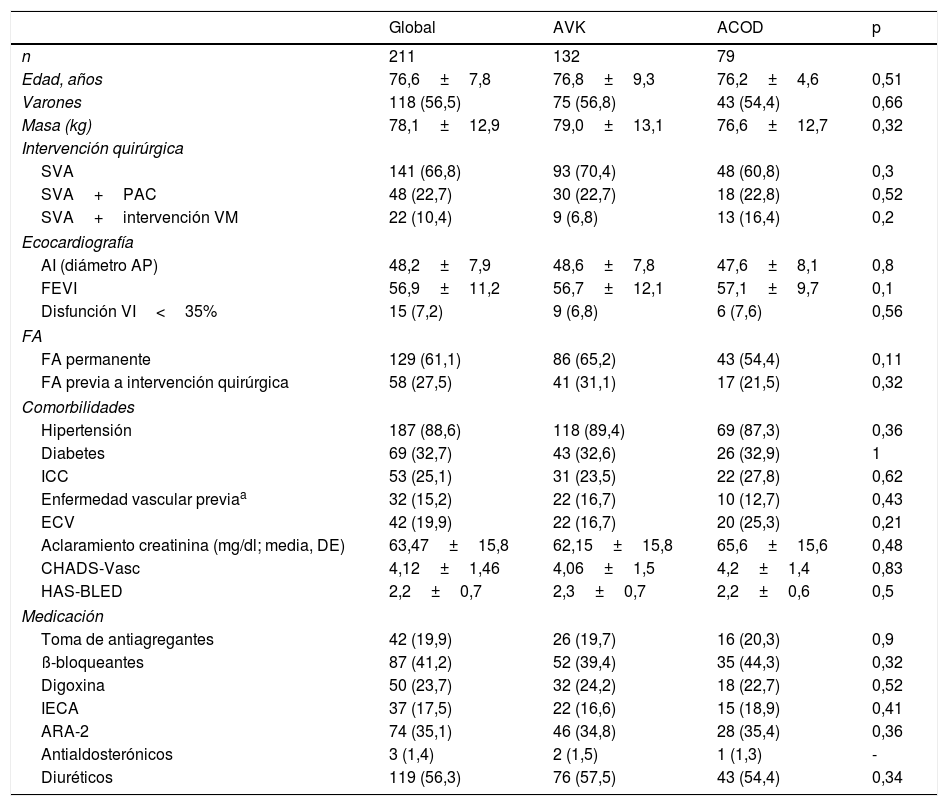
Régimen de anticoagulación oralUn total de 132 pacientes (62,6%) iniciaron ACO con AVK, y 79 (37,4%) con ACOD (apixabán 41 [19%]; edoxabán 20 [9%]; rivaroxabán 11 [5%] y dabigatrán 7 [3%]). De los pacientes con FA previa a la intervención, 17 (29,3%) se encontraban bajo ACOD, y 15 de ellos la mantuvieron ininterrumpidamente tras la intervención (en otros 2 casos, se cambió a AVK antes del alta hospitalaria). Las características basales de pacientes, tanto de la población global como de aquellos con tratamiento con AVK y ACOD, se muestran en la tabla 1.
Características basales de los pacientes incluidos en el estudio
| Global | AVK | ACOD | p | |
|---|---|---|---|---|
| n | 211 | 132 | 79 | |
| Edad, años | 76,6±7,8 | 76,8±9,3 | 76,2±4,6 | 0,51 |
| Varones | 118 (56,5) | 75 (56,8) | 43 (54,4) | 0,66 |
| Masa (kg) | 78,1±12,9 | 79,0±13,1 | 76,6±12,7 | 0,32 |
| Intervención quirúrgica | ||||
| SVA | 141 (66,8) | 93 (70,4) | 48 (60,8) | 0,3 |
| SVA+PAC | 48 (22,7) | 30 (22,7) | 18 (22,8) | 0,52 |
| SVA+intervención VM | 22 (10,4) | 9 (6,8) | 13 (16,4) | 0,2 |
| Ecocardiografía | ||||
| AI (diámetro AP) | 48,2±7,9 | 48,6±7,8 | 47,6±8,1 | 0,8 |
| FEVI | 56,9±11,2 | 56,7±12,1 | 57,1±9,7 | 0,1 |
| Disfunción VI<35% | 15 (7,2) | 9 (6,8) | 6 (7,6) | 0,56 |
| FA | ||||
| FA permanente | 129 (61,1) | 86 (65,2) | 43 (54,4) | 0,11 |
| FA previa a intervención quirúrgica | 58 (27,5) | 41 (31,1) | 17 (21,5) | 0,32 |
| Comorbilidades | ||||
| Hipertensión | 187 (88,6) | 118 (89,4) | 69 (87,3) | 0,36 |
| Diabetes | 69 (32,7) | 43 (32,6) | 26 (32,9) | 1 |
| ICC | 53 (25,1) | 31 (23,5) | 22 (27,8) | 0,62 |
| Enfermedad vascular previaa | 32 (15,2) | 22 (16,7) | 10 (12,7) | 0,43 |
| ECV | 42 (19,9) | 22 (16,7) | 20 (25,3) | 0,21 |
| Aclaramiento creatinina (mg/dl; media, DE) | 63,47±15,8 | 62,15±15,8 | 65,6±15,6 | 0,48 |
| CHADS-Vasc | 4,12±1,46 | 4,06±1,5 | 4,2±1,4 | 0,83 |
| HAS-BLED | 2,2±0,7 | 2,3±0,7 | 2,2±0,6 | 0,5 |
| Medicación | ||||
| Toma de antiagregantes | 42 (19,9) | 26 (19,7) | 16 (20,3) | 0,9 |
| ß-bloqueantes | 87 (41,2) | 52 (39,4) | 35 (44,3) | 0,32 |
| Digoxina | 50 (23,7) | 32 (24,2) | 18 (22,7) | 0,52 |
| IECA | 37 (17,5) | 22 (16,6) | 15 (18,9) | 0,41 |
| ARA-2 | 74 (35,1) | 46 (34,8) | 28 (35,4) | 0,36 |
| Antialdosterónicos | 3 (1,4) | 2 (1,5) | 1 (1,3) | - |
| Diuréticos | 119 (56,3) | 76 (57,5) | 43 (54,4) | 0,34 |
Los datos expresan n (%) o media±desviación estándar.
ACOD: anticoagulante oral directo; AI: aurícula izquierda; ARA-2: antagonistas del receptor de la angiotensina-2; AVK: antagonista de la vitamina K; DE: desviación estándar; ECV: enfermedad cerebrovascular previa; FA: fibrilación auricular; ICC: insuficiencia cardíaca; IECA: inhibidores de la enzima convertidora de angiotensina; PAC: pontaje aorto-coronario; SVA: sustitución valvular aórtica; VM: válvula mitral.
En un 60% de los pacientes bajo tratamiento con AVK se dispuso de controles de INR accesibles suficientes para evaluar el tiempo en rango terapéutico, calculado según el método de Rosendaal et al.6. La media resultó del 56,7%, con un 31% de pacientes >70%.
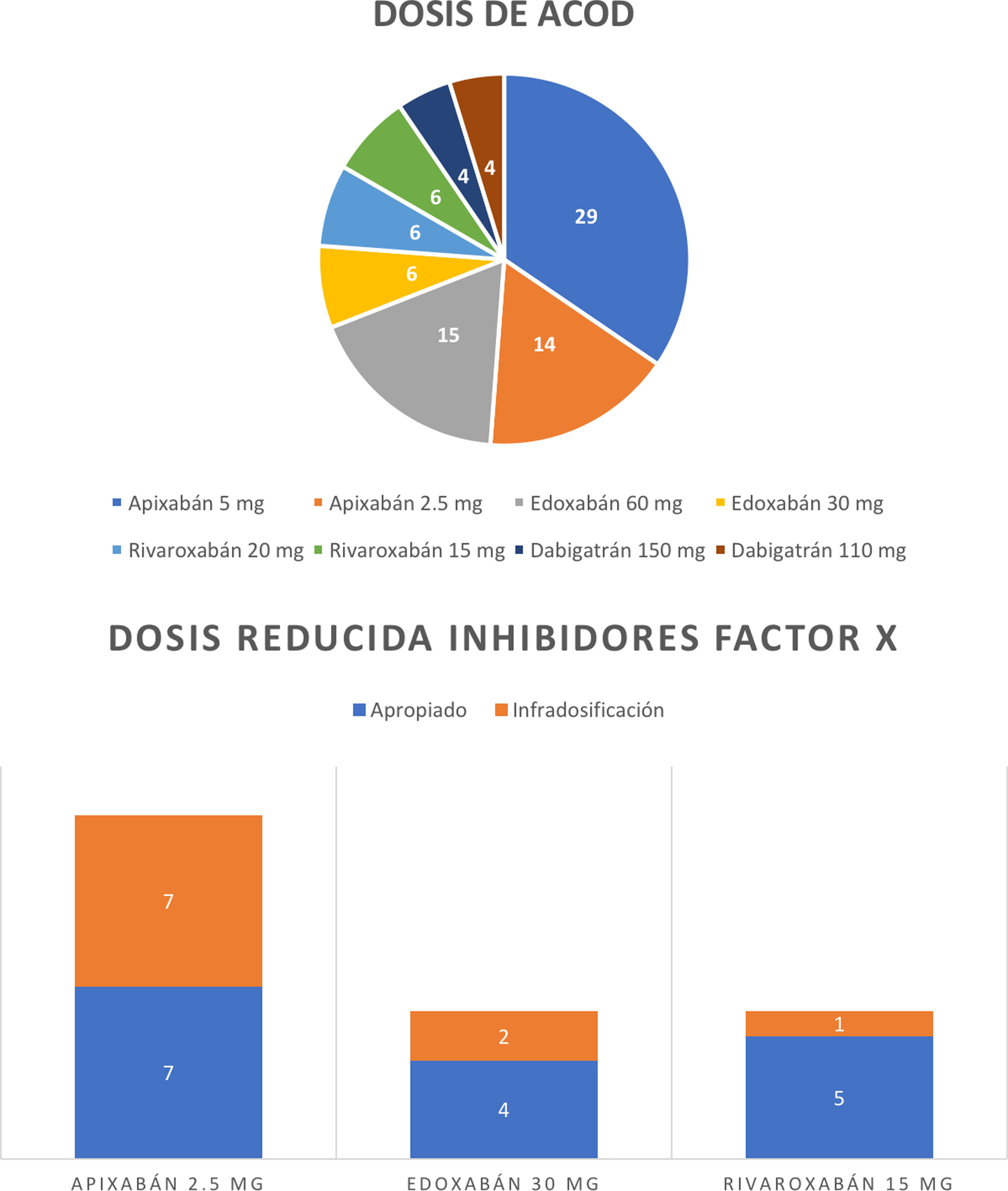
La elección de dosis de los ACOD estuvo siempre sujeta al criterio del médico responsable del paciente. En cuanto a la adecuación de la dosificación a la baja de los distintos ACOD inhibidores del factor X en los que este criterio es aplicable según las recomendaciones de la Agencia Española de Medicamentos, se observó que en 10 pacientes de los 26 (38,5%) tratados con reducción de dosis no se cumplían estrictamente estas recomendaciones, fundamentalmente en los tratados con apixabán (7/14; 50%) (fig. 1).
Distribución de dosis de ACOD. La Agencia Española de Medicamentos recomienda la dosis reducida en los siguientes casos: apixabán, en pacientes con filtrado glomerular de 15-29ml/min, y en aquellos con al menos 2 de las siguientes características: edad ≥80 años, peso corporal ≤60kg o creatinina sérica ≥1,5mg/dl (133μmol/l); edoxabán, en filtrados glomerulares <50ml/min, si peso ≤60kg o uso concomitante de inhibidores potentes de P-gp; rivaroxabán, en pacientes con filtrados glomerulares <50ml/min; dabigatrán, en edad >80 años, insuficiencia renal moderada (aclaramiento de creatinina <50ml/min) y/o edad entre 75-79 años cuando el riesgo hemorrágico es alto, o tratamiento con verapamilo.
Un total de 7 pacientes tratados inicialmente con AVK (5,3%) cambiaron a ACOD, en 3 casos por labilidad de INR, con tiempos <50% en rango terapéutico; en 3 casos por hemorragia mayor (2 hemorragias subaracnoideas y una hemorragia digestiva baja); en el caso restante, por ictus isquémico de perfil embólico.
De los pacientes tratados inicialmente con ACOD, 3 (3,8%) cambiaron a AVK, 2 de ellos por empeoramiento de la función renal y el tercero tras un episodio de hemorragia digestiva baja, para volver a ACOD después de iniciar un tratamiento de quimioterapia por el inicio tumoral, con una marcada inestabilidad subsiguiente de los valores de INR.
Eventos isquémicos y hemorrágicosEl seguimiento medio fue de 32,85±15,8 meses. Los eventos se resumen en la tabla 2. Un total de 8 pacientes experimentaron un evento cerebrovascular agudo de perfil embólico (tiempo medio a evento de 10,7±7 meses); 5 en el grupo de AVK (2 accidentes cerebrovasculares y 3 AIT) y 3 en el grupo ACOD (un accidente cerebrovascular y 2 AIT). La incidencia acumulada de ictus/AIT en los grupos AVK y ACOD fue, respectivamente, del 3,8% frente al 3,7% (p=0,85), con una tasa de incidencia de 1,32 por 100 personas/año en el grupo AVK frente a 1,5 por 100 personas/año en el grupo ACOD. Además de estos eventos cerebrovasculares, 3 pacientes del grupo AVK experimentaron embolias periféricas. Incluyendo estas, el total de eventos embólicos con AVK fue del 6% (2,08 por 100 pacientes/año). Señalar, además, que 3 pacientes AVK y 2 ACOD con historia de cardiopatía isquémica (y pontaje coronario en 3 de ellos) presentaron infarto agudo de miocardio.
Incidencia acumulada de las variables a estudio
| Evento (n, %) | AVK | ACOD | Valor de p |
|---|---|---|---|
| Evento cerebrovascular agudo —ictus, AIT— | 5 (3,8) | 3 (3,7) | 0,85 |
| Sangrado mayor | 14 (10,6) | 4 (5) | 0,2 |
| Ictus hemorrágico | 6 (4,5) | 0 | 0,07 |
| Sangrado menor (clínicamente relevante) | 13 (9,8) | 8 (10) | 0,9 |
Los datos expresan n (%).
ACOD: anticoagulante oral directo; AIT: accidente isquémico transitorio; AVK: antagonista de la vitamina K.
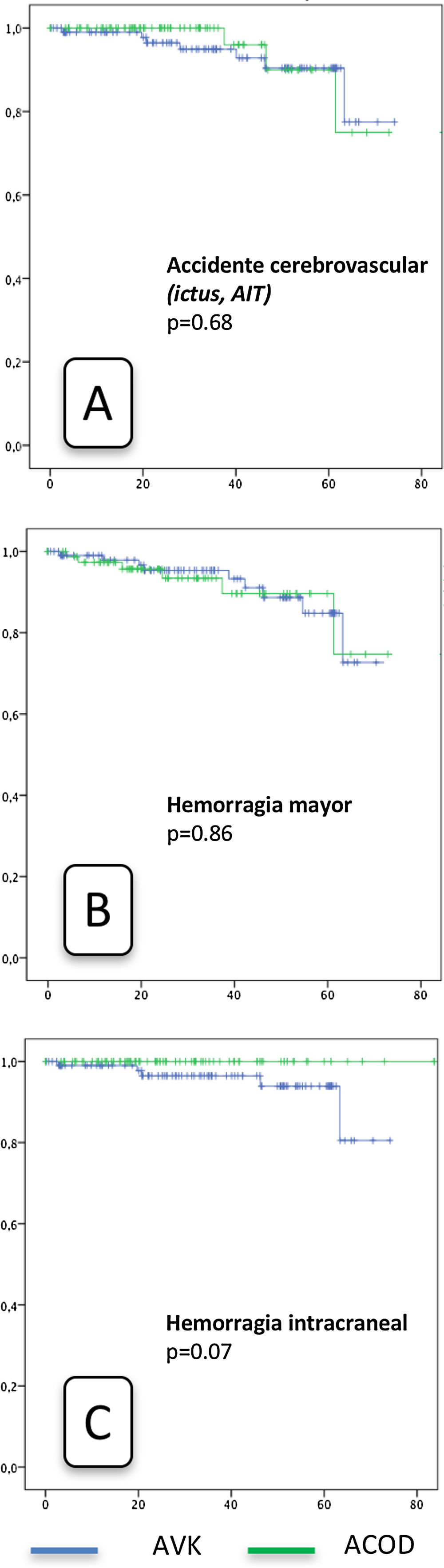
Se produjeron sangrados mayores en 14 pacientes del grupo AVK y en 4 pacientes ACOD (10,6%; 3,7 por 100 pacientes/año frente al 5%; 2,02 por 100 pacientes/año; p=0,2) (tiempo medio 17,5±9,4 meses). Cabe destacar entre ellos 6 hemorragias intracraneales en el grupo AVK que supusieron el fallecimiento de 4 pacientes, con ningún caso en el grupo ACOD (p=0,07). El resto de hemorragias mayores se debieron a hemorragias digestivas, a excepción de un taponamiento cardiaco en un paciente bajo AVK. Los ictus hemorrágicos se desglosan en 3 hematomas subdurales, 2 hemorragias intraparenquimatosas y una hemorragia subaracnoidea espontánea.
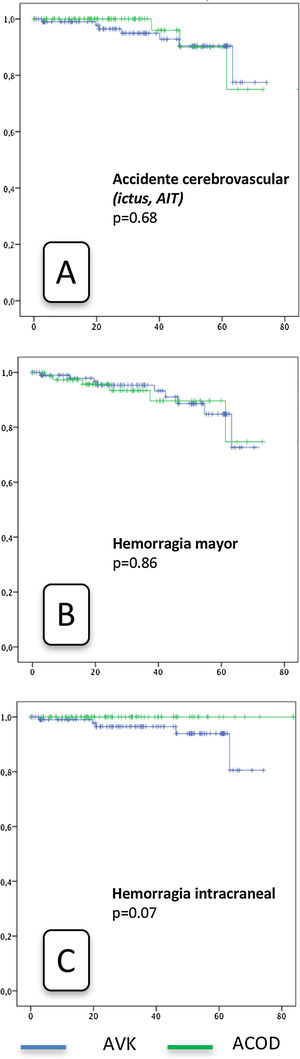
Las curvas de supervivencia acumulada libre de eventos no mostraron diferencias significativas entre grupos (fig. 2).
Finalmente, 13 pacientes con AVK y 8 pacientes con ACOD experimentaron hemorragias menores (9,8%; 3,4 por 100 pacientes/año frente al 10%; 4,1 por 100 pacientes/año; p=0,9).
Sí existieron diferencias significativas en la mortalidad total. En el grupo tratado con AVK se produjeron 24 (18,5%) muertes, de las cuales 15 tuvieron causa cardiovascular7 (muerte súbita en 2 casos e insuficiencia cardiaca en 9, además de las 4 hemorragias intracraneales reseñadas), y el resto por diversas comorbilidades (procesos infecciosos en 10 casos; neoplasia en 3; enfermedad renal terminal en uno; demencia avanzada en uno), siendo desconocida la causa del fallecimiento en 3 pacientes. De 5 pacientes fallecidos con ACOD (6,32%; p=0,014), en un caso no se identificó la causa, el resto se debieron a procesos infecciosos.
Pacientes con inicio de anticoagulantes orales directos <3 meses tras reemplazo valvularUn total de 29 pacientes (edad media 75,3±4,6 años) iniciaron ACOD (apixabán=18; edoxabán=5; rivaroxabán=4 y dabigatrán=2) en los primeros 3 meses tras la sustitución valvular aórtica, asociada a pontaje aortocoronario en un paciente y a cirugía mitral en 4 pacientes (reparación en 3, sustitución en uno). Quince pacientes ya tratados previamente con ACOD por FA preexistente mantuvieron este sin puente con AVK; el resto de ellos lo iniciaron tras un tiempo medio de 32,2±7,2 días con AVK, por mal control de INR (4), hemorragia mayor (1) o intolerancia a AVK (1), además de 8 pacientes con inicio directo. En estos pacientes con inicio de ACOD antes de los primeros 3 meses tras el reemplazo valvular se presentaron 2 hemorragias digestivas sin eventos embólicos y con normofunción protésica.
DiscusiónEl principal hallazgo de nuestro estudio es que el uso de ACOD en pacientes con FA y sustitución valvular por bioprótesis no muestra diferencias estadísticamente significativas en la tasa de eventos embólicos o hemorrágicos, en comparación con el tratamiento con AVK.
Estos datos, con las reservas de las limitaciones del estudio, están en consonancia con los datos publicados en subanálisis de los ensayos clínicos de ACOD que incluyeron estos pacientes, así como con estudios de menor tamaño en vida real.
Los ACOD constituyen una alternativa al AVK en la prevención de ictus y eventos tromboembólicos en pacientes con FA, hasta establecerse como opción preferencial, especialmente en pacientes que inicien ACO. Sin embargo, los grandes ensayos pivotales que sustentan su uso incluyen pacientes con FA no valvular, excluyendo aquellos con mayor riesgo embólico (fundamentalmente FA en el contexto de estenosis mitral, o pacientes portadores de prótesis mecánicas). Detrás de esta decisión se encontraba la posibilidad de que la fisiopatología de los fenómenos tromboembólicos en este subgrupo de pacientes resultase diferente de la del resto de entidades subyacentes en la FA8. Los decepcionantes resultados del ensayo Randomized Phase II Study to Evaluate the Safety and Pharmacokinetics of Oral Dabigatran Etexilate in Patients after Heart Valve Replacement (RE-ALIGN), suspendido de forma prematura porque el uso de dabigatrán frente a AVK en pacientes con prótesis mecánicas se asoció a una tasa mayor de eventos embólicos y hemorrágicos, reforzó esta posición9. La diferencia entre FA valvular y no valvular, no obstante, ha estado sometida a controversia por la gran variedad de los pacientes con enfermedad valvular cardiaca incluidos en los diferentes ensayos, lo que generaba confusión entre los profesionales que se enfrentan a diario a estos pacientes10 hasta que se eliminó en las guías de manejo clínico de FA de la Sociedad Europea de Cardiología de 201611. En todo caso, los datos derivados de estudios post-hoc de los ensayos pivotales de ACOD, recogidos en 3 metaanálisis, mostraban cómo los ACOD podrían considerarse agentes de primera línea también en pacientes con enfermedad valvular, excluidas siempre la estenosis mitral y las válvulas mecánicas12–14. Concretando aún más, los datos extraídos de Apixaban for Reduction in Stroke and Other Thromboembolic Events in Atrial Fibrillation (ARISTOTLE) y Effective Anticoagulation with Factor Xa Next Generation in AF-Thrombolysis in Myocardial Infarction 48 (ENGAGE AF-TIMI 48), los únicos 2 ensayos que incluyeron pacientes portadores de prótesis biológicas, apuntan a la ausencia de diferencias en la tasa de eventos clínicos entre apixabán y edoxabán frente a AVK en esta población. En ARISTOTLE se recogen datos de 104 pacientes con bioprótesis (aórtica en 73 casos, mitral en 26, y ambas en 5) y FA, sin diferencias significativas en ninguno de los parámetros evaluados15. En ENGAGE AF-TIMI 48 se incluyó a 191 pacientes con bioprótesis (aórtica en 60 casos y mitral en 131), además de 123 pacientes con reparación valvular. No se encontraron diferencias entre los tratados con dosis alta de edoxabán frente a AVK, y sí tasas menores de hemorragia mayor en aquellos tratados con la dosis menor16. En ambos casos destaca una baja incidencia de eventos clínicos, con amplios intervalos de confianza14.
Resultados similares se recogieron en varios trabajos de vida real, no aleatorizados, incluyendo uno en nuestro país17–19. Si bien el escaso tamaño muestral y los tiempos de seguimiento relativamente cortos limitan la solidez de las conclusiones que se pueden extraer de ellos, algunos aspectos merecen reflexión. Así, la tasa de eventos isquémicos resulta relativamente baja en los que incluyen un mayor número de pacientes, como nuestro trabajo20. Si bien se suele señalar un riesgo mayor (aunque no significativo) de ictus y tromboembolismo respecto a pacientes con FA sin cirugía valvular, quizá los pacientes con FA y bioprótesis tengan un riesgo tromboembólico similar al de formas no valvulares de FA a igualdad de edad y otros factores de riesgo21, lo que apoyaría la necesidad de mayores tamaños muestrales para observar potenciales diferencias. Las tasas de hemorragias mayores presentan ciertas variaciones, que podrían explicarse en las diferentes características de las poblaciones estudiadas, fundamentalmente la edad y la toma concomitante de antiagregantes. Esta oscila entre el 6% del trabajo de Russo et al.20, con resultados muy similares a los descritos por nuestro grupo, y el 72% de Yadlapati et al.22, en el que la incidencia acumulada de sangrado mayor es del 7% (si bien no establece comparaciones con pacientes con AVK). Recientemente, Di Biase et al.23 reportan datos similares en cuanto a eficacia y seguridad en un trabajo multicéntrico prospectivo, extendiendo esta utilidad a un entorno con alto riesgo tromboembólico como la ablación de venas pulmonares (en pacientes con FA y bioprótesis). Una de las ventajas conocidas de los ACOD respecto a la AVK en los grandes ensayos pivotales, así como en los trabajos de vida real, es la menor tasa de ictus hemorrágicos. En el análisis de Malik et al.14, el tratamiento con ACOD fue superior en la reducción de hemorragia intracraneal en pacientes con enfermedad valvular, si bien en este grupo se incluyen una amplia heterogeneidad de entidades, y no exclusivamente portadores de bioprótesis. Esta diferencia no se ha reportado en ningún trabajo centrado exclusivamente en pacientes con bioprótesis. Sin embargo, creemos que resulta uno de los aspectos más destacables de nuestra serie, similar a lo descrito también por el grupo de Russo et al., aunque nuevamente con tan escaso número de eventos debemos ser cautos al establecer conclusiones definitivas (el trabajo de Yadlapati et al, sí describe 2 ictus hemorrágicos en pacientes con ACOD)20,22.
Estas evidencias han supuesto una modificación de las guías, que en su versión europea recogen los ACOD como alternativa a AVK a partir del tercer mes del implante de bioprótesis, con un grado de recomendación IIaC24,25. Este margen temporal se basa en el mayor riesgo tromboembólico de pacientes con bioprótesis en los primeros 3 meses tras el recambio, aún en ritmo sinusal26–28, aunque el beneficio de la anticoagulación con bioprótesis aórticas resulta controvertido29–31. El Dabigatran versus Warfarin After Bioprosthesis Valve Replacement for the Management of Atrial Fibrillation Postoperatively (DAWA) fue un estudio piloto aleatorizado que intentó demostrar la utilidad de ACOD (en este caso, dabigatrán) en este contexto, usando como variable principal la presencia de trombo intracavitario en ecocardiograma transesofágico a 90 días32. Los resultados no mostraron diferencias entre AVK y ACOD, si bien el pequeño tamaño muestral y las limitaciones propias de un estudio meramente piloto impiden extraer conclusiones sólidas. Recientemente, los resultados del ensayo randomizado Explore the Efficacy and Safety of edoxabaN in Patients After Heart Valve Repair or Bioprosthetic vaLve Replacement (ENAVLE) apuntan a una no inferioridad del edoxabán en este rango temporal en pacientes sometidos a recambio biológico, sin indicación de profilaxis embólica por FA33. A la espera de nuevos estudios multicéntricos prospectivos que exploren esta posibilidad, nuestros datos en 29 pacientes que iniciaron ACOD antes de esos 3 meses, junto a 20 pacientes descritos por Yadlapati et al. parecen corroborar este punto.
Finalmente, merece la pena la discusión sobre 2 aspectos de la terapia anticoagulante que limitan sus potenciales beneficios. De un lado, la prevalencia de infradosificación de ACOD ya descrita en otros entornos34. En nuestra población probablemente viene condicionada por la percepción de muy alto riesgo en estos pacientes, muchos de ellos añosos y con alta prevalencia de enfermedad renal y otras comorbilidades que confieren un variable grado de fragilidad que, no obstante, no es criterio establecido para ajuste de dosis, que debe realizarse de forma rigurosa. Datos similares se han descrito recientemente en pacientes con FA no valvular sometidos a implante transcatéter de prótesis valvular aórtica35. Del mismo modo, destaca la dificultad de mantener un INR en rango terapéutico estable en una alta proporción de sujetos. Diversos estudios realizados en España muestran que, independientemente de dónde sean atendidos los pacientes, en el 40-55% de los casos existe un control pobre del INR36. En nuestra serie, únicamente el 30% presenta TTR>70%, dintel que se ha establecido como óptimo para disminuir eventos adversos y reducir el riesgo de ictus37.
LimitacionesEste estudio debe interpretarse con las limitaciones que supone que sea retrospectivo y no aleatorizado. Como todos los registros observacionales, está sujeto a factores de confusión más o menos evidentes. En este sentido, se podría argumentar que en España el marco legal de la financiación pública condiciona el uso de ACOD, lo que podría dificultar la comparación entre grupos de pacientes. Este hecho podría diluirse en nuestra serie tras establecerse un plan regional de salud en 2014 que incluye un ambicioso protocolo de manejo de la FA dirigido a reducir la incidencia de ictus en la región que incide en la prescripción de ACOD, incluso como fármacos de primera elección. El tamaño muestral es la segunda limitación. Aun incluyendo un número de pacientes mayor que registros similares, especialmente en el ámbito español, está infrapotenciado y debemos considerarlo meramente exploratorio. No obstante, ante la ausencia de ensayos clínicos específicos para esta población, la información procedente de estudios observacionales podría resultar relevante en la práctica clínica diaria. No se ha podido obtener información completa sobre el tiempo en rango terapéutico de los pacientes tratados con AVK. Sin embargo, el grado de control que se describe es similar al reportado en otros estudios en nuestro país.
ConclusionesEn nuestro medio, la utilización de ACOD como prevención de fenómenos embólicos en pacientes con bioprótesis y FA resulta una alternativa segura y eficaz frente a los AVK. Equilibrar la balanza entre riesgos y beneficios inherentes al inicio de ACO requiere una cuidadosa consideración de las comorbilidades; en este contexto, los ACOD aparecen como alternativas válidas al AVK.
La prevalencia de FA en pacientes sometidos a sustitución valvular es alta. Los ACOD han mostrado un mejor perfil de seguridad y eficacia que los AVK en el contexto de la FA no valvular, pero existen pocos estudios que analicen su papel en pacientes con recambio valvular, más allá de análisis post-hoc de los ensayos pivotales y series cortas en vida real.
¿Qué novedades aporta?El presente trabajo muestra que el uso de ACOD en comparación con el de AVK se asoció a incidencias muy similares de eventos trombóticos-isquémicos, sin diferencias significativas en la tasa de hemorragias mayores. No se presentaron eventos relevantes en los pacientes que iniciaron ACOD en los primeros 3 meses después de la cirugía.
No existen fuentes de financiación a declarar.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.