Diversos estudios de prevención primaria y secundaria han documentado que un mayor grado de reducción en los niveles de colesterol unido a proteínas de baja densidad (cLDL) se asocia a una mayor disminución en las tasas de eventos cardiovasculares. Los inhibidores de la PCSK9 logran disminuciones importantes, rápidas y mantenidas en los niveles de cLDL. Las nuevas guías de práctica clínica sobre dislipemias establecen unos nuevos niveles objetivo de cLDL muy reducidos en los pacientes que presentan un riesgo cardiovascular muy elevado. Estos objetivos son difícilmente alcanzables con un tratamiento basado únicamente en estatinas, incluso en combinación con ezetimiba. La adición de inhibidores de la PCSK9 puede tener un papel determinante para alcanzar estas recomendaciones. Sin embargo, es importante identificar los subgrupos de pacientes que más se pueden beneficiar de esta marcada reducción en los niveles lipídicos. En el presente documento se describen los perfiles de pacientes en los que la máxima disminución en los niveles de cLDL debe constituir un objetivo prioritario, y se plantean las estrategias para facilitar el uso juicioso de estos nuevos fármacos.
Different primary and secondary prevention studies have documented that a greater degree of reduction in low-density lipoprotein cholesterol (LDL-C) levels is associated with a greater decrease in cardiovascular event rates. PCSK9 inhibitors achieve important, rapid and sustained decreases in LDL-C. New clinical practice guidelines for the management of dyslipidemia establish reduced target levels of LDL-C. These goals are hardly achievable with a statin-only treatment, even in combination with ezetimibe. The addition of PCSK9 inhibitors can play a determining role in achieving these recommendations. However, it is important to identify the patient subgroups that can most benefit from this marked reduction in LDL-C levels. This document describes the profiles of patients with cardiovascular disease in which the maximum decrease in LDL-C levels should be a priority objective, considering strategies to achieve these levels and to facilitate the judicious use of these new drugs.
La enfermedad cardiovascular (CV) aterosclerótica continúa siendo una de las principales causas de mortalidad y morbilidad en los países occidentales. Es la responsable del 45% de la mortalidad global en Europa1, con un 35% de muertes prematuras en la población de menores de 75años de edad2. El colesterol unido a lipoproteínas de baja densidad (cLDL) elevado es uno de los principales factores de riesgo CV. Existe una amplia evidencia acerca de que los pacientes en quienes se disminuyen las concentraciones de cLDL a los niveles recomendados por las guías de práctica clínica reducen su riesgo de mortalidad y de presentar complicaciones CV3. La magnitud de dicho beneficio es tiempo y riesgo dependiente. En concreto, en España se ha descrito una reducción de la mortalidad coronaria en relación a una mayor utilización de estatinas4.
Sin embargo, a pesar de la existencia de fármacos hipolipemiantes con eficacia y seguridad probadas, en muchos pacientes con un riesgo CV elevado la reducción del cLDL es subóptima5. En un reciente estudio europeo se documentó que solo el 67% de los pacientes con alto riesgo de enfermedad CV recibían estatinas y que se conseguía el objetivo de un cLDL <100mg/dl únicamente en el 55% de los casos6. En España, según datos del Registro de Pacientes de Alto Riesgo Cardiovascular (REPAR), el tratamiento con dosis altas de estatinas se asociaba a un mayor control del cLDL, aunque solo se conseguían niveles dentro de los valores recomendados en el 26% de pacientes con una enfermedad coronaria ya documentada7. Las causas que pueden explicar la dificultad para conseguir un adecuado control de los niveles de cLDL son diversas y su abordaje debe ser multifactorial (tabla 1). Además, en algunos subgrupos de pacientes puede ser más difícil alcanzar los objetivos terapéuticos. Los pacientes con hipercolesterolemia familiar, por ejemplo, parten de concentraciones de cLDL basal extraordinariamente elevadas, lo que puede impedir que alcancen las cifras de colesterol recomendadas a pesar de un tratamiento hipolipemiante óptimo8. Por otra parte, los pacientes con un riesgo CV muy elevado precisan reducciones del cLDL más grandes que frecuentemente no se pueden conseguir debido a la importante variabilidad en la respuesta hipolipemiante a las estatinas9 e incluso con su combinación con ezetimiba. Los pacientes con intolerancia total o parcial a las estatinas representan otro subgrupo de difícil tratamiento.
Principales causas por las que no se alcanzan los valores recomendados en el control del nivel de cLDL y estrategias para facilitar la identificación y la detección precoz de los pacientes de riesgo cardiovascular muy elevado
| Causas por las que no se alcanzan los valores recomendados en el nivel de cLDL: |
| - Prioridad en los objetivos y dedicación asistencial de los profesionales hacia el tratamiento de la enfermedad coronaria aguda |
| - Conocimiento limitado de las guías de práctica clínica y ausencia de protocolos específicos en los diferentes niveles asistenciales |
| - Sobreestimación, por parte de los profesionales, del porcentaje de pacientes que se considera que están con niveles controlados |
| - Utilización de dosis de hipolipemiantes menores a las recomendadas |
| - Deficiente adherencia a la medicación por parte de los pacientes |
| - Sobrecarga de trabajo asistencial para realizar valoraciones con precisión en los pacientes. Limitaciones y barreras establecidas por el sistema (IPT, comunidades autónomas, hospitales) |
| - Temor de los profesionales a los efectos secundarios de los fármacos |
| Estrategias para facilitar la identificación y la detección precoz de los pacientes de riesgo cardiovascular muy elevado: |
| - Unificación de criterios y protocolos en los distintos dispositivos asistenciales. Planificar una continuidad asistencial después del alta |
| - Sensibilizar a los profesionales de la importancia de la identificación de este perfil de pacientes. Realizar una formación completa y específica |
| - Remarcar la evidencia existente del impacto pronóstico beneficioso de un tratamiento hipolipemiante adecuado |
| - Acceso fácil, rápido y con tiempo suficiente al historial completo y detallado de los pacientes |
| - Evaluación completa en el momento del alta hospitalaria. Considerar los antecedentes, factores de riesgo cardiovascular, historia cardiológica previa, respuesta terapéutica a los tratamientos hipolipemiantes, extensión de la enfermedad coronaria, afectación de otros territorios, riesgo cardiovascular calculado, etc. |
| - Remitir a los pacientes de riesgo cardiovascular muy elevado a un programa de rehabilitación cardiaca o, en su defecto, a una consulta monográfica especializada |
| - Identificación de los pacientes de muy alto riesgo que pueden seguir circuitos distintos a los estandarizados en los programas de prevención secundaria |
| - Establecer una estrecha relación asistencial y de intercambio de conocimiento con los dispositivos de asistencia primaria, realizando estrategias conjuntas para la identificación de este subgrupo de pacientes |
cLDL: colesterol unido a lipoproteínas de baja densidad; IPT: informe de posicionamiento terapéutico.
Es importante remarcar la evidencia obtenida en estudios de prevención primaria y secundaria acerca de que un mayor grado de reducción en los niveles de cLDL se asocia a una mayor disminución en las tasas de eventos CV10. Por cada mmol/l (aproximadamente 39mg/dl) de reducción en las cifras de cLDL, el riesgo relativo de eventos CV disminuye un 23%10. En el año 2015, el estudio IMPROVE-IT demostró que una disminución del cLDL a niveles inferiores a los recomendados en ese momento (se alcanzó un valor medio de 54mg/dl en el grupo de tratamiento simvastatina-ezetimiba) seguía proporcionando un beneficio adicional en la reducción de eventos CV a largo plazo11. Paralelamente se publicaron los primeros datos con los inhibidores de la proproteína convertasa subtilisina/kexina tipo9 (iPCSK9), que, añadidos a las estatinas, conseguían una importante reducción, rápida y mantenida en los niveles de cLDL. Los recientes estudios con estos fármacos, ya en poblaciones muy numerosas de pacientes con enfermedad CV estable12, o después de un síndrome coronario agudo13, han confirmado que esta importante reducción en los niveles de cLDL se asocia a una disminución aún mayor en las tasas de eventos CV. Esta evidencia ha sido trasladada a las guías del tratamiento de las dislipemias más recientes, que recomiendan como objetivo terapéutico alcanzar niveles de cLDL muy reducidos. Los iPCSK9 son fármacos que pueden facilitar la obtención de estos niveles. Actualmente, y considerando los cambios que se están produciendo en el abordaje de los pacientes con dislipemia y enfermedad CV, este documento, generado por expertos que pertenecen a diferentes sociedades y organismos científicos (tabla 2), intenta clarificar los perfiles de pacientes que más se pueden beneficiar de estas recomendaciones y de estos nuevos tratamientos.
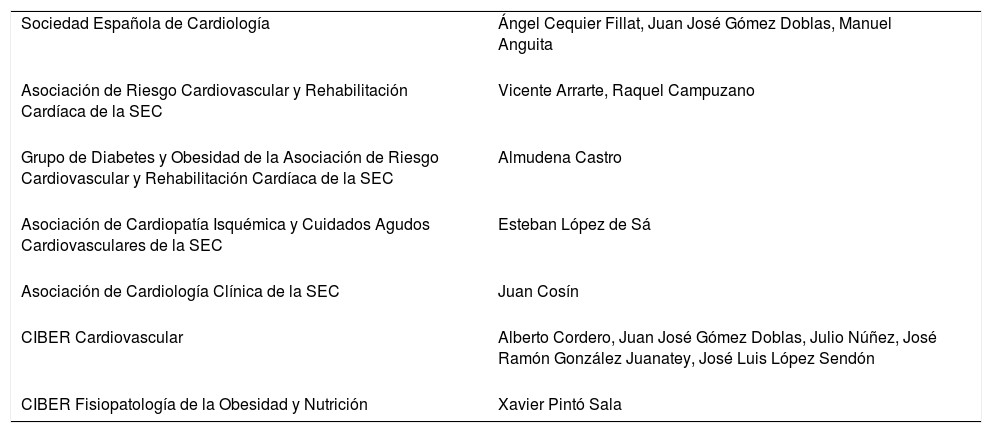
Sociedades, asociaciones y organismos científicos y representantes que han participado en el documento de consenso
| Sociedad Española de Cardiología | Ángel Cequier Fillat, Juan José Gómez Doblas, Manuel Anguita |
| Asociación de Riesgo Cardiovascular y Rehabilitación Cardíaca de la SEC | Vicente Arrarte, Raquel Campuzano |
| Grupo de Diabetes y Obesidad de la Asociación de Riesgo Cardiovascular y Rehabilitación Cardíaca de la SEC | Almudena Castro |
| Asociación de Cardiopatía Isquémica y Cuidados Agudos Cardiovasculares de la SEC | Esteban López de Sá |
| Asociación de Cardiología Clínica de la SEC | Juan Cosín |
| CIBER Cardiovascular | Alberto Cordero, Juan José Gómez Doblas, Julio Núñez, José Ramón González Juanatey, José Luis López Sendón |
| CIBER Fisiopatología de la Obesidad y Nutrición | Xavier Pintó Sala |
La proteína enzimática PCSK9 desempeña un importante papel en la regulación del metabolismo de los lípidos. El cLDL circulante tiene un potente efecto aterogénico, y el organismo dispone de un sistema de degradación de lipoproteínas de baja densidad (LDL) en el hígado y, simultáneamente, de un sistema, en cierto modo, ahorrador de LDL. En el hepatocito se producen receptores específicos del cLDL que son liberados a la superficie celular. Estos receptores capturan el cLDL circulante y lo internalizan en el hepatocito mediante un proceso de endocitosis; este se destruye en los lisosomas, liberando el receptor de LDL, que se recicla y vuelve a desplazarse de nuevo a la superficie del hepatocito, donde puede capturar otra molécula de LDL. Este proceso de reciclado puede repetirse hasta 100 veces14. En el interior del hepatocito se produce otra proteína, la PCSK9, que también se secreta al exterior celular, donde se une a los receptores del cLDL. Este complejo formado por el receptor de LDL y la proteína PCSK9 impide el reciclado del receptor de LDL a la superficie del hepatocito. En cierto modo, la proteína PCSK9 es un mediador de la degradación de los receptores del cLDL, con el fin de ahorrar LDL14.
Cuando la síntesis de PCSK9 está aumentada, como en el caso de la hipercolesterolemia familiar, se reduce el número de receptores de LDL en la membrana del hepatocito, por lo que aumenta la concentración plasmática de LDL que acelera la aterosclerosis14,15. Cuando la expresión de la proteína PCSK9 está disminuida, como sucede en personas con mutaciones en los genes reguladores de la PCSK9 (142X y 679X), los receptores de LDL no se destruyen, sino que se reciclan después de transportar una molécula de LDL y vuelven a la superficie del hepatocito para capturar otra molécula de LDL. En esta situación disminuye la concentración plasmática de cLDL y se retrasa la aterosclerosis15. Estas observaciones convierten a la proteína PCSK9 en un objetivo clave en el tratamiento de las dislipemias con concentraciones elevadas de cLDL. De los anticuerpos monoclonales generados contra la proteína PCSK9, dos de ellos (evolocumab y alirocumab) son 100% humanos, con un potencial de inmunogenicidad muy bajo, y han sido estudiados extensamente, tanto desde el punto de vista farmacodinámico como clínico. Recientemente inclisiran, un ARN interferente, ha demostrado reducciones potentes y duraderas de cLDL con administraciones dosificadas cada 6meses, con un excelente perfil de seguridad y tolerancia16.
Impacto clínico de los iPCSK9Diferentes ensayos clínicos han demostrado que los iPCSK9 producen disminuciones de los niveles de cLDL dependientes de la dosis, con reducciones de alrededor del 60%, que ya empiezan a ser perceptibles a las 48h de iniciar el tratamiento. Asimismo disminuyen las concentraciones de triglicéridos hasta un 20% y de lipoproteína(a) [Lp(a)] hasta un 25-30%, con una elevación marginal del colesterol unido a proteínas de alta densidad17. Las reducciones en los diferentes niveles lipídicos se suman a las que se llegan a alcanzar con estatinas u otros fármacos hipolipemiantes, y asociados al tratamiento hipolipemiante convencional han demostrado ser muy eficaces para conseguir reducciones importantes en el cLDL tanto en la hipercolesterolemia familiar heterocigota18-20 como en la homocigota21.
En relación con el posible papel de los iPCSK9 en pacientes con enfermedad CV, dos estudios recientes han definido su potencial beneficio en muestras muy numerosas de pacientes. En el estudio FOURIER se comparó el evolocumab con placebo en una población de 27.564 pacientes con enfermedad CV estable con niveles de cLDL ≥70mg/dl a pesar de estar recibiendo dosis máximas de estatinas12. Como objetivo primario se evaluó la incidencia de muerte CV, infarto de miocardio, accidente cerebrovascular y hospitalización por angina o revascularización coronaria. A las 48semanas de tratamiento el porcentaje de reducción del cLDL con evolocumab en comparación con placebo fue del 59% (mediana inicial de 92mg/dl, que pasó a 30mg/dl durante el seguimiento). Se observó una reducción significativa del riesgo de la variable principal del 15% (hazard ratio [HR]=0,85; intervalo de confianza del 95% [IC95%], 0,79-0,92; p<0,001), que en valores absolutos fue del 2%. Las curvas ya empezaban a divergir a los 6meses de haberse iniciado el estudio. Una serie de análisis secundarios preespecificados en la población incluida en dicho estudio han demostrado una mayor eficacia del evolocumab en la reducción absoluta del riesgo en pacientes diabéticos22, en pacientes con historia de infarto de miocardio reciente (en los 2años previos), con antecedentes de múltiples infartos (≥2) o con una enfermedad coronaria multivaso residual23,24, en pacientes con enfermedad arterial periférica25,26 y en pacientes con un riesgo inflamatorio basal aumentado categorizado por una concentración basal de proteínaC reactiva ultrasensible elevada27,28. Estos escenarios confirman que el beneficio CV de la reducción del cLDL es riesgo y tiempo dependiente.
En el estudio ODYSSEY OUTCOMES se incluyeron 18.924 pacientes después de un síndrome coronario agudo, con niveles de cLDL ≥70mg/dl a pesar de recibir dosis máximas de estatinas, que se aleatorizaron a tratamiento con alirocumab o a placebo13. La variable principal estaba compuesta de muerte por enfermedad coronaria, infarto de miocardio no mortal, accidente cerebrovascular isquémico o angina inestable que requería hospitalización. Tras una mediana de seguimiento de 2,8años el 9,5% de los pacientes tratados con alirocumab y el 11,1% de los tratados con placebo presentaron algún evento (HR=0,85; IC95%, 0,78-0,93; p<0,001). En este estudio las curvas iniciaron su divergencia a los 12meses de seguimiento. Los resultados de diferentes análisis secundarios preespecificados mostraron disminuciones significativas del riesgo de eventos CV en los pacientes con un cLDL basal ≥100mg/dl13, diabéticos29, pacientes con enfermedad polivascular aterotrombótica30, con cirugía coronaria de revascularización previa31 y con niveles muy elevados de Lp(a)32. Aunque considerado como un dato exploratorio, se documentó una reducción del número total de muertes por diferentes causas con alirocumab y una disminución en la incidencia de eventos CV no fatales33. Un reciente metaanálisis en red que examinaba el efecto de distintas dosis de alirocumab para reducir los valores de cLDL no ha demostrado diferencias significativas entre ellas, pero en todos los casos las disminuciones del cLDL eran superiores a las obtenidas con ezetimiba34.
Tanto en el estudio ODYSSEY OUTCOMES35 como en el estudio FOURIER36 se ha documentado una estrecha relación entre la progresiva disminución de los niveles de cLDL <77mg/dl (2mmol/l) y una reducción adicional en las tasas de eventos CV mayores, sin un incremento en los efectos secundarios. Estas observaciones hacen extensibles a una importante población de pacientes los datos previos del beneficio de una mayor reducción en las concentraciones de cLDL ya observadas con estatinas y ezetimiba en un limitado número de pacientes. La evidencia generada con estos fármacos justifica que, en los pacientes con un riesgo CV muy elevado, se intente conseguir una reducción de las concentraciones de cLDL a niveles inferiores a los recomendados en las guías de tratamiento de las dislipemias previas37,38. Los datos obtenidos de estudios diseñados para detectar cambios en las funciones cognitivas39 y los 6años de seguimiento del estudio IMPROVE-IT11 no han objetivado que concentraciones bajas y prolongadas de cLDL se asocien a efectos secundarios. Sin embargo, son necesarios más estudios con seguimientos a mucho más largo plazo para excluir la aparición de complicaciones tardías asociadas al mantenimiento de concentraciones de cLDL muy bajas.
Guías de práctica clínica sobre el tratamiento de las dislipemias e iPCSK9En las guías de la Sociedad Europea de Cardiología (ESC) y la European Atherosclerosis Society (EAS) de 201637, considerando la evidencia existente hasta aquel momento, se establecieron una serie de niveles de cLDL objetivo que debían alcanzarse en cada uno de los grupos de riesgo CV, y que oscilan entre <115mg/dl (en los pacientes de bajo riesgo) y <de 70mg/dl (pacientes de muy alto riesgo). Solo estaban indicados los iPCSK9 (recomendación claseIIb, nivel de evidenciaC) en los casos de pacientes de muy alto riesgo y con niveles de cLDL persistentemente elevados a pesar de recibir dosis altas de estatinas combinadas con ezetimiba (o por intolerancia a las estatinas). En el mismo año, la Sociedad Española de Cardiología redactó un documento de posicionamiento para definir los grupos de pacientes con enfermedad coronaria en los que las indicaciones de los iPCSK9 podían estar justificadas40.
En 2018 se publicaron las guías de diferentes sociedades americanas sobre el abordaje y el tratamiento de las dislipemias38 donde se establecía una serie de algoritmos basados en la identificación de diferentes grupos de riesgo de enfermedad CV. Las estatinas debían seguir siendo la medicación de primera elección, adecuando su intensidad para alcanzar las reducciones de cLDL recomendadas. Si después de instituir un tratamiento con estatinas de máxima intensidad o a dosis máxima no se alcanzan los niveles deseados de cLDL (cLDL <70mg/dl en pacientes con enfermedad CV de riesgo muy elevado), se recomienda la administración de ezetimiba (claseIIa) y, en el caso de persistencia de niveles de cLDL elevados, la administración de un fármaco anti-PCSK9 (claseIIa).
Sin embargo, las nuevas guías de la ESC/EAS de 201941 han introducido cambios importantes respecto a la edición europea previa y a las actuales guías americanas. Extienden las recomendaciones sobre la prevención CV a todo el potencial del conocimiento existente y no solo estrictamente a los resultados de los estudios aleatorizados. El tratamiento hipolipemiante se fundamenta en tres conceptos: a)los estudios realizados para evaluar su impacto clínico indican que la reducción del riesgo relativo de los eventos CV es proporcional a la reducción absoluta de las concentraciones de cLDL; b)«cuanto más bajo, mejor»: una reducción de los niveles de cLDL mediante estatinas, ezetimiba o iPCSK9 es segura y efectiva incluso con concentraciones <55mg/dl, y c)la intensidad del tratamiento hipolipemiante para reducir el cLDL debe basarse en dos premisas: 1)el riesgo es independiente de su causa (prevención primaria o secundaria, diabetes mellitus [DM] o insuficiencia renal), y 2)el cLDL basal determinará qué magnitud de reducción en el riesgo se puede obtener. Los niveles de cLDL recomendados como objetivo tienen relación con el riesgo CV de los pacientes y el beneficio de su reducción es riesgo y tiempo dependiente.
En comparación con las guías de la ESC/ESA de 201637, los cambios más relevantes se han producido en los pacientes de muy alto riesgo CV: de un nivel objetivo de cLDL <70mg/dl (o una reducción >50% si el cLDL basal se situaba entre 70 y 135mg/dl) recomendado en 2016, el objetivo ha pasado en 2019 a un nivel de cLDL <55mg/dl y una reducción >50% del cLDL basal (claseIA). En los pacientes de alto riesgo el nivel de cLDL a conseguir es <70mg/dl, con una reducción >50% del cLDL basal (claseIA). En los pacientes de riesgo moderado el nivel objetivo en las guías actuales es <100mg/dl (claseIIaA). El objetivo en los pacientes de riesgo bajo no se ha modificado (cLDL <115mg/dl; claseIIbA).
Las nuevas guías han ampliado aún más los criterios para considerar a un paciente como de riesgo CV muy elevado (tabla 3). La identificación de un paciente como de riesgo CV muy elevado obliga a valorar detalladamente su tratamiento hipolipemiante, ya que es recomendable situar las concentraciones de cLDL <55mg/dl y una reducción >50% del cLDL basal. Conseguir esta reducción solo será posible en muchos pacientes mediante la administración conjunta de estatinas, ezetimiba e iPCSK9. En la tabla 4 se describen también los niveles objetivo de cLDL, tanto en prevención primaria como en secundaria, en relación con el riesgo clínico de los pacientes recomendados por las dichas guías. Además, se definen con precisión las posibles combinaciones para alcanzar esta reducción y en qué momento se debe establecer la indicación de tratamiento con un iPCSK9. Un aspecto que cabe destacar son las recomendaciones para los pacientes que presentan un síndrome coronario agudo.
Criterios de riesgo cardiovascular muy elevado según la descripción de las guías de la Sociedad Europea de Cardiología y la European Atherosclerosis Society de 2019 para el abordaje de las dislipemias41
| a) Enfermedad cardiovascular documentada, clínicamente o mediante técnicas de imagen (invasivas o no invasivas). Incluye: síndrome coronario previo (infarto, angina inestable, angina estable), revascularización coronaria previa (percutánea o quirúrgica), accidente cerebrovascular o isquemia transitoria, vasculopatía periférica, enfermedad significativa en TAC coronaria o en la coronariografía (enfermedad multivaso) o en ecografía Doppler carotídea |
| b) Diabetes con afectación de un órgano diana, o con ≥3 factores de riesgo mayor o si la diabetes es de tipo1 con >20 años de evolución |
| c) Insuficiencia renal crónica grave (TFGe <30ml/min/1,73 m2) |
| d) Un SCORE >10% de muerte cardiovascular en 10años |
| e) Hipercolesterolemia familiar con enfermedad cardiovascular u otro factor de riesgo mayor |
TAC: tomografía axial computarizada; TFGe: tasa de filtrado glomerular renal estimada.
Niveles objetivo de cLDL en prevención primaria y secundaria (clase y niveles de evidencia) y combinaciones recomendadas, según las guías de la Sociedad Europea de Cardiología y la European Atherosclerosis Society de 20219 para el abordaje de las dislipemias41
| Niveles objetivo de cLDL | ||
| Prevención primaria | Individuos de riesgo CV muy elevado y sin hipercolesterolemia familiar: nivel de cLDL <55 mg/dl y una reducción del cLDL ≥50% de su valor basal | Clase I, evidencia C |
| Individuos de riesgo CV muy elevado con hipercolesterolemia familiar: nivel de cLDL <55 mg/dl y una reducción del cLDL ≥50% de su valor basal | Clase IIa, evidencia C | |
| Prevención secundaria | Pacientes de riesgo CV muy elevado: nivel de cLDL <55 mg/dl y una reducción del cLDL ≥50% de su valor basal | Clase I, evidencia A |
| Pacientes de riesgo CV muy elevado si presentan un segundo evento en los 2años siguientes estando en tratamiento con estatinas: nivel de cLDL <40 mg/dl | Clase IIb, evidencia B | |
| Recomendaciones de las combinaciones con un iPCSK9 | ||
| Prevención secundaria, pacientes de riesgo CV muy elevado | Si con dosis máximas toleradas de estatinas y ezetimiba no se alcanzan los niveles objetivo de cLDL | Clase I, evidencia A |
| Pacientes con hipercolesterolemia familiar de riesgo CV muy elevado | Si con dosis máximas toleradas de estatinas y ezetimiba no se alcanza los niveles objetivo de cLDL | Clase I, evidencia A |
| Pacientes tras un síndrome coronario agudo | Si en la reevaluación a las 4-6 semanas posteriores no se alcanzan los niveles objetivo de cLDL a pesar de tratamiento con dosis máximas toleradas de estatinas y ezetimiba | Clase I, evidencia B |
| Pacientes que se presentan con un síndrome coronario agudo | Si ya están bajo tratamiento con dosis máximas toleradas de estatinas y ezetimiba y los niveles de cLDL no están en el rango objetivo, debe considerarse añadir un iPCSK9 durante la hospitalización | Clase IIa, evidencia C |
cLDL: colesterol unido a lipoproteínas de baja densidad; CV: cardiovascular; iPCSK9: inhibidores de la PCSK9.
Actualmente los iPCSK9 alirocumab y evolocumab están aprobados en España como medicamentos de dispensación hospitalaria, con unas indicaciones basadas en los primeros estudios realizados en los que el impacto clínico de estos fármacos aún no había sido demostrado. Están aprobados para su financiación en las indicaciones de hipercolesterolemia familiar y enfermedad CV establecida (cardiopatía isquémica, enfermedad cerebrovascular isquémica y enfermedad arterial periférica) si los niveles de cLDL son >100mg/dl a pesar de recibir dosis máximas toleradas de estatinas o si existe intolerancia o contraindicación a estas.
Las nuevas guías de la ESC/EAS de 201941 establecen unos nuevos niveles objetivo de cLDL muy reducidos que precisarán de una intensificación del tratamiento hipolipemiante, principalmente en los pacientes de muy elevado riesgo CV isquémico. En dichas guías quedan muy bien definidos los perfiles de pacientes con un riesgo muy elevado de presentar eventos CV (tabla 3). Sin embargo, se han realizado subanálisis predefinidos dentro de los dos grandes estudios con evolocumab y alirocumab para identificar los subgrupos de pacientes en que los iPCSK9 pueden tener un papel fundamental en la reducción de las concentraciones de cLDL y en la disminución del riesgo CV (tabla 5).
| Reducción relativa de riesgo | Reducción absoluta de riesgo | |
|---|---|---|
| Estudio FOURIER-evolocumaba | ||
| Diabéticos21 | 18% | 2,7% |
| Insuficiencia renal crónica en estadio ≥342 | 21% | 2,5% |
| Antecedente de un IAM reciente (<2 años)22 | 24% | 2,9% |
| Antecedentes de ≥2 infartos previos22 | 21% | 2,6% |
| Enfermedad coronaria multivaso22 | 30% | 3,4% |
| Enfermedad vascular periférica24 | 27% | 3,5% |
| Pacientes con niveles de Lp(a) muy elevados43 | 23% | 2,5% |
| Estudio ODYSSEY OUTCOMES-alirocumabb | ||
| Pacientes con niveles de cLDL >100mg/dl28 | 14% | 3,4% |
| Diabéticos29 | 16% | 2,3% |
| Pacientes polivasculares (afectación de 3territorios)30 | 36% | 13% |
| Cirugía coronaria de revascularización previa31 | 23% | 6,4% |
| Pacientes con niveles muy elevados de Lp(a)32 | 11% | 2,1% |
cLDL: colesterol unido a lipoproteínas de baja densidad; CV: cardiovascular; IAM: infarto agudo de miocardio.
En el subanálisis de los pacientes con o sin DM21 del ensayo FOURIER la disminución del riesgo para la variable principal con los iPCSK9 fue del 17% en los pacientes con DM y del 13% en los pacientes sin DM, debido en gran medida a una reducción en el riesgo absoluto de revascularización coronaria. El estudio también demostró que el uso de evolocumab no estaba asociado a un aumento del riesgo de DM de nueva aparición, ni a un empeoramiento de la glucemia. Estos datos también han sido confirmados en un reciente metaanálisis44.
En otro subestudio del FOURIER que analizó los pacientes con antecedentes de infarto de miocardio en los últimos 2años, historia de ≥2infartos o con enfermedad coronaria residual multivaso, el tratamiento con evolocumab se asoció a una reducción relativa del riesgo para la variable secundaria (combinación de muerte CV, infarto de miocardio o ictus) del 24, del 21 y del 30%, respectivamente22. Los pacientes que presentaban ≥1 de estos criterios mostraban reducciones en los riesgos absolutos de entre el 2,6 y el 3,4%. Otros grupos de pacientes en los que evolocumab se ha asociado a reducciones relativas y absolutas importantes en la aparición de eventos CV son los que presentaban insuficiencia renal crónica avanzada42, enfermedad vascular periférica24 y niveles de Lp(a) muy elevados43. Respecto a la eficacia de estos fármacos en sujetos más jóvenes, el subanálisis del estudio FOURIER en pacientes estratificados por edad no mostró diferencias en la eficacia del evolocumab, tanto para la variable principal como para la variable secundaria12.
También diferentes subestudios del ODYSSEY OUTCOMES han mostrado que alirocumab se asocia a reducciones importantes en eventos isquémicos mayores en determinados pacientes (tabla 5). Los pacientes diabéticos29, los pacientes con afectación vascular en varios territorios30 o con antecedentes de cirugía coronaria previa31, y también los pacientes con niveles de Lp(a) muy elevados32, obtuvieron un beneficio muy relevante con alirocumab.
Estrategias recomendadasEn primer lugar es importante remarcar la necesidad de que los pacientes en riesgo deben recibir un tratamiento óptimo y tener un control global de sus factores de riesgo, tanto con medidas higiénico-dietéticas como farmacológicas (estatinas de alta intensidad y ezetimiba que reduzcan el cLDL, al menos, un 50%), y que la adherencia a los fármacos sea superior al 80%. La identificación de las principales causas por las que no se alcanzan frecuentemente los valores recomendados para el control del cLDL y su corrección es imprescindible en los pacientes con riesgo CV muy elevado, considerando las recomendaciones recientes de que una máxima disminución del cLDL debe constituir un objetivo terapéutico prioritario (tabla 1).
En segundo lugar, todos los pacientes que ingresan por enfermedad coronaria son de muy alto riesgo CV. Por ello, ya desde el ingreso debe plantearse la estrategia terapéutica para conseguir los objetivos de control según los niveles lipídicos de partida y el tratamiento hipolipemiante previo al evento. En todos los casos hay que confirmar o replantear la estrategia de tratamiento a las 4-6semanas según los objetivos de cLDL conseguidos. Es relativamente sencilla una identificación integrada de los factores de riesgo coronario, los antecedentes vasculares y la historia cardiológica, la evolución previa de los niveles de lípidos, la respuesta a los tratamientos hipolipemiantes recibidos y el grado de extensión de la enfermedad CV. En los pacientes que queden estratificados como de muy alto riesgo CV debe plantearse un seguimiento estructurado tras el alta en unidades de rehabilitación cardiaca para intentar alcanzar los niveles objetivo recomendados en el menor tiempo posible.
En tercer lugar, todos los pacientes de riesgo CV muy elevado deben alcanzar niveles de cLDL <55mg/dl, tal como se recomienda en las guías de la ESC/EAS más recientes41. Es un objetivo difícil y complejo, al menos en el momento actual. Los estudios aleatorizados comentados ponen de manifiesto que los pacientes que reúnen varias características o criterios de riesgo CV elevado son los que presentan una reducción más precoz e intensa en dicho riesgo al disminuir los niveles de cLDL con los iPCSK9. Por el contrario, en los pacientes que no tienen ninguno o un solo criterio de riesgo elevado de eventos CV, la disminución del cLDL con iPCSK9 no se asocia a un beneficio tan relevante, al menos durante los periodos de seguimiento descritos hasta ahora. En la tabla 6 se resumen los predictores clínicos y anatómicos clásicamente asociados a un riesgo isquémico muy elevado en la enfermedad coronaria. El riesgo CV total debe ser individualizado. En los pacientes con ≥2 de estos predictores es imprescindible disminuir los niveles lipídicos a los valores recomendados por las guías más actuales. En muchos de estos pacientes alcanzar dichos objetivos de cLDL solo será posible mediante la administración adicional de iPCSK9.
Predictores clínicos y anatómicos de muy alto riesgo isquémico en la enfermedad coronaria. Los pacientes con ≥2 predictores (riesgo extremo) son quienes pueden obtener un mayor beneficio pronóstico con una marcada reducción en sus concentraciones de cLDL
| Riesgo clínico |
| Edad avanzada |
| Diabetesa |
| Insuficiencia renal crónicaa |
| Hipercolesterolemia familiara |
| Síndrome coronario agudo (sobre todo en paciente joven) |
| Vasculopatía periféricaa |
| Infarto de miocardio previo (sobre todo reciente o si han sido varios episodios)a |
| Antecedente de cirugía de revascularización coronariaa |
| Historia de insuficiencia cardiaca |
| Episodios isquémicos recurrentes |
| Riesgo anatómico |
| Enfermedad coronaria extensa (multivaso)a |
| Enfermedad coronaria no revascularizable |
| Aterosclerosis que afecta a varios territorios vascularesa |
| Carga aterosclerótica muy importante (técnicas de imagen)a |
cLDL: colesterol unido a lipoproteínas de baja densidad.
Sin embargo, es importante remarcar que quedan aún preguntas relevantes por responder. Es necesario poder precisar la seguridad de estos fármacos a más largo plazo, la relación coste efectividad (tienen un coste relativamente elevado), su impacto sobre la mortalidad y si los pacientes de menor riesgo también pueden beneficiarse de una intensa reducción de los niveles de cLDL.
ConclusionesLa disponibilidad de los iPCSK9 con demostrada eficacia hipolipemiante abre nuevos horizontes para lograr una disminución del riesgo en la prevención secundaria de la enfermedad CV aterosclerótica. Los estudios recientes realizados con estos fármacos han confirmado que la importante reducción que producen en los niveles de cLDL se sigue asociando a una disminución adicional en las tasas de eventos CV. Esta evidencia ha sido trasladada a las guías de práctica clínica más recientes sobre el tratamiento de las dislipemias, que recomiendan niveles muy reducidos de los valores de cLDL como objetivo terapéutico. Los iPCSK9 son fármacos que pueden facilitar la obtención de estos niveles. Por ello, es importante definir las características y los perfiles de los pacientes que más se pueden beneficiar de estas recomendaciones para facilitar el uso juicioso de estos nuevos fármacos en la práctica clínica real desde la perspectiva de que su beneficio es tiempo y riesgo dependiente.
FinanciaciónEl presente trabajo no ha sido financiado por ningún patrocinador.
Conflicto de interesesÁ. Cequier ha firmado contratos de investigación con Abbott Vascular, Biosensors, Boston Scientific, Meddtronic, Biomenco, Cordis, Orbus y la Sociedad Española de Cardiología; ha recibido honorarios por conferencias y consultoría de Abbott Vascular, Biosensors, Medtronic, Ferrer Internacional, Terumo, Sanofi, Novonordisk, Amgen, Bayer, Boehringer Ingelheim, Daiichi Sankyo, al margen del trabajo presentado. V. Arrarte ha recibido honorarios por conferencias y consultoría de Amgen, Sanofi, Rovi, Almirall, Esteve y MSD, al margen del trabajo presentado. R. Campuzano ha recibido honorarios por conferencias y consultoría de Amgen y Sanofi, al margen del trabajo presentado. A. Cordero ha recibido honorarios por conferencias y consultoría de Bristol Myers Squibb, Amgen, Lilly, Boehringer Ingelheim, Bayer, Novartis y Ferrer, al margen del trabajo presentado. J. Núñez ha recibido honorarios por conferencias y consultoría de Amgen, al margen del trabajo presentado. X. Pintó ha recibido honorarios por conferencias y consultoría de Amgen, AstraZeneca, Esteve, Ferrer, Merck, Mylan y Sanofi, al margen del trabajo presentado. X. García-Moll ha recibido honorarios por conferencias y consultoría de Amgen, Sanofi y MSD, al margen del trabajo presentado. J.J. Gómez Doblas ha recibido honorarios por conferencias y consultoría de Amgen y Sanofi, al margen del trabajo presentado. E. López de Sá ha firmado contratos de investigación con Sanofi y AstraZeneca; ha recibido honorarios por conferencias y consultoría de MSD, Sanofi, Zoll y Becton Dickinson, al margen del trabajo presentado. Los demás autores no tienen conflicto de intereses.
Los autores agradecen el apoyo editorial de Ediciones Mayo, así como a la Dra. Marta Pulido por su colaboración en la redacción del manuscrito.