Actualización y novedades en cardiología. Visión del cardiólogo joven
Más datosLa cardiología a distancia, o telecardiología, evoluciona constantemente a medida que se desarrollan herramientas en los diferentes ámbitos de la especialidad. La consulta a distancia en tiempo real, la detección de fibrilación auricular con teléfono o reloj inteligente, las posibilidades potenciales en cardiopatía isquémica, el desarrollo de programas a distancia de rehabilitación cardiaca, la telemonitorización en insuficiencia cardiaca y la monitorización invasiva que incluyen los dispositivos implantables son los aspectos centrales incluidos en esta revisión.
Remote cardiology or telecardiology is constantly evolving parallel to the development of tools in different aspects of the specialty. Real-time remote consultation, detection of atrial fibrillation with a smartphone or smartwatch, potential possibilities in ischemic heart disease, development of remote cardiac rehabilitation programs, telemonitoring in heart failure, and invasive monitoring features included in implantable devices are the central aspects included in this review.
En los últimos años, la tecnología destinada a monitorizar los parámetros fisiológicos ha experimentado un gran desarrollo, y se ha hecho portátil, por lo que cada vez es más accesible a la población. Paralelamente, se han llevado a cabo investigaciones sobre telemonitorización con este tipo de dispositivos.
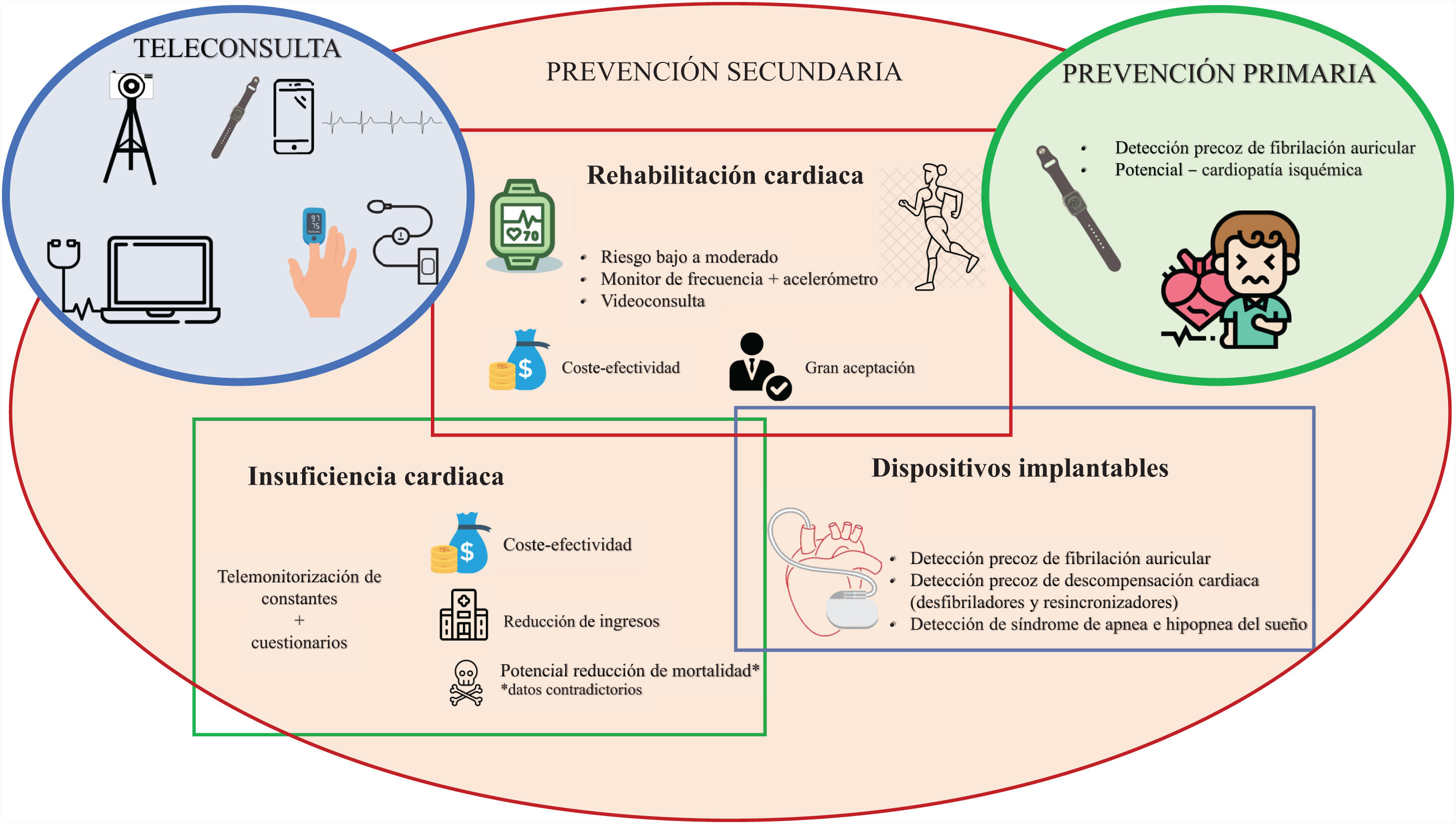
A continuación se lleva a cabo una revisión sobre la telecardiología en distintos escenarios clínicos, todos ellos recogidos en la tabla 1 y esquematizados en la figura 1.
Resumen de posibilidades. Telemedicina en cardiología
| Escenario | Soluciones tecnológicas | Función | Limitaciones |
|---|---|---|---|
| Prevención primaria | Fotopletismografía incluida en relojes o teléfonos inteligentes | Detección de ritmo acelerado o irregularValidado para la detección de fibrilación auricular | Alta tasa de falsos positivos, especialmente durante el ejercicio |
| Teleconsulta | Videollamada | Realización de la consulta | Compatible con la LOPD |
| Registro electrocardiográfico (relojes inteligentes) | Electrocardiograma no presencial | Poco práctico para conseguir derivaciones precordialesNo derivaciones aumentadas | |
| Fonendoscopio digital | Examen físico remoto | Hardware en poder del pacienteMínimo conocimiento médico del paciente | |
| Monitorización activa | Monitorización específica de condiciones cardiovasculares en tiempo real | Alta colaboración y responsabilidad por parte del paciente | |
| Monitorización pasiva | Dispositivos portátiles que miden frecuencia respiratoria, saturación de oxígeno, acelerómetros, temperatura de la piel, trastornos del sueño… | Alta cantidad de datos difíciles de procesarSin valor sin la colaboración activa del paciente | |
| Telerrehabilitación cardiaca | Variable según el centroHabitualmente monitor de frecuencia cardiaca, acelerómetro, videoconsulta y la opción de descargar datos | Seguimiento de los programas de entrenamiento impartidos en el hospital utilizando dispositivos de monitorización y comunicación a distancia | Pacientes de bajo y moderado riesgoAlto grado de motivación del pacienteTiene una parte presencialZonas grises: responsabilidad de la trasmisión de datos, revisión de datos transmitidos fuera de horario… |
| Dispositivos implantables | Holter implantable | Detección de bradiarritmias en estudio del síncopeDetección de fibrilación auricular en estudio de ictus criptogénico | InvasivoComplicaciones locales rarasDos años de vida útil aproximadamente |
| Dispositivos de estimulación | Detección de arritmias, principalmente fibrilación auricular silente o episodios de taquicardia auricular, con una aceptable precisión diagnóstica | Tratamiento controvertido en los episodios de taquicardia auricular | |
| Dispositivos en pacientes con IC (DAI, TRC-P, TRC-D) | Prevención de descompensaciones por IC (impedancia intratorácica, variabilidad de la frecuencia cardiaca, parámetros respiratorios, inferencia de primer y tercer ruido y actividad física) | No disponible en todos los dispositivosAlgoritmos diferentes según la casa comercialDiferente escala de validaciónMuy heterogéneo y casa-dependiente | |
| Detección de síndrome de apnea-hipopnea obstructiva del sueño | Sensores de ventilación minuto: detectan variaciones respiratorias mediante la medida de la impedancia intratorácica; son capaces de detectar episodios de apnea e hipopnea | Falta de validación de su tratamiento |
DAI: desfibrilador automático implantable; IC: insuficiencia cardiaca; LOPD: Ley Orgánica de Protección de Datos; TRC-D: terapia de resincronización cardiaca con función DAI; TRC-P: terapia de resincronización cardiaca sin función DAI.
La forma de entender y llevar a cabo las consultas de cardiología está evolucionando continuamente, más si cabe en los últimos dos años. La pandemia por el virus SARS-CoV-2, junto con el envejecimiento poblacional y el aumento de la demanda asistencial por la propia evolución de la especialidad y el paso de patologías agudas —previamente con supervivencias reducidas— a patologías crónicas, hacen que el modelo de consulta clásico coexista con la consulta telemática. Prueba de ello es la aparición en los últimos años de varios documentos de consenso o guías para el desarrollo de esta peculiar modalidad de consulta1-3.
Estos documentos de consenso fomentan y facilitan el uso y la implementación de la tecnología en la práctica clínica. Hoy en día disponemos de varias herramientas que hacen posible una consulta básica de telemedicina similar a la presencial:
VideollamadasLa videollamada es una herramienta ya incorporada a la mayoría de los seguros privados y que comienza a utilizarse de forma extendida dentro de la sanidad pública. El software utilizado debe garantizar el adecuado cumplimiento de la Ley Orgánica de Protección de Datos (Ley Orgánica 7/2021, de 26 de mayo)4.
Registros electrocardiográficosLa mayor parte de los llamados «relojes inteligentes» y varias herramientas complementarias a los últimos teléfonos móviles permiten realizar con mayor o menor exactitud un registro electrocardiográfico5. Por ahora, su única aplicación validada es la detección de ritmos irregulares6, y han llegado a modificar las guías clínicas para el diagnóstico de fibrilación auricular (FA)7. Se pueden exportar y enviar, lo que hace posible su lectura durante la teleconsulta.
Fonendoscopios digitalesLos fonendoscopios como EKO COR200 Core (EKO TM, Países Bajos), eKuore (eKuore Medical Devices, España) o AMD-370 (AMD Global Medicine, Estados Unidos) pueden ayudar a llevar a cabo un examen físico remoto, lo cual mejora la calidad de la teleconsulta. El problema que tienen que superar quienes quieran usarlo es que el paciente debe tener acceso al hardware y ser capaz de conocer los focos cardiacos, tras lo cual se pueden trasmitir los datos en directo.
Monitorización específica de condiciones cardiovascularesLos dispositivos de monitorización específica de condiciones cardiovasculares —como los de intelliH (IntelliH Inc., Estados Unidos), Biofourmis (Biofourmis Inc., Singapur), CareMindr (CareMindr Inc., Estados Unidos), Current Health (Current Health Inc., Estados Unidos), Hello Heart (Hello Heart Inc., Estados Unidos), Livongo (Teladoc Health Inc., Estados Unidos), Medical Innovations (Medical Innovations Inc., Estados Unidos), Myia (Myia Labs Inc., Estados Unidos) u Orma Health (Orma Health Inc., Estados Unidos)— necesitan la colaboración activa del paciente en la entrada y en la actualización de datos, y brindan datos procesables para informar en tiempo real.
Monitorización pasivaLa monitorización pasiva de funciones fisiológicas se lleva a cabo a través de sensores disponibles para medir la frecuencia respiratoria, la saturación de oxígeno, los acelerómetros, la temperatura de la piel y los trastornos del sueño. Todos estos sistemas se pueden encontrar en dispositivos portátiles o asociados a teléfonos o relojes inteligentes8.
Fibrilación auricularLa FA es la arritmia más común en adultos8. Su prevalencia aumenta paralelamente al envejecimiento poblacional9-11 y, además, se asocia con un incremento de la morbimortalidad, especialmente al asociarse con mayor riesgo de ictus isquémico y mayor mortalidad total. Su diagnóstico requiere un electrocardiograma (ECG), lo cual supone un reto, ya que muchos de los episodios son asintomáticos12-15. La detección temprana podría contribuir a la instauración precoz de un tratamiento que podría disminuir el ictus y otras consecuencias derivadas de la arritmia16-18.
Ante la gran distribución poblacional de relojes y teléfonos inteligentes, durante los últimos años se ha planteado la posibilidad de utilizar dicha tecnología para detectar FA. Recientemente se han llevado a cabo distintos estudios en este sentido6,19-21. Desde un punto de vista tecnológico, existen dos tipos de sistemas distintos integrados en los dispositivos inteligentes. Por un lado, la fotopletismografía, basada en la señal de presión generada por el impulso sanguíneo en las arterias. Esta señal genera unas ondas de pulso de las que se puede analizar tanto la regularidad del intervalo entre impulsos como la morfología generada por el propio impulso. Por otro lado, la electrocardiografía, que evalúa directamente la actividad eléctrica generada en el corazón a lo largo del ciclo cardiaco.
En los distintos estudios, los algoritmos de detección de la FA basados en las tecnologías previamente descritas tienen, en general, una sensibilidad y una especificidad superiores al 90%, así como un elevado valor predictivo positivo para la detección de FA y su distinción del ritmo cardiaco normal22-26. Existen estudios que además demuestran el impacto que tiene la detección de FA mediante este tipo de dispositivos, ya que permiten iniciar la anticoagulación de manera precoz27-29.
La principal limitación de este tipo de dispositivos es que, con una frecuencia variable entre los distintos estudios y dispositivos, se generan trazados artefactados de difícil interpretación. Por otro lado, generan gran cantidad de información que, para ser eficiente, requiere un análisis mediante inteligencia artificial.
Prevención secundaria y evidencia disponibleLa principal evidencia disponible en prevención secundaria se incluye en la tabla 2
Resumen de la evidencia disponible en prevención secundaria
| Escenario | Objetivos | Resultado | Referencias |
|---|---|---|---|
| Rehabilitación cardiaca | Aceptación | Tasas altas de aceptación (71-99% de participantes). Desinterés en el contacto por SMS o notificaciones móviles en 40% de los estudios. Preferencia por el cara a cara | 33-36 |
| Factibilidad | Los participantes evaluaron las herramientas (SMS, sensores, apps o webs) como fáciles de usar y entender, convenientes y cómodas. Solo el 20-30% informó de problemas de fiabilidad | ||
| Costes | Se reportó aproximadamente el 70% menos de coste en comparación con los programas hospitalarios. Probabilidad del 72-90% de coste-efectividad para intervención basada en SMS. Probabilidades moderadas-altas de que la telerrehabilitación sea más rentable que la rehabilitación hospitalaria | ||
| Reducción del colesterol | Colesterol total: −0,29 (−0,44 a −0,15) mmol/lColesterol HDL: −0,09 (−0,19 a 0,00) mmol/lColesterol LDL: −0,18 (−0,33 a −0,04) mmol/l | ||
| Actividad física | Aumento de 0,23 (0,11 a 0,36) minutos por semana | ||
| Adherencia a la medicación | Se utiliza para la medición la escala Morisky Medication Adherence. Aumento de hasta 1,10 (1,00 a 1,22) puntos | ||
| Tabaquismo | Riesgo relativo para continuar fumando del 0,87 (0,67-1,13) | ||
| HbA1c | Riesgo relativo de la reducción del 1,04 (0,40-2,70) | ||
| DEI | Detección de FA silente | Se revisan 7 estudios en los que se objetiva un riesgo relativo para eventos embólicos de 2,1 a 9,4 en pacientes en los que se detecta enfermedad silente | 37-47 |
| Detección de descompensación de la IC | Sistema HeartLogic: S: 98% y E: 90% para detección precoz de descompensaciones. Aumento de péptidos natriuréticos en fase de alerta. Tiempo de alerta a descompensación de 20±15 días. Tasa de alertas inexplicadas: 0,39 alertas/año-paciente. Tasa de alertas falsas positivas: 0,64 alertas/año-paciente. Carga de trabajo: 1hora semanal para 30 pacientes por centro | ||
| Diagnóstico de SAHS | Índice de dificultad respiratoria (impedancia torácica) >13,3 tiene S del 73% y E del 78% (sin FA, S: 77% y E: 100%; con FA, E: 57%) para el diagnóstico de SAHS | ||
| IC | Reducción de visitas por descompensación | Reducción de las visitas al servicio de urgencias del 56,5%. Reducción de ingresos hospitalarios del 46,9%. Sin diferencias de mortalidad | 52-60 |
| Monitorización ambulatoria de la PAPm | Reducción de ingresos del 30% | ||
| Teleasistencia sistematizada (programa AMULET) | Reducción del riesgo de primera hospitalización (HR=0,62; IC95%: 0,42-0,91). Reducción del riesgo del total de hospitalizaciones (HR=0,64; IC95%: 0,41-0,99). Sin diferencias en la mortalidad cardiovascular | ||
| Reducción de costes | Reducción del gasto medio de 3.546euros por paciente en el grupo de telemedicina |
E: especificidad; FA: fibrilación auricular; HbA1c: glucohemoglobina; HR: hazard ratio (riesgo relativo); IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; PAPm: presión de la arteria pulmonar media; S: sensibilidad; SAHS: síndrome de apnea-hipopnea del sueño.
La cardiopatía isquémica sigue siendo una de las principales causas de muerte y morbilidad en todo el mundo. La prevención secundaria es fundamental para mejorar el pronóstico en estos pacientes. En este sentido, la rehabilitación cardiaca es una herramienta fundamental. Sin embargo, la implementación de programas de rehabilitación cardiaca es variable en los distintos medios. Además, durante los últimos años, la pandemia de COVID-19 ha dificultado su normal funcionamiento en el medio hospitalario.
Para intentar paliar todos estos déficits de los programas tradicionales de rehabilitación cardiaca surge la telemonitorización en prevención secundaria, o telerrehabilitación cardiaca30, en la que el entrenamiento y el seguimiento de los pacientes se llevan a cabo en el ámbito extrahospitalario con ayuda de dispositivos telecomunicados31. Habitualmente, estos programas están dirigidos a pacientes de riesgo bajo y moderado. Los dispositivos que suelen facilitarse a los pacientes son un monitor de frecuencia cardiaca y un acelerómetro. El programa de rehabilitación se dirige mediante videoconsultas32.
Se ha comprobado en diversos estudios clínicos de distintos países que esta modalidad de rehabilitación cardiaca es coste-efectiva33,34. Asimismo, una revisión sistemática publicada en 2020 concluye que las intervenciones de telerrehabilitación cardiaca obtuvieron gran aceptación entre la mayoría de los participantes, que consideraban que, al ser cómodo, flexible y de fácil acceso, se trataba de un modelo alternativo al tradicional35,36.
En nuestro ámbito, se ha desarrollado el proyecto Aula RC37, una plataforma online que dispone de varios apartados; uno de ellos está dedicado al paciente y contiene información útil que fomenta su formación y autocuidado y ofrece ejercicios de entrenamiento.
Telemonitorización con dispositivos implantablesUn porcentaje importante de los pacientes que se benefician de consultas a distancia o telemonitorización son portadores de dispositivos cardiacos electrónicos implantables (DEI), tales como marcapasos, desfibriladores automáticos implantables o terapias de resincronización cardíaca. Estos DEI, aparte de sus funciones habituales, pueden desempeñar otras tareas de interés clínico38-41.
Detección de arritmiasPrincipalmente las de la FA silente, con una aceptable precisión diagnóstica (valor predictivo positivo del 95%). Son varios los estudios observacionales que han correlacionado la carga arrítmica con el riesgo embólico, aunque hasta la fecha no se ha podido demostrar una relación temporal entre ambos. Sin embargo, la indicación de anticoagulación en pacientes con episodios de FA detectados por dispositivos es controvertida, con dudas respecto a cuánto debe durar el episodio o cuál debe ser la carga arrítmica global. Aun así, la detección de FA silente por los DEI ofrece la posibilidad de una identificación e intervención temprana38,39.
Prevención de descompensaciones de insuficiencia cardiacaEn desfibriladores y en la terapia de resincronización cardiaca es de especial interés monitorizar los parámetros fisiológicos de interés en la IC, cuyo registro puede anticipar episodios de descompensaciones. Se han propuesto algoritmos que combinan varios parámetros clínicamente silentes de retención de fluidos, con una buena correlación con el estado clínico real, que permiten clasificar a los pacientes según el riesgo de descompensación en alto riesgo o bajo riesgo. El tiempo entre la detección de una alerta de alto riesgo y la aparición clínica de IC es de unos 34días42, lo cual da margen a una actuación terapéutica precoz para prevenir hospitalizaciones y descompensaciones graves.
Algunos de estos parámetros son el descenso en la impedancia intratorácica, el descenso de la variabilidad de la frecuencia cardiaca y de la frecuencia cardíaca nocturna, los parámetros respiratorios (frecuencia respiratoria, volumen y variación respiratorios), la inferencia del primer y tercer ruido cardiaco y la actividad del paciente38,39,43-45.
Diagnóstico de síndrome de apnea-hipopnea del sueñoLos DEI presentan sensores de ventilación minuto para adaptar la frecuencia cardiaca a la actividad del paciente. Estos sensores tienen la capacidad de detectar variaciones respiratorias mediante la medida de la impedancia intratorácica y son capaces de detectar episodios de apnea (ausencia de actividad respiratoria durante más de 10segundos) e hipopnea (reducción de la amplitud respiratoria con respecto a los ciclos previos durante 10segundos). Con estos datos se obtiene el índice de apneas-hipopneas por hora, que ha mostrado una aceptable correlación con la polisomnografía, patrón oro en el diagnóstico del síndrome de apnea-hipopnea del sueño (SAHS)40,46-48.
En resumen, los DEI ofrecen herramientas de suma utilidad en el seguimiento de los pacientes. Sin embargo, no debemos olvidar que no reemplazan el seguimiento rutinario, sino que son un complemento de este. Es de esperar que estas aplicaciones crezcan de forma exponencial en el futuro.
Telemonitorización en insuficiencia cardiacaEn pacientes con IC, la telemedicina permite que el paciente esté en contacto estrecho con el profesional de la salud e intercambie información útil para el tratamiento de su enfermedad sin que sea necesaria una visita presencial. La telemedicina permite la identificación precoz de descompensaciones y un tratamiento más temprano, que redunda en la reducción de ingresos. Por otro lado, la teleasistencia permite a los pacientes obtener un mejor conocimiento de su enfermedad, al participar activamente en la monitorización y el ajuste del tratamiento. Además, mediante este sistema, los tiempos de desplazamiento y de espera del paciente se reducen, lo que conlleva un aumento en su calidad de vida49-53.
Profundizando en la reducción de visitas ambulatorias e ingresos hospitalarios, un estudio reciente demostró una reducción de las visitas al servicio de urgencias por IC del 56,5%, así como una reducción del número de ingresos hospitalarios del 46,9%, sin aumento en la mortalidad54. Abraham et al.55 utilizaron un sistema inalámbrico de monitorización hemodinámica implantable para determinar la presión arterial pulmonar y señalaron una reducción significativa de la duración de las hospitalizaciones y la tasa de ingresos hospitalarios hasta en un 30% por IC. Krzesiński et al.56 mostraron como la implementación de la teleasistencia en el programa AMULET, en comparación con la atención estándar, redujo el riesgo de primera hospitalización por IC (hazard ratio [HR]=0,62; intervalo de confianza del 95% [IC95%]: 0,42-0,91; p=0,015), así como el riesgo del total de hospitalizaciones por IC (HR=0,64; IC95%: 0,41-0,99; p=0,044), sin diferencias en la mortalidad cardiovascular.
Este sistema lleva ya un tiempo implantado (por ejemplo, en el seguimiento de DEI); sin embargo, la reciente pandemia provocada por el virus SARS-CoV-2 ha evidenciado la necesidad y la utilidad de la telemedicina al demandar el cuidado de los pacientes evitando las visitas al hospital1-3,57. Existe una amplia gama de variables que se pueden emplear para la teleasistencia. La mayoría de ellas las registran manualmente los pacientes a través de un dispositivo; en cambio, otras se obtienen con dispositivos invasivos y se registran automáticamente49-53.
La telemedicina aporta numerosas ventajas al sistema sanitario en este ámbito. Estos beneficios no solo se expresan clínicamente, sino también económicamente. Así, en un estudio llevado a cabo en la unidad de IC del Hospital del Mar y del Instituto Hospital del Mar de Investigaciones Médicas, mostró diferencias significativas en cuanto al coste para el sistema de salud, con una reducción del gasto medio de 3.546euros por paciente en el grupo de telemedicina. El cálculo se determinó desde el día después de la salida del hospital e incluyó los gastos de hospitalización, de diagnóstico y de atención ambulatoria58,59.
Sin embargo, no se ha demostrado claramente la efectividad de la teleasistencia en cuanto a la reducción de la morbilidad y la mortalidad de los pacientes, ya que los resultados obtenidos son contradictorios60. Para tratar de aclarar este aspecto, son necesarios nuevos ensayos clínicos aleatorizados en los que se empleen sistemas de telemedicina que combinen variables invasivas y no invasivas con monitorización y tratamiento diarios, para esclarecer plenamente la utilidad de la teleasistencia en el campo de la IC. Actualmente hay estudios en marcha que tratan de demostrar que el tratamiento domiciliario de los pacientes con IC es factible, efectivo y seguro y, por lo tanto, libera recursos para otros grupos de pacientes61-64.
Otros potenciales escenarios: la cardiopatía isquémicaUn escenario poco explorado y que potencialmente podría beneficiarse de la inmediatez y la precisión de la telemedicina es la cardiopatía isquémica aguda, en concreto el síndrome coronario agudo con elevación de ST.
La posibilidad de hacer ECG con un dispositivo de bolsillo podría agilizar el diagnóstico de la cardiopatía isquémica en situaciones en las que no se dispone de un ECG convencional5. Hay estudios de muestras pequeñas para validar sistemas basados en teléfonos inteligentes como Kardia (AliveCor Labs, Estados Unidos)65 o relojes inteligentes66 en los que se incluyen pacientes con cardiopatía isquémica dentro del ámbito hospitalario. No obstante, para poder validar estas herramientas se necesitan estudios más amplios que caractericen las posibles limitaciones y que se desarrollen en el ámbito extrahospitalario con presencia de los llamados «servicios médicos de primer contacto/nivel» que deberían llevar a cabo el diagnóstico y activar, en su caso, el código infarto.
Uso actual de la telemedicina en cardiología: el proyecto SEConectadaDesde el grupo de trabajo de la Sociedad Española de Cardiología se ha lanzado la plataforma SEConectada67, que pone en valor la telemedicina en cardiología, y en la que se ofrecen herramientas e información para hacer un buen uso de ella en tres escenarios de la especialidad: la IC, la FA y el síndrome coronario crónico.
Esta herramienta, nacida de la necesidad de acercar la innovación a la consulta actual en el contexto epidemiológico de la pandemia de COVID-19, ofrece pautas diagnósticas, estrategias de seguimiento e infografía útil para mejorar la práctica clínica habitual.
Además, se incluyen otros aspectos relevantes en el seguimiento a distancia del paciente, como asesoramiento legal o consejos para una videoconsulta eficaz.
Posibles barreras en la implementación de la telemedicinaComo hemos visto, la telemedicina está más avanzada en ciertas áreas de la cardiología que en otras. No hay que olvidar que no todos los pacientes son iguales, y en determinados grupos, como podrían ser los pacientes más añosos, con más dificultades para acceder a este tipo de seguimiento, puede que aparezcan dificultades en su implementación. Además, hay pacientes con un perfil socioeconómico bajo, para quienes no será posible disponer del soporte técnico oportuno.
Otra de las cuestiones para tener en cuenta es la amplia oferta disponible de dispositivos con los que se podría realizar la telemedicina, por lo que podría ser complicado elegir el más oportuno para cada paciente, ya que no se dispone de recomendaciones claras.
A pesar de las grandes ventajas que parecen surgir de este nuevo modelo, aún quedan incógnitas por resolver68, como son la responsabilidad de una posible transmisión incorrecta de datos desde el dispositivo electrónico, responsabilidad del médico ante los datos transmitidos fuera del horario habitual, cómo organizar la telemedicina (programar las visitas virtuales), etc.
No hay que olvidar los aspectos legales relacionados con esta nueva relación médico-paciente, en los que el centro encargado (no el médico) debe asegurar que la tecnología que se vaya a utilizar cumple con las licencias correctas y contar con canales encriptados para cumplir con la ley de protección de datos (cobertura legal de las plataformas para contactar con los pacientes) y mantener la confidencialidad del paciente en todo momento. Sumándose a esto, la falta de formación actual de los médicos en este campo de la teleconsulta puede ser un impedimento para su implementación, aunque ahora, como hemos comentado previamente, se dispone de herramientas como la SEConectada para ayudarnos a mejorar.
ConclusionesLa cardiología es una de las especialidades médicas con más interés en la innovación y la adopción temprana de avances tecnológicos. La pandemia de COVID-19 ha acelerado su uso, con dispositivos y herramientas que permitan un seguimiento telemático de los pacientes y la detección precoz de alteraciones que posibiliten un diagnóstico y tratamiento más tempranos.
No obstante, todos estos avances plantean una serie de retos. Uno de ellos es que la industria biotecnológica adapte los dispositivos, sus plataformas y aplicaciones para permitir su integración en los sistemas clínicos informáticos. Otro reto es la elección del mejor dispositivo de telemonitorización en cada situación clínica, para cada paciente y para cada médico. Otra dificultad se plantea a la hora de gestionar y analizar el gran volumen de información generada por todos los dispositivos, que probablemente requerirá el desarrollo de inteligencia artificial con algoritmos para su cribado inicial.
El futuro de la cardiología y la atención cardiovascular integrarán, sin duda, los dispositivos portátiles, la monitorización remota, el aprendizaje automático, la inteligencia artificial y los algoritmos para estratificar el riesgo de los pacientes, y así poder ofrecerles una mejor asistencia.
FinanciaciónNo se ha recibido financiación para este artículo.
Contribución de los autoresTodos los autores contribuyeron igualmente en la redacción y la corrección crítica de este artículo. R. Carrillo Alemán, primer autor, realizó la corrección y el ensamblaje final. G. L. Alonso Salinas, último autor, coordinó el proyecto.
Conflicto de interesesNo hay conflictos de intereses.