El implante percutáneo de válvula aórtica (TAVI) se ha postulado como alternativa al reemplazo quirúrgico (SVA). Se compararon ambos utilizando el Conjunto Mínimo Básico de Datos del Sistema Nacional de Salud.
MétodosEstudio observacional retrospectivo. Se incluyó a pacientes dados de alta de hospitales del Sistema Nacional de Salud español a los que se realizó SVA o TAVI entre 2014 y 2015. Las variables resultado fueron mortalidad intrahospitalaria, estancia y tasa de complicaciones. Se ajustó la mortalidad por riesgo (regresión logística multinivel) y la estancia por gravedad, contrastando la mortalidad intrahospitalaria entre TAVI y SVA mediante emparejamiento por puntuaciones de propensión.
ResultadosSe identificaron 17.343 episodios TAVI o SVA, seleccionándose 1.725 TAVI y 8.616 SVA aisladas. Los pacientes TAVI tenían mayor edad media (81,1± 6,6 frente a 70,2±11,4 años; p<0,001), mayor proporción de mujeres (52,2 frente a 42,9%; p<0,001) y más comorbilidad (índice Charlson: 7,2±1,6 frente a 6,5±1,7; p<0,001). La mortalidad bruta intrahospitalaria fue 4,46% en TAVI y 4,53% en SVA. La TAVI mostró menor mortalidad intrahospitalaria ajustada por riesgo que la SVA (OR=0,58; IC95%, 0,44-0,7; p <0,001), se constató también mediante emparejamiento por puntuaciones de propensión (OR=0,49; IC95%, 0,36-0,66; χ2, p <0,001). La estancia media ajustada fue más elevada en SVA.
ConclusionesEn el periodo 2014-2015, para una población más compleja que los pacientes sometidos a SVA, la TAVI mostró mejores resultados en cuanto a mortalidad intrahospitalaria y estancia media, si bien presentó mayor incidencia en algunas complicaciones no fatales.
Transcatheter aortic valve implantation (TAVI) has been postulated as an alternative to surgical replacement (SAVR). The results of both procedures were compared using the Minimum Basic Data Set of the National Health System (NHS).
MethodsRetrospective observational study. Patients discharged from Spanish National Health System hospitals who underwent a SVA or TAVI procedure between 2014 and 2015. Outcome variables analysed: in-hospital mortality, length of stay and complication rate. In-hospital mortality was adjusted by risk (multilevel logistic regression) and length of stay by severity, also contrasting in-hospital mortality between TAVI and SVA using propensity score matching.
ResultsAmong 17 343 identified procedures of TAVI or SVA, we selected 1725 TAVI and 8616 isolated valvular SVA. TAVI patients had higher mean age (81.1±6.6 vs 70.2±11.4 years; P <.001), higher proportion of women (52.2% vs 42.9%; P <.001) and more comorbidities (Charlson index: 7.2±1.6 vs 6.5±1.7; P <.001). The raw in-hospital mortality was 4.46% in TAVI and 4.53% in SVA. TAVI showed lower risk-adjusted in-hospital mortality than SVA (OR, 0.58; 95%CI, 0.44-0.7; P <.001), also being found using propensity score matching (OR, 0.49; 95%CI, 0.36-0.66; χ2, P <.001). The adjusted mean stay was higher in SVA.
ConclusionsIn the 2014-5 period, for a population more complex than those undergoing SVA, TAVI showed less mortality and mean stay with higher rate of some non-fatal in-hospital events than SVA.
La estenosis aórtica es una enfermedad frecuente y progresiva que, en sus estadios avanzados, ocasiona sustanciales tasas de morbimortalidad1. El único tratamiento capaz de modificar la historia natural de esta enfermedad ha sido clásicamente la sustitución valvular aórtica quirúrgica (SVA) con circulación extracorpórea. En las últimas 2 décadas hemos asistido a una revolución en el tratamiento de estos enfermos tras el desarrollo del implante endovascular percutáneo de válvula aórtica (TAVI), procedimiento mucho menos invasivo que la mencionada intervención quirúrgica por esternotomía media.
Inicialmente, los implantes TAVI se limitaron a pacientes inoperables o de alto riesgo quirúrgico2. Posteriormente, tras confirmar unos excelentes resultados clínicos en ensayos clínicos, en estudios de vida real y junto a los importantes avances tecnológicos que han experimentado tanto las prótesis transcatéter como los dispositivos de introducción o liberación de las mismas, el TAVI se ha ido postulando como una técnica muy competitiva, sino superior, respecto al patrón de referencia constituido por la SVA. Estos resultados también se han observado posteriormente en pacientes de riesgo quirúrgico intermedio y bajo2,3, de forma que en muchos países occidentales se ha producido un cambio de paradigma tal que los procedimientos TAVI ya superan globalmente a los quirúrgicos3.
Puesto que nuestro país no ha sido ajeno a estos cambios en la atención a los enfermos con estenosis aórtica grave sintomática, el presente estudio tiene por objeto comparar los resultados de ambos procedimientos de implantación protésica utilizando los datos del mundo real registrados en el Conjunto Mínimo Básico de Datos (CMBD) del sistema nacional de salud (SNS), en un periodo de plena expansión de la técnica transcatéter.
MétodosPoblación y fuentes de datosSe realizó un estudio observacional retrospectivo de todos los pacientes dados de alta en los hospitales del SNS español a quienes se realizó un procedimiento de SVA o TAVI. La fuente de los datos utilizados fue el CMBD del SNS, que incluye información sobre las características demográficas de los pacientes ingresados, así como variables administrativas referidas al proceso de atención, y clínicas relacionadas con los diagnósticos y los procedimientos, codificados mediante la Clasificación Internacional de Enfermedades, Novena Revisión, Modificación Clínica (CIE-9-MC)4.
La población de estudio se obtuvo a partir de los episodios registrados en el CMBD entre el 1 de enero de 2014 (año en el que se registró por vez primera el código TAVI en el CMBD) y el 31 de diciembre de 2015, con códigos de procedimiento 35.25. y 35.22 para la SVA y 35.05 para la TAVI. La información disponible en los registros del CMBD de los años 2016 y 2017 no permite incluir casos en este estudio, al existir un notable subregistro de centros, episodios y procedimientos relacionado con el cambio de la base de datos y el sistema de clasificación de enfermedades y procedimientos.
Se excluyeron los episodios correspondientes a pacientes <18 años, aquellos registrados como «alta voluntaria», alta por «traslado a centro sociosanitario» o motivo de alta «desconocido», los que causaron 1 estancia o menos si el alta fue a domicilio y los clasificados dentro de la categoría diagnóstica mayor 14 de los grupos relacionados por el diagnóstico (embarazo, parto y puerperio). Aquellos traslados de hospital en los que se identificó el hospital de destino se consolidaron en un único episodio; se excluyeron las altas por traslado a otros hospitales cuando no fue posible identificar el hospital del destino al no disponer del resultado final, así como para evitar duplicidades
Para hacer más homogénea la comparación de resultados entre ambas técnicas, se excluyeron los episodios con diagnóstico principal o secundario de shock cardiogénico (785.51) o de endocarditis infecciosa (421.0, 421.1, 421.9, 424.99), al no poder discriminar si estaban, o no, presentes al ingreso y los episodios con diagnóstico principal de IAM (410.*1 o 410.*0). En episodios de SVA se excluyeron los episodios con otra cirugía cardiaca mayor concomitante: sustitución de otras válvulas (35.23 al 35.28), valvuloplastia (35.1*), revascularización aortocoronaria (36.10-36.19), operaciones sobre estructuras adyacentes a las válvulas cardiacas (35.3*) o cirugía aórtica (38.40; 38.45; o presencia de 441.* -aneurisma aórtico y disecante- como diagnóstico principal o secundario). En los episodios de TAVI se excluyeron los episodios con presencia concomitante de angioplastia coronaria (00.66, 36.06, 36.07). Cuando en un mismo episodio coincidía un procedimiento de TAVI y SVA se incluyó como TAVI; la SVA se consideró como una complicación.
Las variables de resultado analizadas fueron la mortalidad intrahospitalaria y la duración de la estancia y la aparición de complicaciones. Para el estudio de las complicaciones se utilizaron los códigos de diagnósticos que se muestran en la tabla 1del material adicional. No se incluyó entre las complicaciones la fibrilación auricular tras el procedimiento, al no poder discriminar si está presente al ingreso. La regurgitación aórtica tras el procedimiento está englobada en el epígrafe de «complicaciones por prótesis de válvula cardiaca».
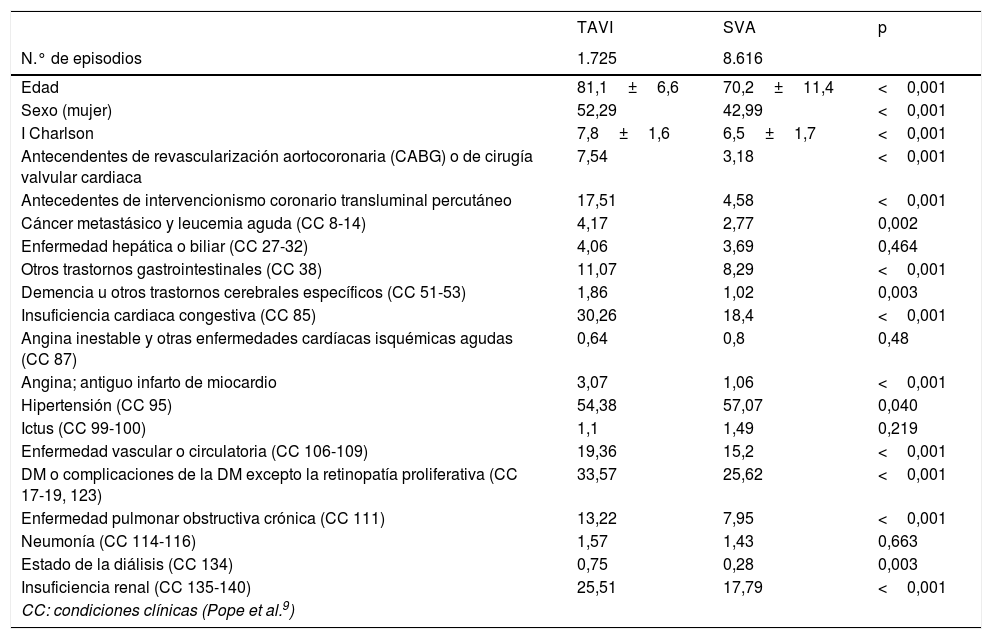
Características de los pacientes con TAVI o SVA
| TAVI | SVA | p | |
|---|---|---|---|
| N.° de episodios | 1.725 | 8.616 | |
| Edad | 81,1±6,6 | 70,2±11,4 | <0,001 |
| Sexo (mujer) | 52,29 | 42,99 | <0,001 |
| I Charlson | 7,8±1,6 | 6,5±1,7 | <0,001 |
| Antecendentes de revascularización aortocoronaria (CABG) o de cirugía valvular cardiaca | 7,54 | 3,18 | <0,001 |
| Antecedentes de intervencionismo coronario transluminal percutáneo | 17,51 | 4,58 | <0,001 |
| Cáncer metastásico y leucemia aguda (CC 8-14) | 4,17 | 2,77 | 0,002 |
| Enfermedad hepática o biliar (CC 27-32) | 4,06 | 3,69 | 0,464 |
| Otros trastornos gastrointestinales (CC 38) | 11,07 | 8,29 | <0,001 |
| Demencia u otros trastornos cerebrales específicos (CC 51-53) | 1,86 | 1,02 | 0,003 |
| Insuficiencia cardiaca congestiva (CC 85) | 30,26 | 18,4 | <0,001 |
| Angina inestable y otras enfermedades cardíacas isquémicas agudas (CC 87) | 0,64 | 0,8 | 0,48 |
| Angina; antiguo infarto de miocardio | 3,07 | 1,06 | <0,001 |
| Hipertensión (CC 95) | 54,38 | 57,07 | 0,040 |
| Ictus (CC 99-100) | 1,1 | 1,49 | 0,219 |
| Enfermedad vascular o circulatoria (CC 106-109) | 19,36 | 15,2 | <0,001 |
| DM o complicaciones de la DM excepto la retinopatía proliferativa (CC 17-19, 123) | 33,57 | 25,62 | <0,001 |
| Enfermedad pulmonar obstructiva crónica (CC 111) | 13,22 | 7,95 | <0,001 |
| Neumonía (CC 114-116) | 1,57 | 1,43 | 0,663 |
| Estado de la diálisis (CC 134) | 0,75 | 0,28 | 0,003 |
| Insuficiencia renal (CC 135-140) | 25,51 | 17,79 | <0,001 |
| CC: condiciones clínicas (Pope et al.9) |
CABG: cirugía de revascularización coronaria; CC: condiciones clínicas; DM: diabetes mellitus; SVA: sustitución valvular aórtica quirúrgica; TAVI: implante percutáneo de válvula aórtica.
Los datos expresan % o promedio ± desviación estándar.
Para el ajuste por riesgo de la mortalidad intrahospitalaria, algo necesario al existir características propias de los pacientes y de los centros donde son atendidos que influyen en los resultados asistenciales con independencia de la calidad de la atención dispensada5, se especificaron los modelos basados en la metodología de los Centres for Medicare and Medicaid Services (CMS).
Se consideró como variables independientes las incluidas en el modelo de mortalidad a los 30 días en la cirugía de revascularización coronaria6, incorporando algunas variables que, contempladas en la puntuación de la Society of Thoracic Surgeons)7 para el reemplazo valvular aórtico, se pueden identificar en el CMBD, adaptando el modelo de los CMS a la estructura de datos del CMBD, previa agrupación de los diagnósticos secundarios según las categorías de condiciones clínicas (CC) elaboradas por Pope et al.8, actualizadas anualmente por la Agency for Healthcare Research and Quality9.
Dado que la probabilidad de muerte intrahospitalaria de un paciente es una combinación de sus factores individuales de riesgo (casuística) y de la calidad de la atención dispensada (funcionamiento)10, se ajustaron modelos de regresión logística multinivel, que contemplan, además de variables clínicas y demográficas, un efecto aleatorio específico a nivel de hospital11,12. Para el modelo de ajuste se consideraron solo comorbilidades con significación estadística y odds ratio (OR)> 1,0. Las variables que finalmente entraron en el modelo de ajuste de la mortalidad intrahospitalaria se recogen en la tabla 1. Para su estimación se utilizó la técnica de eliminación hacia atrás; los niveles de significación para la selección y eliminación de los factores fueron p <0,05 y p ≥ 0,10, respectivamente. La calibración se analizó gráficamente tras agrupar a los pacientes en deciles con respecto a las probabilidades predichas y tabular las probabilidades medias predichas frente las observadas y la discriminación mediante el área bajo las curvas receiver operating characteristic (AUROC). A partir de los modelos especificados se calcularon las razones de mortalidad intrahospitalaria estandarizadas por riesgo como el cociente entre el resultado previsto (que considera individualmente el funcionamiento del hospital donde se atiende al paciente) y el esperado (que considera un funcionamiento estándar según la media de todos los hospitales) multiplicado por la tasa bruta de mortalidad13.
Para minimizar el sesgo de selección en la comparación de resultados entre la SVA y el TAVI se evaluó el impacto de ambos procedimientos en la mortalidad intrahospitalaria mediante emparejamiento por puntuaciones de propensión (opción k-nearest neighbors matching, psmatch2, Stata), seleccionando entre los episodios con SVA aquellos con perfil más parecido a cada episodio de TAVI, según las características demográficas y las comorbilidades de los pacientes. El emparejamiento se realizó a partir de los modelos de ajuste por riesgo, con proporción 1:1 y sin reemplazo. Se calculó la probabilidad de muerte intrahospitalaria, el efecto de las diferencias entre ambos grupos (efecto promedio del tratamiento o average treatment effect [ATT]) y las OR con sus intervalos de confianza del 95% (IC95%).
Estancia mediaPara el ajuste de la duración de la estancia, teniendo en cuenta la naturaleza sesgada de su distribución14, se utilizó un modelo de regresión de Poisson multinivel con efectos mixtos y se consideraron como factores de riesgo, además del año del alta, la edad y el sexo del paciente, así como los niveles de gravedad de los grupos relacionados por el diagnóstico refinados por todos los pacientes (en inglés, APR-GRD). La duración esperada de la estancia se obtuvo a partir de las predicciones individuales resultantes del modelo ajustado y se calculó la razón de la duración de la estancia ajustada por riesgo como el cociente entre la duración de la estancia observada y la esperada.
Para analizar la incidencia de complicaciones en ambos procedimientos se contrastaron las tasas brutas.
En todos los modelos multinivel se calcularon las OR y sus IC95%. Las variables cuantitativas se expresaron como medias±desviación estándar y las cualitativas, como frecuencias y porcentajes. Para la comparación entre variables cuantitativas se utilizó la t de Student para 2 categorías y análisis de la varianza (ANOVA), con corrección del nivel de significación con el método de Bonferroni, para 3 o más. Las comparaciones entre variables categóricas se realizaron mediante la prueba χ2 o el estadístico exacto de Fisher. Todos los contrastes realizados fueron bilaterales y las diferencias se consideraron significativas para p <0,05. Los análisis estadísticos se realizaron con STATA 13 y SPSS 21.0.
ResultadosSe identificaron 17.343 episodios de hospitalización con uno o más procedimientos de TAVI o SVA en> 17 años, de los que se seleccionaron, tras las exclusiones (fig. 1), 1.725 episodios de TAVI y 8.616 de SVA; 16 episodios de TAVI recibieron también SVA.
Las diferencias en el perfil de los pacientes intervenidos mediante SVA y TAVI se muestran en la tabla 1. En los pacientes con TAVI, la edad media y la proporción de mujeres fueron significativamente mayores que en los pacientes con SVA (81,1±6,6 frente a 70,2±11,4 años y 52,2 frente a 42,9%, respectivamente; p <0,001 en ambos casos). El índice de Charlson también era significativamente más alto en los pacientes con TAVI (7,2±1,6 frente a 6,5±1,7; p <0,001), con mayor proporción de condiciones crónicas.
La tasa bruta de mortalidad fue del 4,46% en lo pacientes tratados mediante TAVI y del 4,53% en los tratados mediante SVA. El modelo de ajuste para la mortalidad intrahospitalaria del remplazo valvular aórtico (SVA+TAVI) (tabla 2) mostró una buena discriminación (AUROC=0,81; IC95%, 0,79-0,83) y calibración (p <0,001) (figura 1 del material adicional). La OR mediana del modelo fue de 1,58, lo que denota una elevada variabilidad interhospitalaria.
Análisis multivariante de la mortalidad intrahospitalaria de pacientes con procedimientos TAVI o SVA
| Factores de riesgo | OR | IC95% | p |
|---|---|---|---|
| Edad | 1,02 | 1,01-1,04 | <0,001 |
| Sexo | 1,33 | 1,08-1,63 | 0,007 |
| Procedimiento (SVA) | 1,71 | 1,28-2,29 | <0,001 |
| Antecendentes de revascularización aortocoronaria (CABG) o de cirugía valvular cardiaca | 1,80 | 1,16-2,80 | 0,009 |
| Enfermedad hepática o biliar (CC 27-32) | 5,32 | 3,91-7,25 | <0,001 |
| Insuficiencia cardiaca congestive (CC 85) | 2,48 | 1,99-3,09 | <0,001 |
| Angina inestable y otras enfermedades cardiacas isquémicas agudas (CC 87) | 3,04 | 1,36-6,78 | 0,007 |
| Angina; antiguo infarto de miocardio | 2,08 | 1,11-3,88 | 0,022 |
| Ictus (CC 99-100) | 4,15 | 2,47-6,95 | <0,001 |
| Enfermedad vascular o circulatoria (CC 106-109) | 2,03 | 1,60-2,57 | <0,001 |
| Neumonía (CC 114-116) | 7,43 | 4,87-11,33 | <0,001 |
| Insuficiencia renal (CC 135-140) | 4,73 | 3,84-5,84 | <0,001 |
CABG: cirugía de revascularización coronaria; CC: condiciones clínicas; IC95%: intervalo de confianza del 95%; OR: odds ratio; SVA: sustitución valvular aórtica quirúrgica; TAVI: implante percutáneo de válvula aórtica.
El TAVI se asoció con menor riesgo de fallecimiento que la SVA (OR=0,58; IC95%, 0,44-0,7; p <0,001). Los factores de riesgo con mayor peso predictivo de la mortalidad intrahospitalaria fueron la neumonía, la insuficiencia hepática y la insuficiencia renal (OR=7,4; IC95%, 4,9-11,3; OR=4,7; IC95%, 3,8-5,8; con p <0,001 en ambos casos) (tabla 2). La menor probabilidad de muerte intrahospitalaria a igualdad de riesgo para TAVI frente SVA también se halló mediante emparejamiento por puntuaciones de propensión (ATT: 0,060 frente a 0,059; OR=0,49; IC95%, 0,36-0,66; χ2, p <0,001) (tabla 2 del material adicional). La razón ajustada de mortalidad estandarizada por riesgo para TAVI era significativamente inferior a SVA (4,8±1,8 frente a 4,9±1,9; p=0,028).
La estancia media bruta fue más elevada en aquellos pacientes con procedimiento de SVA que TAVI (11,7±10,5 frente a 15,1±14,3 días; p <0,001), manteniéndose la diferencia cuando se ajustaba por riesgo (razón de estancia ajustada por riesgo: 1,07 frente a 0,66; p <0,001).
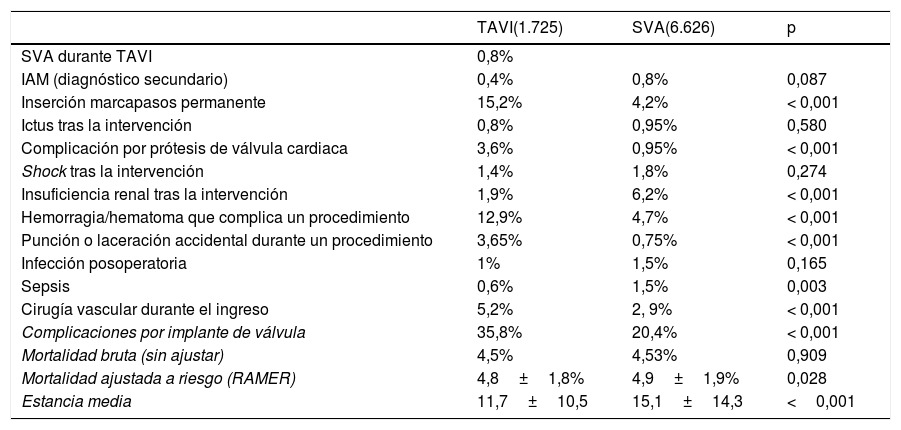
La incidencia bruta de complicaciones relacionadas con los procedimientos se muestra en la tabla 3. En TAVI fue mayor la proporción de complicaciones por inserción de marcapasos permanente (15,2 frente a 4,2%; p <0,001), complicaciones mecánicas por implante de válvula (3,6 frente a 1%; p <0,001), de cirugía vascular durante el ingreso en el TAVI (5,2 frente a 2,9%; p <0,001) y de hemorragia o hematoma que complica el procedimiento (12,9 frente a 4,7%; p <0,001) que en la SVA. Por el contrario, en SVA fue mayor la incidencia de insuficiencia renal tras la intervención (6,2 frente a 1,9%; p <0,001) y sepsis (1,5 frente a 0,6%; p <0,003). La tasa de incidencia total de complicaciones fue mayor en el TAVI que en la SVA (35,8 frente a 10,4%; p <0,001) (tabla 3).
Diferencias en resultados en pacientes TAVI o SVA
| TAVI(1.725) | SVA(6.626) | p | |
|---|---|---|---|
| SVA durante TAVI | 0,8% | ||
| IAM (diagnóstico secundario) | 0,4% | 0,8% | 0,087 |
| Inserción marcapasos permanente | 15,2% | 4,2% | < 0,001 |
| Ictus tras la intervención | 0,8% | 0,95% | 0,580 |
| Complicación por prótesis de válvula cardiaca | 3,6% | 0,95% | < 0,001 |
| Shock tras la intervención | 1,4% | 1,8% | 0,274 |
| Insuficiencia renal tras la intervención | 1,9% | 6,2% | < 0,001 |
| Hemorragia/hematoma que complica un procedimiento | 12,9% | 4,7% | < 0,001 |
| Punción o laceración accidental durante un procedimiento | 3,65% | 0,75% | < 0,001 |
| Infección posoperatoria | 1% | 1,5% | 0,165 |
| Sepsis | 0,6% | 1,5% | 0,003 |
| Cirugía vascular durante el ingreso | 5,2% | 2, 9% | < 0,001 |
| Complicaciones por implante de válvula | 35,8% | 20,4% | < 0,001 |
| Mortalidad bruta (sin ajustar) | 4,5% | 4,53% | 0,909 |
| Mortalidad ajustada a riesgo (RAMER) | 4,8±1,8% | 4,9±1,9% | 0,028 |
| Estancia media | 11,7±10,5 | 15,1±14,3 | <0,001 |
IAM: infarto agudo de miocardio; RAMER: razón ajustada de mortalidad estandarizado por riesgo; SVA: sustitución valvular aórtica quirúrgica; TAVI: implante percutáneo de válvula aórtica.
El presente estudio incluye la comparativa directa con datos de vida real con el mayor número de casos de estenosis aórtica grave sintomática e intervenidos mediante cirugía o TAVI en nuestro SNS publicado hasta ahora.
Su principal hallazgo es que, en un periodo en el que, probablemente la mayoría de los centros del SNS estaban en la curva de aprendizaje del TAVI, tratando una población de mayor comorbilidad y riesgo que la SVA (tabla 1), los resultados inmediatos (intrahospitalarios) de TAVI son significativamente mejores en cuanto a menor mortalidad y estancia media que la SVA. Por otro lado, hay que reseñar también que el implante percutáneo presentó una tasa superior en cuanto a algunas complicaciones no mortales específicas durante el ingreso. Así, se aprecia una tasa de incidencia mayor de complicación de válvula cardiaca, donde se incluye la fuga paravalvular-insuficiencia aórtica, la necesidad de implante de marcapasos definitivo y hemorragias derivadas del punto de acceso vascular, precisándose más frecuentemente cirugía vascular. Además, hubo un pequeño porcentaje de casos TAVI que necesitaron convertirse a SVA. Por otro lado, en nuestra cohorte, en la técnica quirúrgica abierta se constataron con mayor frecuencia otros problemas, como sepsis o insuficiencia renal (tabla 3).
Con todo, los resultados de nuestra serie son congruentes con los descritos en la literatura referidos en el mismo periodo15–20 de tiempo lo que apunta a que, con un potencial margen de mejora, son posiblemente bastante dependientes de la técnica en sí misma.
Como consecuencia de esto, en muchos países, el uso del TAVI ha superado al de la SVA3: en Finlandia, la TAVI sobrepasó a la SVA en 201621, mientras que ese año en Estados Unidos ya supuso el 43,2% (97,3% en mayores de 90 años y 72,2% entre 80 y 90 años), por ejemplo2. Lógicamente y tratándose de una nueva técnica, aún adolecemos de datos a largo plazo. No obstante, se disponen de muchos datos a medio plazo. Así, el estudio PARTNER 2 ya no encontró diferencias de mortalidad o ictus entre TAVI y SVA a los 5 años22.
Por tanto, los hallazgos de nuestro estudio se deben completar con el seguimiento a largo plazo y con las modificaciones en los resultados que presumiblemente puedan derivarse del esperable acúmulo de experiencia en los grupos intervencionistas y de la continua mejora de los dispositivos para TAVI. En general, el campo del TAVI ha sufrido un intenso desarrollo en los últimos 10 años con un gran incremento en sus números absolutos3, en paralelo a multitud de publicaciones, datos acumulados de ensayos clínicos y registros. Así, el TAVI actualmente se considera como un tratamiento plenamente consolidado. Esta evolución no habría sido posible sin el desarrollo de mejoras en las prótesis en sí mismas, con mejores procesos de crimpado y sus consecuentes menores perfiles, lo que ha permitido disminuir el tamaño de los introductores, mayor durabilidad y rendimiento hemodinámico, menores costes y más modelos disponibles de prótesis, produciéndose menos complicaciones23. Además, el procedimiento se ha simplificado mucho, incluso recomendándose anestesia local sobre la general, aspecto asociado a un importante impacto pronóstico periprocedural24.
Asimismo, la extensión de las nuevas indicaciones para tratar con TAVI a pacientes de bajo riesgo y las mencionadas mejoras en las prótesis y vías de acceso, probablemente reducirán sustancialmente la elevada incidencia de complicaciones del TAVI hallada en el periodo de la curva de aprendizaje al que se refiere nuestro estudio, lo que podría conllevar la adopción de este tratamiento transcatéter como primera elección para la mayor parte de los enfermos con estenosis aórtica.
LimitacionesAunque es un análisis retrospectivo basado en datos administrativos, la validez del uso de registros administrativos se ha contrastado con registros clínicos12,25 y la fiabilidad de estos estudios probablemente permite una comparación pública de hospitales en términos de resultados10. No obstante, no se ha validado la calidad del CMBD en la estenosis aórtica. Aunque es posible que una base de datos administrativa infraestime eventos clínicos (infarto o ictus durante el procedimiento) y comorbilidades, los datos de nuestra serie son similares a los comunicados en los registros. Asimismo, no se puede excluir la presencia de factores de confusión no medidos que pueden influir sobre los resultados. Al tratarse de resultados a muy corto plazo y de 2014-2015 cualquier inferencia al escenario actual de la técnica se debe hacer con cautela.
ConclusionesEn el periodo de la curva de aprendizaje (2014-2015) del TAVI y para una población más compleja que los pacientes sometidos a SVA, el TAVI mostró mejores resultados en cuanto a mortalidad intrahospitalaria y estancia media, si bien presentó mayor incidencia en algunas complicaciones no fatales. Estos hallazgos se deben confirmar mediante seguimiento a más largo plazo y en el marco de una esperable mejora de los resultados del TAVI, basados en la experiencia y conocimiento acumulado de este procedimiento.
- -
La estenosis aórtica es una enfermedad frecuente y progresiva que conlleva sustanciales tasas de morbimortalidad.
- -
El tratamiento clásico de sus estadios avanzados es el reemplazo valvular quirúrgico con circulación extracorpórea.
- -
En las últimas 2 décadas se han producido importantes avances en las técnicas de TAVI tanto en sala de hemodinámica como en quirófano, sin precisar circulación extracorpórea. Estas técnicas se han ido generalizando y actualmente están plenamente instauradas, suponiendo una alternativa al método quirúrgico tradicional o incluso son de primera elección en muchos casos.
- -
El presente estudio analiza el mayor número de casos de estenosis aórtica grave sintomática, tratada mediante cirugía o TAVI en España publicado hasta ahora.
- -
En una técnica hoy en día en expansión, considerando como «curva de aprendizaje» el periodo 2014-2015, se proporciona y se analizan los datos comparados de la vida real registrados en el CMBD del SNS español.
- -
Tras evaluar más de 17.000 episodios de TAVI o sustitución valvular quirúrgica, la primera opción aplicó a una población más compleja, mayor incidencia de complicaciones, pero mejores resultados (mortalidad y estancia media) intrahospitalarios.
Este estudio se ha financiado mediante una subvención no condicionada de la Fundación Interhospitalaria de Investigación Cardiovascular.
Conflictos de interesesNinguno en relación con el presente manuscrito.