La enfermedad de Kawasaki supone la segunda vasculitis más frecuente en la infancia. La implantación del tratamiento con inmunoglobulina intravenosa ha permitido reducir la historia natural de la enfermedad, así como disminuir la tasa de complicaciones cardiovasculares. Sin embargo, el aneurisma coronario y el infarto miocárdico siguen suponiendo sus principales complicaciones. La medición del diámetro coronario mediante ecocardiografía es la base del tratamiento del paciente con lesiones coronarias, ya que este tamaño es la principal variable que se emplea para decidir el plan de actuación. No obstante, se dispone de otras pruebas útiles para su valoración. Además del aneurisma, existen otras complicaciones cardiovasculares menos relevantes, como la miocarditis, el síndrome de shock, valvulopatías, etc. La creciente cohorte de pacientes con secuelas cardiovasculares que necesitan seguimiento obliga al aumento del interés de los facultativos en esta enfermedad.
Kawasaki disease means the second most frequent vasculitis in the pediatric age. The introduction of immunoglobulin therapy has achieved to reduce its natural history and the cardiovascular complications. Nevertheless, the main complication of Kawasaki disease are the coronary aneurysm and the following vessel obstruction. The coronary diameter measurement made from echocardiography is the basis in these patients’ clinical management since this size is considered the main determining factor to choose the most suitable therapy. Nonetheless, we have other useful tests that can be also used. Besides aneurysms, we can find less relevant cardiovascular complications such as myocarditis, shock syndrome, heart valve diseases, etc. The growing cohort of patients diagnosed in early childhood of cardiovascular complications needed of follow-up forces us to increase the interest of physician about this disease.
La enfermedad de Kawasaki (EK) es una vasculitis de arterias de mediano calibre autolimitada típicamente infantil, caracterizada por la presencia de las siguientes manifestaciones: fiebre alta, conjuntivitis bilateral no supurativa, cambios en labios y cavidad oral, exantema, cambios en las extremidades y presencia de una linfadenopatía cervical no supurativa. Se considera la segunda vasculitis de la infancia más frecuente1,2.
Sin embargo, aunque su fase aguda es predominantemente pediátrica, su importancia a largo plazo radica en sus efectos cardiovasculares, principalmente el aumento de riesgo de enfermedad coronaria a edades tempranas. La EK supone la principal causa de daño cardiaco adquirido en los países desarrollados3. Además, también se ha relacionado con un aumento del riesgo de desarrollo de cualquier otra enfermedad autoinmune y cáncer, así como de mayor mortalidad por cualquier causa4.
Su incidencia en Japón fue de 319,6 casos por cada 100.000 niños de 0 a 4 años durante los años 2015-2016, pero también puede aparecer en adolescentes y adultos con mucha menor frecuencia. En España no se dispone de datos, aunque comunidades como Cataluña la estimaron en 2016 en 8 de cada 100.000 niños en menores de 5 años1,5.
La etiopatogenia de la EK se desconoce actualmente, aunque influirían diversos factores genéticos, ambientales, infecciosos e inmunológicos.
La EK tiende a presentar una evolución trifásica, con una fase aguda en los primeros 7-14 días, una fase subaguda en las siguientes 4 semanas y una fase de convalecencia entre la cuarta y la octava semana tras el inicio de la enfermedad. Es en la fase subaguda donde hay más riesgo de aparición de secuelas cardiacas6.
Su tratamiento se basa en la combinación de dosis altas de inmunoglobulina intravenosa junto a aspirina a dosis antiinflamatorias, lo que ha conseguido reducir la incidencia de aneurismas coronarios, acortar la fiebre y mejorar los parámetros de laboratorio. Sin embargo, cerca del 20% de los niños presentan fiebre persistente. Esta entidad se denomina «refractariedad a inmunoglobulina intravenosa», con distintos factores que aumentan el riesgo de padecerlo, como la administración del tratamiento tras el cuarto día de fiebre, una velocidad de sedimentación glomerular incrementada o el descenso de hemoglobina y plaquetas. Si se sospecha de resistencia, se dispone de una serie de tratamientos coadyuvantes, como los corticoides o los inhibidores de la calcineurina6,7.
Los objetivos de este artículo son los de presentar las características básicas de esta enfermedad, reseñar la importancia de sus complicaciones cardiovasculares y cómo estas deben tratarse, y exponer las diferencias entre las 2 principales guías del tratamiento de estas a nivel global.
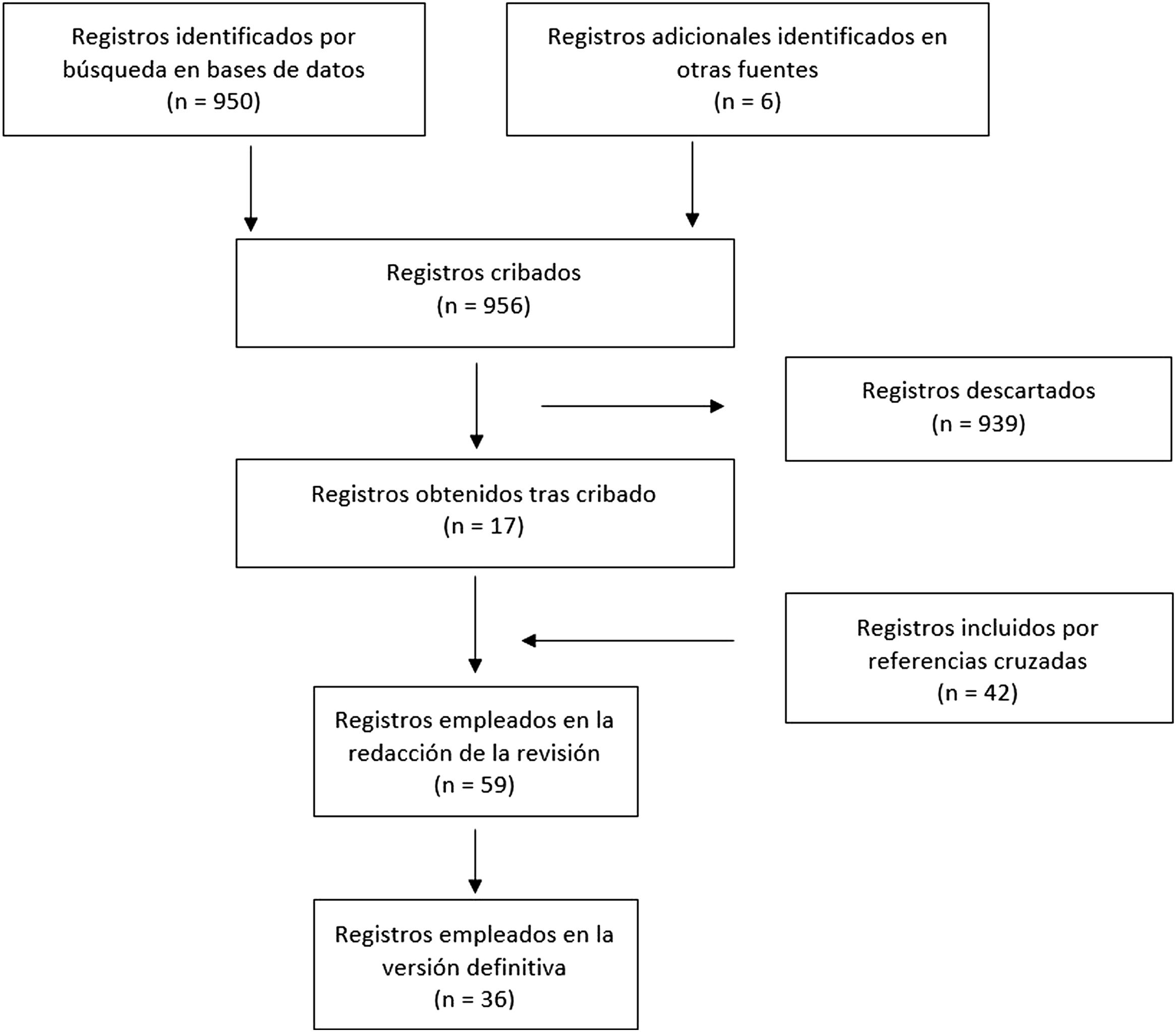
MétodosPara llevar a cabo la presente revisión bibliográfica se ha utilizado la siguiente estrategia de búsqueda en PubMed/MEDLINE, incluyendo solo los artículos publicados en los últimos 5 años: “Kawasaki Disease” AND (“autoimmune disease” OR “cardiovascular prognosis” OR “multisystem inflammatory syndrome in children”). Se encontraron 950 artículos a día 13 de febrero de 2022. Además, se obtuvieron 6 textos de otras fuentes, sumando un total de 956 documentos.
Se estimaron aquellos estudios sobre la EK en general y sobre sus complicaciones cardiovasculares en particular, ya fuesen revisiones narrativas, sistemáticas o trabajos experimentales realizados sobre humanos o animales. Tras el cribado, se desestiman 939 documentos. De los 17 restantes, mediante referencias cruzadas que aparecen en los respectivos apartados de la bibliografía, se seleccionan 42 artículos. En total, la redacción se inicia con estos 59 registros. Finalmente, el manuscrito emplea 36 referencias. En la figura 1 aparece el diagrama de flujo que expone la secuencia de búsqueda y cribado.
Resultados y discusiónConcepto y epidemiología de las manifestaciones y complicaciones cardiovascularesDurante la fase aguda de la enfermedad y posteriormente aparecen alteraciones cardiovasculares que pueden pasar desapercibidas si los pacientes no son sometidos a un estudio exhaustivo. Estas manifestaciones y sus complicaciones son la principal causa de morbimortalidad de la EK, aunque se mueven en un amplio espectro de gravedad, desde alteraciones inespecíficas en un electrocardiograma hasta la muerte súbita. En Japón, durante la fase aguda aparecen complicaciones cardiovasculares en el 7,9%. En fases posteriores, se desarrollan secuelas en el 2,3%, siendo más frecuentes en varones, excepto las valvulopatías5.
Clínica y diagnóstico durante la fase agudaHallazgos clínicosDurante la fase aguda se afectan pericardio, miocardio y endocardio, incluidas las válvulas y las arterias coronarias. Aunque la clínica es típicamente inespecífica, destacan el precordio hiperdinámico y la taquicardia. En ocasiones se consigue auscultar un soplo pansistólico en foco mitral y, más raramente, uno diastólico en foco aórtico, que se corresponden con disfunciones valvulares. La presencia de roce pericárdico a la auscultación o de signos de taponamiento cardiaco son menos comunes3.
Hallazgos ecocardiográficosLa ecocardiografía transtorácica es la base del diagnóstico y seguimiento por imagen, siendo capaz de valorar la morfología y el tamaño de las coronarias, lesiones valvulares y la función del ventrículo izquierdo. Además, permite valorar la miocarditis y la disfunción sistólica del ventrículo izquierdo, el pericardio y los signos de insuficiencia mitral y aórtica.
Se recomienda realizarla en el momento del diagnóstico, de una a 2 semanas tras el inicio y de 5 a 6 semanas tras el alta en todos los casos. En aquellos donde se observen lesiones el seguimiento con ecocardiografía se prolongará en el tiempo, al menos 2 cada semana hasta que la lesión deje de crecer3,8,9.
En cuanto a la ecocardiografía de estrés, se puede emplear el ejercicio (preferible en niños mayores), la dobutamina (preferible en niños muy pequeños) o el dipiridamol para valorar la función ventricular izquierda. Esta prueba se puede emplear en el diagnóstico y el seguimiento de la isquemia cardiaca de forma mínimamente invasiva y sin radiación5.
Aneurismas y enfermedad coronarios en el contexto de la enfermedad de KawasakiEl aneurisma coronario es, con gran diferencia, la complicación cardiovascular princeps de la EK, ya que es el principal factor pronóstico de la misma y marca el manejo de la enfermedad a largo plazo. Concretamente, se producen alteraciones del flujo coronario dentro de estos aneurismas, lo que favorece la formación de trombos y el desarrollo de síndromes coronarios agudos. En la actualidad, con el tratamiento adecuado, su incidencia oscila en los 1-5% de los casos según las series, pero hasta el 1% desarrollará aneurismas gigantes a pesar del tratamiento adecuado3,5,10.
La evidencia ha demostrado que el riesgo de eventos cardiovasculares (trombosis, estenosis, intervención, infartos, muerte) es directamente proporcional al tamaño de los aneurismas. Hasta el 16% de los pacientes con aneurismas desarrollará una oclusión completa, pero puede ser clínicamente asintomática gracias a la formación de circulación colateral, y no es infrecuente que se detecte por primera vez en alguna prueba de imagen realizada durante el seguimiento11–13.
Las arterias más afectadas son el tronco común izquierdo (24%), la arteria coronaria derecha (20%) y la circunfleja (20%)3.
En la evaluación y diagnóstico de las secuelas cardiovasculares se emplean principalmente marcadores bioquímicos, el electrocardiograma, la ecocardiografía, la angiografía coronaria, la imagen de perfusión coronaria, la tomografía computarizada coronaria y la cardiorresonancia magnética.
La ecocardiografía es el principal instrumento de diagnóstico, valoración pronóstica y seguimiento de las lesiones coronarias. Se considera anormal un diámetro coronario superior a 3mm en niños menores de 5 años o 4mm en mayores de 5, aunque los expertos recomiendan el empleo del Z-score en mayores de 5 años (≥2,5)5. Para ello, escogemos el diámetro superior que encontremos en la arteria. En la tabla 1 observamos cómo se clasifican las lesiones coronarias según el tamaño5.
Clasificación de las lesiones coronarias según el tamaño medido por ecocardiografía transtorácica, según medición en milímetros y ajuste por Z-score
| Dilatación/ectasia (solo reconocida por la AHA) | Z-score entre 2 y 2,5 o también menor de 2 al inicio, pero que durante el seguimiento baja al menos un punto |
| Aneurisma pequeño | Z-score entre 2,5-5 o 3-4mm en niños menores de 5 años |
| Aneurisma mediano | Z-score entre 5-10 o 4-8mm en niños menores de 5 años |
| Aneurisma gigante | Z-score>10 o≥8mm sin importar la edad |
La clave de esta clasificación es el valor pronóstico del tamaño de las lesiones. Diversos estudios demuestran el mayor riesgo de persistencia de las alteraciones (el punto de no retorno sería de 5,6mm), trombosis y estenosis en los aneurismas de mayor tamaño5,14. Según Son et al., existe una diferencia estadísticamente significativa en la aparición de aneurismas tras la fase aguda entre aquellos pacientes con un Z-score basal≤2 (2%) y≥2 (16%), con p<0,00115.
Por otro lado, el cálculo del Z-score permite la estandarización con el objetivo de poder comparar medidas. Actualmente, se considera que los métodos más rigurosos serían el de los japoneses, con un método lambda-mu-sigma para el análisis de regresión de la superficie corporal16, y el canadiense, mediante la función de raíz cuadrada para el cálculo de la superficie17.
Sin embargo, la sensibilidad y la especificidad de esta prueba para detectar trombosis y estenosis no son claras y la visualización de las coronarias se va complicando en cuanto el niño crece y su tamaño aumenta. Por ello, es recomendable el empleo de otras técnicas de imagen3.
En este sentido, la tomografía computarizada cardiaca y la cardiorresonancia magnética han permitido mejorar la resolución y precisión en lesiones estenóticas, habiendo reemplazado parcialmente a la coronariografía. La tomografía computarizada permite el empleo de scores basados en el calcio detectado en las coronarias. Kahn et al. demostraron en 2017 que el calcio de los vasos puede ser utilizado para diagnosticar alteraciones coronarias no detectadas previamente en pacientes con certeza o sospecha de antecedente de EK (sensibilidad del 95% y especificidad del 100%)5,18. Por otra parte, la cardiorresonancia magnética se emplea más para valorar la morfología del miocardio, la función cardiaca y el desplazamiento de las paredes. En adultos, un metaanálisis ha demostrado su utilidad para diagnosticar lesiones coronarias causantes de isquemia mediante test de estrés con gadolinio (sensibilidad del 90% y especificidad del 85%)5,19.
Por otra parte, la imagen de perfusión miocárdica con tecnecio-99 y la tomografía por emisión de positrones permiten la detección de isquemia en pacientes con alteraciones coronarias, así como revelar alteraciones no estructurales de las arterias en ausencia de dilataciones. Así, Kashyap et al. demostraron que aparecían resultados positivos en estas pruebas en pacientes sin lesiones coronarias visibles, que se debían a una disfunción endotelial5,20.
En cuanto al análisis sérico, se debe centrar en 2 aspectos: las enzimas de daño miocárdico mediante la determinación de troponina T ante toda sospecha de evento isquémico, y los marcadores de arterioesclerosis (moléculas de perfil lipídico como las lipoproteínas de baja densidad y los triglicéridos). Ya existen estudios que demuestran que los pacientes con EK tienen mayores niveles de colesterol total y apolipoproteína B (principal componente lipoproteico de la lipoproteína de muy baja densidad y lipoproteínas de baja densidad), lo que demuestra el mayor riesgo de arterioesclerosis en estos pacientes5,21.
Finalmente, la angiografía coronaria es la prueba de imagen más invasiva de la que disponemos para la evaluación en la EK, pero nos permite una imagen detallada de la luz arterial, siendo la técnica gold standard para la evaluación del grado de estenosis, el pronóstico y la elección de tratamiento5.
Permite valorar el origen de las alteraciones detectadas y la estructura y dinámica de flujo dentro de la arteria, así como definir el concepto de «estenosis significativa» cuando la obstrucción es≥75% en una arteria coronaria principal o≥50% en el tronco principal de la coronaria izquierda. En estos casos, es deseable realizar varios procesos diagnósticos por imagen en intervalos de 6 meses a años según la progresión, incluso en ausencia de signos de isquemia3,5,12.
Si se desarrolla oclusión crónica, en todos los casos se encuentra circulación colateral, siendo típicamente suficiente para evitar lesiones isquémicas. Por otra parte, la coronariografía clásica se complementa mediante sensores de presión intracoronarios, ecografía intravascular y mediciones de la velocidad del flujo coronario mediante Doppler para evaluar la gravedad de la funcionalidad en una estenosis, antes, durante y después de la terapia de reperfusión5.
Entre las desventajas e inconvenientes del cateterismo destacan una mortalidad menor del 0,2% y otras complicaciones como trastornos cerebrovasculares, infartos y hemorragias (<0,5%). También se debe tener en cuenta la exposición a radiación ionizante y el riesgo de hematomas y pseudoaneurismas en la arteria femoral por la punción en pacientes anticoagulados5.
Estratificación del riesgo coronarioSi tras el primer mes desde el inicio persiste alguna dilatación la lesión se denomina «secuela coronaria». Para su tratamiento se han desarrollado clasificaciones según el tamaño y la regresión o persistencia de las lesiones, siendo estos claves en el seguimiento, la profilaxis y el tratamiento de los pacientes de forma individualizada. Los principales son los de la American Heart Association de 2017 y la de las Japanese Circulatory Society/Japanese Society of Cardiac Surgery de 2020, que aparecen recogidas en la tabla 23,5.
Comparación de las clasificaciones de estratificación del riesgo coronario de la JCS/JSCS (2020) y AHA (2017)
| JCS/JSCS (2020) | AHA (2017) |
|---|---|
| Ausencia de dilatación en la fase aguda | Ausencia de lesiones en todo momento: Z-score<2 |
| Dilatación transitoria en la fase aguda: dilatación leve que normaliza en el primer mes tras el inicio | Ectasia: Z-score 2 a<2,5 |
| Regresión: lesión(es) que continuaba(n) tras el primer mes ha(n) desaparecido durante el seguimiento y no se ha pasado al grupo v | Aneurisma pequeño: ≥2,5 a<5 |
| Presente o persistente | |
| Regresión a ectasia o tamaño normal | |
| Persistencia de aneurismas | Aneurisma mediano: Z-score≥5 a<10 y tamaño<8mm |
| Presente o persistente | |
| Regresión a aneurisma pequeño | |
| Regresión a ectasia o tamaño normal | |
| Lesión coronaria estenótica | Aneurisma gigante: Z-score≥10 o un tamaño de≥8mm |
| Sin signos isquémicos | Presente o persistente |
| Con signos isquémicos | Regresión a aneurisma mediano |
| Regresión a aneurisma pequeño | |
| Regresión a ectasia o tamaño normal |
Aparte del tamaño, existen otros factores que aumentan el riesgo y, por tanto, deben influir en el tratamiento, como son el número total de aneurismas, el número total de ramas afectadas, la presencia de irregularidades en la luz, la ausencia de vasos colaterales, la presencia de anormalidades funcionales o la presencia de infartos o trombos previos3.
Tratamiento de la enfermedad coronariaEl tratamiento de las secuelas cardiovasculares de la EK se basa principalmente en la prevención de la trombosis en las lesiones coronarias y en su tratamiento cuando aparecen oclusiones. Realmente es muy similar a la prevención secundaria de la enfermedad coronaria aterotrombótica; sin embargo, varios fármacos que se emplean en ese caso no están indicados para niños5.
En la tabla 3 aparecen los fármacos recomendados dependiendo del riesgo que presenten3,5.
Fármacos recomendados en la prevención del evento cardiaco en el contexto de la enfermedad de Kawasaki
| Fármaco | Indicaciones e información complementaria | Nivel de evidencia |
|---|---|---|
| Ácido acetilsalicílico | Dosis antiagregantes 2-3 meses en todos los casos, desprescribiéndose si no aparecen aneurismas. Si aparecen, se indica de manera indefinida | Clase I, nivel C |
| Heparina sódica/enoxaparina | En fase aguda si aparecen aneurismas, sobre todo en aquellos gigantes | Clase IIa, nivel C en caso de aneurismas gigantes persistentes |
| Anticoagulación oralWarfarina | Tras la fase aguda se deben administrar junto a aspirina en aquellos casos donde persistan aneurismas, especialmente en los gigantes y los que pasan de gigante a mediano. La dosis del anticoagulante debe ser controlada mediante la medición del INR (2-2,5/3)La transición de HBPM a warfarina se recomienda cuando los aneurismas han dejado de crecer y el paciente está estable. Actualmente, los anticoagulantes de acción directa no están aprobados en niños | Clase IIb, excepto la indicación en gigantes persistentes y gigantes con regresión a mediano, que tiene una evidencia de clase iia |
| Otros antiagregantesClopidogrel, ticlopidina, dipiridamol | Se pueden emplear junto a aspirina en aquellos pacientes con aneurismas de tamaño mediano o gigante como terapia sustitutiva de la anticoagulación. En caso de alto riesgo de trombosis coronaria se puede mantener una triple terapia con doble anticoagulación y anticoagulación oral | Clase IIb para la AHA y clase iia y nivel C para la JCS/JSCS |
| Bloqueadores betaCarvedilol, metoprolol | Pacientes con aneurismas gigantes persistentes o que hayan regresado a tamaño mediano o pequeño a partir de uno gigante | Clase IIb, nivel C |
| Estatinas | Pacientes con aneurismas (persistentes o que hayan regresado a la normalidad) por su efecto pleiotrópico y antiinflamatorio, la inhibición de la coagulación y la promoción de la trombólisis | Clase IIb, nivel C |
| Bloqueantes del SRAACandesartán | Se podrían indicar para prevenir la estenosis arterial secundaria al engrosamiento de la íntima en pacientes con aneurismas | Clase IIb, nivel C |
| OtrosCalcioantagonistas dihidropiridínicos, nitratos | Para evitar el vasoespasmo o como control sintomático antianginoso | Clase IIb, nivel C |
Los niños más pequeños con infarto agudo de miocardio pueden presentar una clínica diferente a la del adulto, con palidez, vómitos y dolor abdominal, mientras el dolor torácico suele aparecer en niños más mayores8.
El tratamiento de reperfusión urgente se recomienda en las 12 primeras horas desde el inicio del cuadro y en las 2 primeras horas desde que se entra al hospital en los casos de infarto agudo de miocardio con elevación del ST o con obstrucción completa del tronco común izquierdo.
Existe controversia sobre la implantación o no del stent. Aunque aparecen buenos resultados con su implantación (Oda et al.22), la Japanese Circulatory Society/Japanese Society of Cardiac Surgery no recomienda su uso y se inclina más hacia la angioplastia única con balón. Por otro lado, la American Heart Association refiere que la técnica con balón no ofrece resultados duraderos, por lo que, a pesar de ser complicada su implantación en una arteria tan dañada, sería preferible junto con una ecografía intravaso para asegurar su fijación3,5.
En los niños más pequeños puede indicarse terapia trombolítica farmacológica (urocinasa o tecnoplase, junto con ácido acetilsalicílico y heparina sódica). Su empleo y eficacia quedan evidenciados por la encuesta nacional japonesa sobre su uso en niños con obstrucción coronaria entre 2004-2009, donde el 64% de los centros japoneses que participaron la emplearon, con un porcentaje de éxito del 75%23. En los casos donde se presente un gran trombo y haya un alto riesgo de oclusión, se puede reducir la dosis de tecnoplase si se añade un inhibidor de la glucoproteína iib/iiia. Este fármaco también ha demostrado reducir a los 5 años el tamaño del aneurisma en comparación con pacientes a los que no fue administrado (Z-score −14,0±4,0 frente a −8,2±5,9; p=0,04)24.
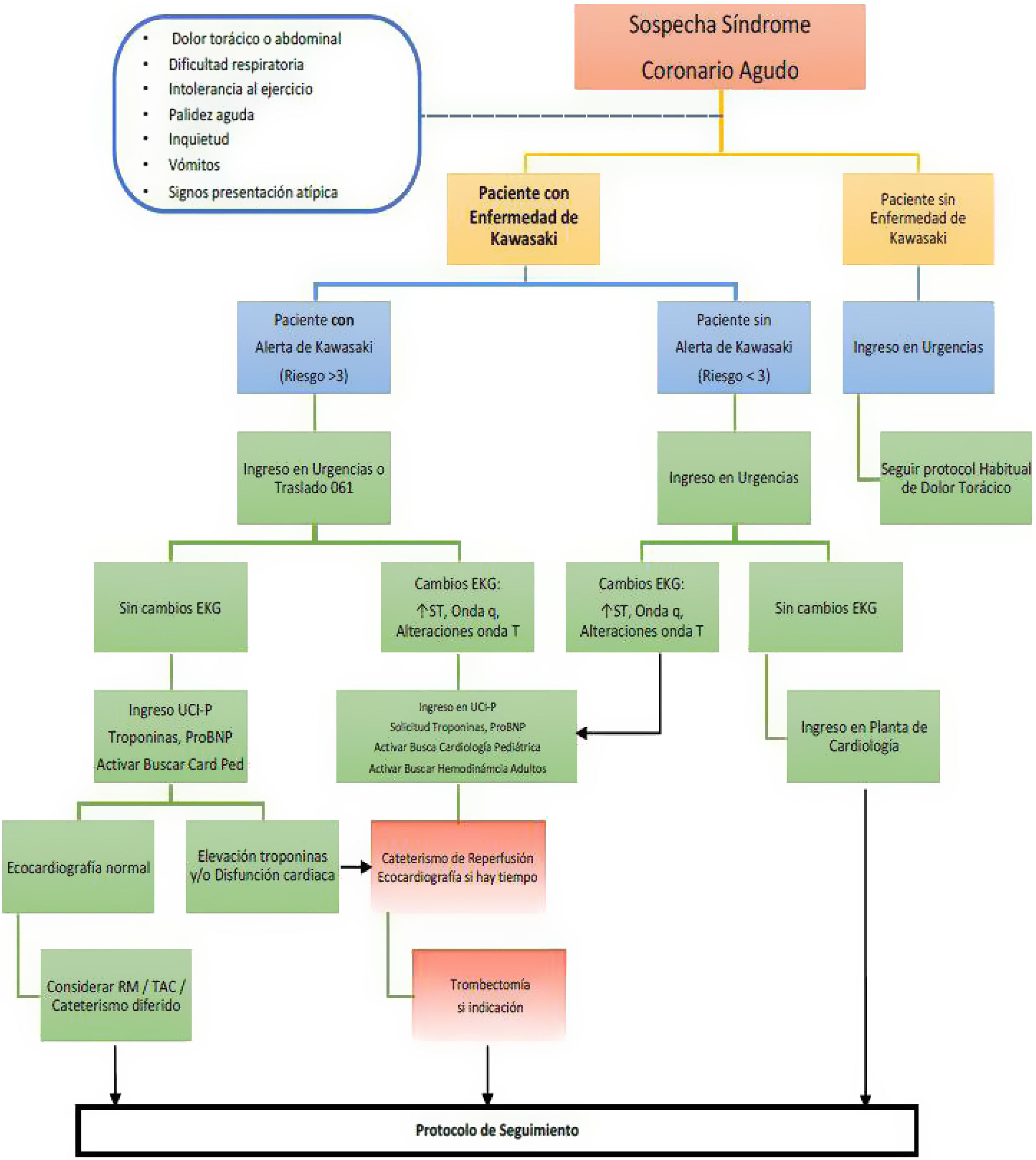
En la figura 2 podemos observar un algoritmo que se sigue en caso de sospecha de síndrome coronario agudo en niños con antecedentes de EK.
Protocolo de síndrome coronario agudo en menores de 14 años con antecedentes de enfermedad de Kawasaki. El nivel de riesgo 3 equivale a la presencia de un aneurisma de pequeño tamaño. EKG: electrocardiograma; ProBNP: propéptido natriurético cerebral; RM: resonancia magnética; TAC: tomografía axial computarizada; UCI-P: Unidad de Cuidados Intensivos pediátrica.
Cortesía de Santos y Valverde.
Como en la enfermedad coronaria aterotrombótica, se dispone de 2 técnicas para la reperfusión de la enfermedad crónica: la angioplastia percutánea y la cirugía aortocoronaria. Estos procedimientos se recomiendan en aquellos pacientes con angina refractaria al tratamiento médico o aquella angina estable y de alto riesgo por la anatomía arterial, así como ante una estenosis significativa de un vaso principal incluso ante la ausencia de signos isquémicos durante las exploraciones. La elección del procedimiento depende de las características del paciente y de las lesiones. En la tabla 4 figuran los principales criterios de selección3,5.
Recomendaciones de angioplastia o cirugía de bypass según las condiciones de las lesiones o del paciente
| Angioplastia percutánea | Cirugía de bypass |
|---|---|
| Afectación de un solo vasoAfectación multivaso focal susceptible de angioplastia | Estenosis significativa en el tronco común izquierdo≥50%Enfermedad multivasoDiabetes mellitus/SYNTAX>22Estenosis en la porción proximal de descendente anteriorColaterales comprometidasLesiones no susceptibles de revascularización percutánea |
Con respecto a la cirugía, el injerto debe provenir de las arterias torácicas internas siempre que sea posible por su menor tasa de reestenosis en el futuro, ya que posee una tasa de permeabilidad a los 20 años del 87% (intervalo de confianza del 95% [IC95%] 78-95) en comparación con el 44% (IC95% 26-61) de injertos de vena safena. La supervivencia a largo plazo de los pacientes sometidos a cirugía es alta, de hasta el 95% (IC95% 88-98) a los 25 años25.
Evolución y seguimientoSegún Tsuda et al.26, en un seguimiento durante 15 años, los aneurismas menores de 6mm no sufrían procesos trombóticos, mientras los moderados de 6-8mm los tenían en un 58% y los gigantes≥8mm, en el 74% de los casos. Por otra parte, la oclusión trombótica y el infarto asociado ocurren frecuentemente antes de los 2 años del inicio. Estos eventos disminuyen la supervivencia del 88% a los 30 años al 59% a los 25. En definitiva, a pesar de estos datos, la mortalidad de estos pacientes es baja, siendo la principal causa el infarto agudo de miocardio en aquellos con aneurismas gigantes durante el primer año, por lo que esta enfermedad supondría entre el 5-9,1% de los infartos agudos de miocardio en adultos menores de 40 años. Por datos como estos, es clave un seguimiento exhaustivo a corto y largo plazo, en especial a los grados más graves, mientras que se puede desestimar el mismo a los 5 años en aquellos sin lesiones persistentes1,2,5.
El seguimiento suele iniciarse a las 4-6 semanas del inicio de la fiebre, cuando los síntomas han desaparecido y la enfermedad coronaria ha alcanzado sus máximas dimensiones. Sus objetivos son prevenir la trombosis y el infarto de miocardio mientras se consigue un mantenimiento óptimo de la salud cardiaca. No hay evidencia de riesgo coronario en pacientes sin secuelas coronarias, incluyendo la dilatación transitoria. Aproximadamente el 50% de las lesiones remiten en el primer año, pero las de mayor tamaño lo tendrán más difícil y los de tamaño gigante raramente se repararán. Aunque remita, la estructura vascular no se normaliza, la disfunción endotelial y el remodelamiento continúan y pueden aparecer estenosis, oclusiones y a veces reexpansiones. La rotura del aneurisma ocurre durante el primer mes (los gigantes en las 2-3 primeras semanas), es decir, en fases más precoces, pudiendo ocasionar isquemia o un taponamiento cardiaco3,5.
El pico de mortalidad ocurre entre los días 15-45 desde el inicio de la fiebre, cuando coincide el establecimiento de la vasculitis coronaria con la trombocitosis y un estado de hipercoagulación. Sin embargo, la muerte repentina por infarto de miocardio puede suceder muchos años después3.
Si se sigue la guía japonesa, el seguimiento depende del grado de riesgo según las lesiones.
Recomendaciones- -
Control de los factores de riesgo cardiovascular: aunque es cierto que la patogenia del trombo coronario por EK no es la misma que la de la enfermedad coronaria clásica, podría reducir el riesgo de eventos21.
- -
Recomendaciones de limitación del ejercicio físico: solo en caso de presencia de aneurisma. Estos pacientes tienen mayor riesgo de obesidad, probablemente por la reducción de los niveles de ejercicio físico hasta en un 50% en comparación con sus compañeros en edad escolar9,27.
- -
Consejo reproductivo3:
- ∘
Se prefieren aquellos anticonceptivos con bajos niveles de estrógenos o que solo contengan progestágenos, o directamente el empleo de otros métodos anticonceptivos no hormonales.
- ∘
Si existe deseo genésico se debe cambiar la warfarina por enoxaparina o una terapia antiagregante dual durante el embarazo y el parto. Además, deben interrumpirse los tratamientos con bloqueantes del sistema renina-angiotensina-aldosterona y estatinas.
Desde el punto de vista histopatológico, la miocarditis por EK es más prevalente que los aneurismas coronarios, encontrándose en la mayoría de los pacientes durante la fase aguda (50-70% de todos los casos); además, constituye la principal causa de muerte precoz. Sin embargo, es subclínica en la gran mayoría de los pacientes o a lo sumo se presenta con una clínica y unos signos ecocardiográficos y electrocardiográficos leves3,29. El diagnóstico se basa en hallazgos clínicos y pruebas de imagen28,29.
Se aprecia ritmo de galope (13% en los primeros 20 días), aumento del índice cardiotorácico en la radiografía posteroanterior de tórax (20%), anormalidades electrocardiográficas en el 40% (prolongación del segmento PR, prolongación del intervalo QTc, cambios en el segmento ST y baja amplitud de la onda R y T) y reducción de la fracción de eyección del ventrículo izquierdo por debajo del 32% en el 19% de los pacientes. En definitiva, el 51% de los pacientes presentan al menos uno de estos criterios de miocarditis aguda al inicio del cuadro. También es útil la elevación del NT-ProBNP secundaria al fallo ventricular en el diagnóstico y para diferenciar la enfermedad de otros procesos febriles, como demuestra un metaanálisis de 2015 (sensibilidad del 89% [IC95% 78-95] y especificidad del 72% [IC95% 58-80])30.
En cuanto a las pruebas de imagen, destaca en primer lugar la ecocardiografía, que demuestra alteraciones de la función sistólica, como la reducción de la fracción de eyección en un 20-56% de los casos y el aumento de las dimensiones telesistólicas y telediastólicas del ventrículo izquierdo.
En segundo lugar, la resonancia magnética cardiaca es el método de referencia para la evaluación de la función auriculoventricular, aportando valor pronóstico. Además, el empleo de gadolinio es el mejor método para la detección de tejido miocárdico no viable o inflamado, por lo que se emplea de rutina en el diagnóstico y seguimiento de la miocarditis significativa. McCandless et al. plantearon que la reducción del pico sistólico de deformación miocárdica del ventrículo izquierdo y de la tasa de deformación miocárdica que se observan por resonancia magnética en la fase aguda de la EK podrían servir para ayudar al diagnóstico de la enfermedad y evitar retrasos en la instauración del tratamiento31.
Finalmente, la imagen nuclear con galio-67 realizada entre los días 5-16 tras el inicio demuestra signos de miocarditis en el 64%. Por otro lado, utilizando tecnecio-99, la miocarditis persiste hasta en el 54% de los pacientes entre las semanas 8 y 12, en contraposición a las series histológicas, donde desaparece a partir de los 20 días del inicio.
Respecto al tratamiento, es evidente que la miocarditis mejora tras la fase aguda, ya que se aprecia que el 57% de aquellos que comienzan con disfunción sistólica se normalizan a las 24h, el 85% en las primeras 48h y casi todos para la sexta semana. Esta mejoría se observa sobre todo en los 10 primeros días cuando se trata con inmunoglobulina intravenosa y ácido acetilsalicílico, pero persiste hasta los 12 meses en aquellos que solo reciben ácido acetilsalicílico. La función ventricular sistólica medida por resonancia magnética se normaliza en todos los casos en el seguimiento, excepto si se produce un infarto miocárdico significativo al inicio del desarrollo de un hipotético aneurisma28.
Sin embargo, la miocarditis grave puede llevar a un compromiso hemodinámico o a la aparición de arritmias fatales en la primera semana de enfermedad, aunque son muy poco frecuentes2,5.
Síndrome del shock cardiovascularEl síndrome del shock cardiovascular por EK se considera una complicación infrecuente, pero muy grave, que se define como hipotensión del componente sistólico y signos de ausencia de perfusión en pacientes con EK. Sucede aproximadamente en el 5% de los niños con EK en Estados Unidos y cursa con un colapso cardiovascular e hipotensión que requiere expansión de volumen y agentes vasoactivos, siendo la presencia de trombocitopenia y coagulopatía notable. Su patogenia es multifactorial y se debe principalmente al aumento de la permeabilidad vascular por la tormenta de citocinas que provoca un shock distributivo, y a la disfunción miocárdica, secundaria a la miocarditis que ocasiona un shock cardiogénico. Los niños con clínica compatible con el shock presentan mayores valores de proteína C reactiva (p=0,005) y troponinas cardiacas (p≤0,001), menor concentración de hemoglobina (p=0,003), hiponatremia (p=0,004), hipoalbuminemia (p=0,004), coagulopatía (p=0,03), mayor riesgo de resistencia a inmunoglobulina intravenosa, anormalidades de las arterias coronarias, insuficiencia mitral y disfunción miocárdica, pudiendo llegar hasta una mortalidad del 6,8%. Además, existe una relación inversa significativa entre el valor de la fracción de eyección del ventrículo izquierdo y la incidencia del shock (OR=0,82; IC95% 0,73-0,93; p=0,0019)3,32–34.
A pesar del incremento de resistencia a inmunoglobulina intravenosa, la mayoría responde al tratamiento. La función ventricular se normaliza en la mayoría de los pacientes de forma precoz cuando se administra inmunoglobulina intravenosa3.
Con la aparición del SARS-CoV-2 se describió un cuadro con características muy similares: el síndrome inflamatorio multisistémico en niños. Sin embargo, su letalidad es mayor, hasta el 18%. Se ha evidenciado que la vacunación con al menos una dosis de cualquier vacuna de ácido ribonucleico mensajero contra el SARS-CoV-2 reduciría hasta un 90% el riesgo de desarrollarlo en los menores de edad35,36.
Otras alteracionesLa EK produce alteraciones a otros niveles, aunque son menos significativas que las explicadas anteriormente. En primer lugar, en el 23-27% de los casos aparece una insuficiencia mitral, generalmente de carácter breve y que se autolimita a la fase aguda. Por otro lado, menos común es la insuficiencia aórtica (1%), que se relaciona con la dilatación de raíz aórtica y dilataciones coronarias. También podemos encontrar arritmias, anormalidades del nódulo sinusal y auriculoventricular, con intervalos PR alargados y cambios no específicos o bajo voltaje del ST y onda T; dilatación de la raíz aórtica y otras arterias de mediano calibre en al menos el 10% de los casos; y pericarditis leve3.
ConclusionesLa EK, a pesar de su baja incidencia, constituye una de las principales causas de daño cardiaco adquirido en la población más joven. Ante el supuesto aumento del número de diagnósticos por la mejora en la formación de los facultativos en la enfermedad, se espera un incremento proporcional de pacientes jóvenes con alteraciones cardiovasculares secundarias a la misma que necesitarán un seguimiento exhaustivo.
Por ello, es indispensable que se aumente cuanto antes el número de trabajos sobre este tema en nuestra población, en particular sobre nuevos tratamientos curativos y preventivos de las complicaciones cardiacas, así como la creación de una guía de manejo de la EK y sus consecuencias cardiovasculares por parte de la European Society of Cardiology, a semejanza de lo que ocurre en Japón y Estados Unidos con sus respectivas guías de actuación.
Contribución de los autoresA. García Núñez ha realizado la búsqueda bibliográfica y la redacción del manuscrito. N. Romero Rodríguez y J.L. Domínguez Cano han contribuido en la concepción inicial del manuscrito, así como en la revisión intelectual y aprobación de la versión final.
FinanciaciónLa presente investigación no ha recibido ninguna beca específica de agencias de los sectores público, comercial, o sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.