Durante alrededor de 50 años se ha utilizado la estimulación apical de ventrículo derecho. Sin embargo, esta técnica puede producir asincronías en pacientes que precisan estimulación frecuente, lo que se asocia a mayor riesgo de insuficiencia cardiaca, disfunción mitral y fibrilación auricular. La estimulación en sitios alternativos del ventrículo derecho, tales como el septo o el tracto de salida, no ha demostrado ser superior a la estimulación apical.
El interés en técnicas que simulen la estimulación fisiológica ha ido creciendo en los últimos años. Dentro de este tipo de técnicas, la más fisiológica y, a día de hoy la más utilizada, es la estimulación hisiana, con múltiples estudios que avalan su factibilidad y beneficios clínicos.
Huang et al.1 demostraron en 2017 la factibilidad de la estimulación por debajo del área del bloqueo en la rama izquierda en un paciente con bloqueo completo de rama izquierda y fallo cardiaco al conseguir la resincronización cardiaca.
La unidad de cuidados intensivos del Hospital Santa Ana ha iniciado un programa de estimulación en la rama izquierda en consenso con el servicio de cardiología de dicho hospital. El programa se inició porque la técnica de estimulación en la rama izquierda se considera que es un procedimiento seguro y reproducible en una unidad de cuidados intensivos con abordaje experto en marcapasos convencionales. Son muchos los dispositivos de electroestimulación cardiaca que se implantan fuera de los laboratorios de electrofisiología y, por ello, dicha técnica debe estar presente en hospitales que implanten marcapasos fuera de los laboratorios de electrofisiología.
Se presenta un estudio descriptivo prospectivo de 30 pacientes y su correspondiente seguimiento en consulta durante los 9primeros meses. Se confirma la obtención del consentimiento informado de los pacientes y la autorización del comité del hospital.
Estos implantes han sido realizados por 2 intensivistas formados en la estimulación en rama izquierda y supervisados por electrofisiólogos con amplia experiencia en la rama. Las intervenciones se hicieron mediante punción ecoguiada de la vena axilar izquierda. El electrodo Select Secure 3830-69 de Medtronic (Minneápolis, EE. UU.) se implantó avanzando sobre la vaina de curva fija C315-His, de Medtronic (Galway, Irlanda). El objetivo fue posicionar el electrodo en el septo muscular interventricular hasta conseguir un patrón de bloqueo de rama derecha (qR o qRS en V1) con la estimulación. La monitorización de la técnica se hizo con el sistema portátil de medición electrofisiológica con estimulador totalmente integrado EP-TRACER 2 Portable (Heilbronn, Alemania).
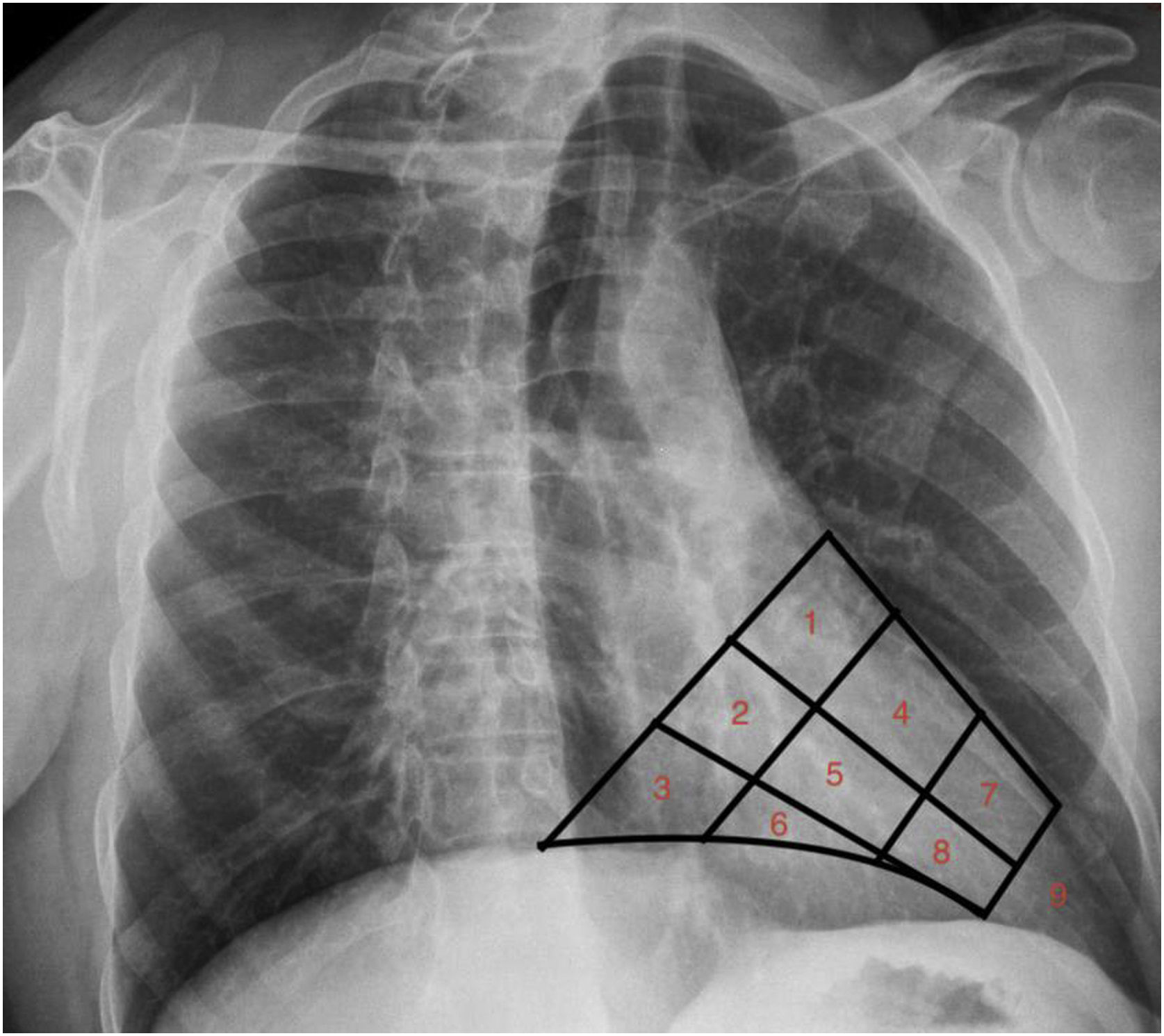
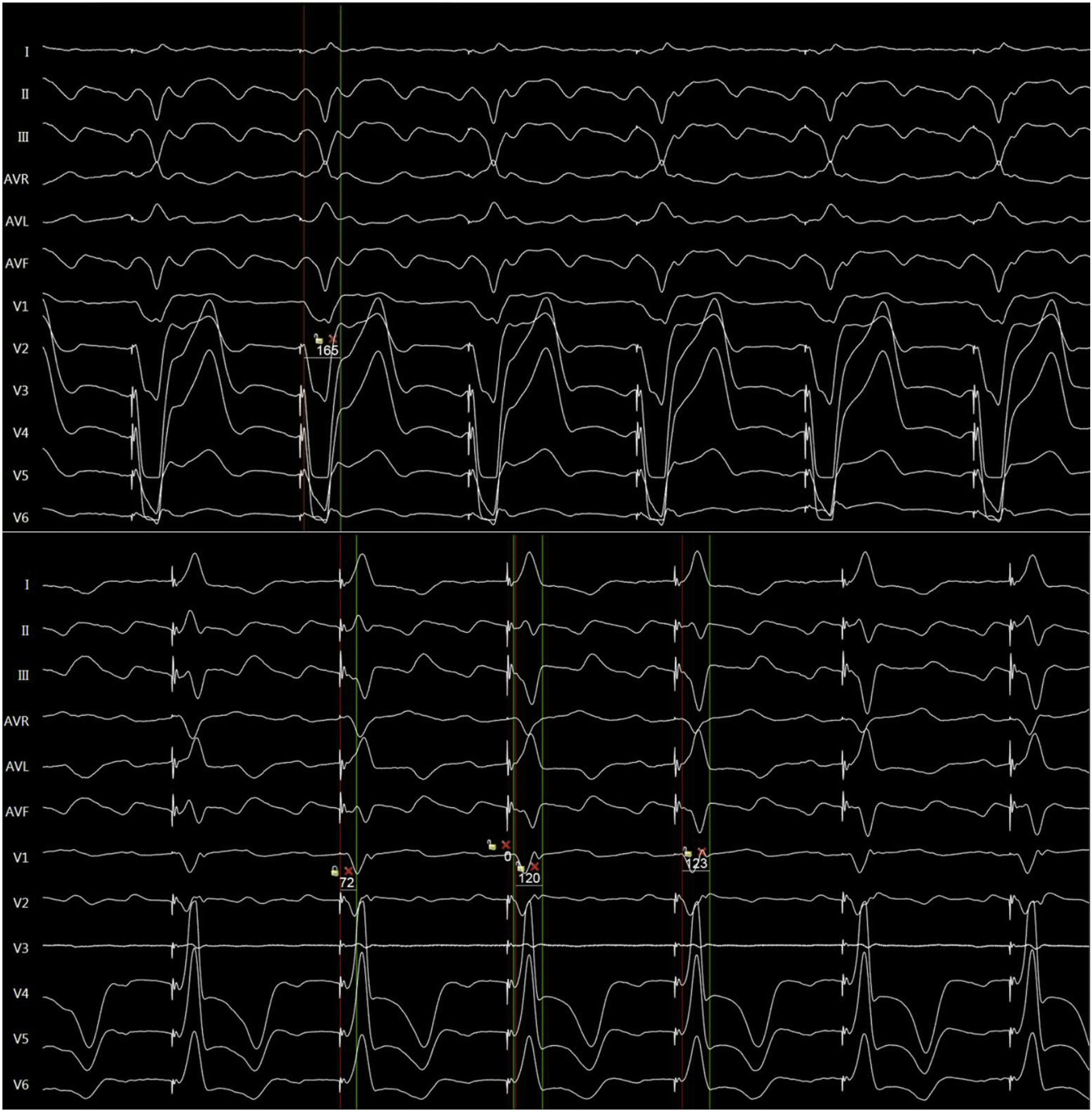
Para la correcta posición del electrodo se utiliza como referencia la imagen radiológica anterior oblicua derecha a 30 grados, dividiendo la silueta cardiaca en 9 segmentos: la división se empieza en la válvula tricúspide y el segmento 9 se sitúa en el ápex (fig. 1). Se realiza un muestreo de un 1,5cm sobre dicho segmento hacia el septo basal y el septo medio hasta obtener el patrón electrocardiográfico necesario al iniciar la estimulación en 5V a 0,4ms. Si se mantiene dicho patrón (qR o qRS en VI) (fig. 2), al disminuir el umbral de estimulación entre 3V y 5V, y tras una primera medición de la impedancia, se comienza a meter el electrodo en el septo intraventricular en una proyección radiológica oblicua izquierda a unos 30 grados. Tras comprobar que el electrodo penetra de forma satisfactoria en el septo, se realizan nuevas mediciones hasta obtener el QRS estimulado más estrecho posible, con un umbral de estimulación siempre <2V a 0,4ms y con unas impedancias <1.100ohm.
Otros de los criterios utilizados para confirmar la estimulación en la rama izquierda han sido la transición de estimulación no selectiva a estimulación selectiva o de estimulación no selectiva a captura miocárdica durante el test de umbral. El acortamiento brusco del tiempo de activación en V6 (>10ms) durante la penetración en el septo con el tiempo de activación corto y constante (< 80ms) a salida alta (5V) y baja (1V). La estimulación programada mostrando PR (potencial de rama) en rama izquierda y en miocardio.
Se implantaron un total de 20 marcapasos bicamerales y 10 monocamerales. De los 30 pacientes analizados, el 40% fueron mujeres y el 60% varones.
La edad media fue de 74 años (63-86 años). La bradiarritmia más frecuente es el bloqueo auriculoventricular completo con bloqueo completo de la rama izquierda del haz de His seguida de la fibrilación auricular lenta con bloqueo completo de rama asociada y el bloqueo de Mobitz II.
Se han realizado 4 upgrade (nueva estimulación en rama izquierda y anulación del electrodo previo en ápex de ventrículo derecho) en pacientes que necesitaban cambio de generador por agotamiento de la batería y que presentaban signos clínicos y ecocardiográficos de insuficiencia cardiaca asociada a la estimulación previa.
La duración del procedimiento fue de 140±60 min, con media de 15,3 min de escopia. La media del QRS nativo fue de 146ms (120-178ms); la media del QRS estimulado fue de 116ms (97-130ms), con mejora de la anchura en la totalidad de los casos.
La media del tiempo de activación del ventrículo izquierdo fue de 78ms (60-95ms). La fracción de eyección del ventrículo izquierdo media previa al implante fue del 56% (37-69%), el control a los 3 meses fue del 61% (55-70%) y a los 6 meses del 62% (5-70%).
La media del umbral de estimulación del ventrículo derecho en el implante fue de 1V a 0,4ms (0,25-2V). En el control de los 3 meses la media descendió a 0,45V a 0,4ms (0,25-0,75V) y se mantuvo en los mismos parámetros en el control a los 9 meses.
La impedancia (monopolar ventrículo derecho) media tras el implante fue de 644ohm (371-900ohm) y en el control a los 3 meses bajó a 441ohm (300-721ohm) y aún más a los 9 meses: 420ohm (295-720ohm).
El umbral de detección del ventrículo derecho medio al finalizar el implante fue de 11mV (3,1-21mV). Este mejoró en el control de los 3 meses a 13,3mV (3-20mV) y se mantuvo en el control de los 9 meses.
No hubo complicaciones asociadas al implante del dispositivo. Un paciente necesitó cardioversión eléctrica tras implante debido a aleteo auricular.
Respecto a la tasa de éxito, se consiguió obtener una señal eléctrica de estimulación compatible con la rama izquierda tanto selectiva como no selectiva en la totalidad de nuestros implantes en rama izquierda, acortando la anchura del QRS.
Pese a que la estimulación hisiana es una de las técnicas más fisiológicas empleada hasta el momento, hay factores que limitan su uso de forma rutinaria. El éxito de un implante requiere una curva de aprendizaje larga hasta para implantadores considerados expertos, hay que asumir umbrales de captura altos durante el implante e incluso existe el riesgo de mantener umbrales altos en revisiones posteriores. Además, la estimulación hisiana puede no resultar exitosa en pacientes con bloqueos hisianos distales, o precisar umbrales inaceptablemente altos para corregir bloqueos de rama.
La estimulación de rama izquierda es una técnica novedosa, surgida ante la mayor evidencia de los efectos deletéreos que provoca en el corazón la estimulación apical sostenida del ventrículo derecho. A pesar de la falta de estudios que corroboren la seguridad y eficacia de esta técnica a largo plazo, en nuestra unidad se ha mostrado como un procedimiento seguro con buenos resultados tras 9 meses de seguimiento.
En este estudio observacional, la estimulación de rama izquierda se muestra como un procedimiento eficaz que consigue mejorar la función ventricular, seguro y reproducible, realizado por intensivistas, en un hospital comarcal. El bloqueo en la rama izquierda, a día de hoy, es una técnica de estimulación cardiaca en auge, más reproducible que la estimulación hisiana y con resultados prometedores.
Se ha corroborado la factibilidad y reproducibilidad de esta técnica y se han mostrado los buenos resultados del seguimiento durante los 9 primeros meses tras el implante.
FinanciaciónEste artículo no ha recibido financiación de ningún tipo.
Contribución de los autoresA. Carranza Pinel ha contribuido a la corrección y revisión del artículo y a su redacción. A. Fuentes Calatayud ha contribuido a la recogida de datos sistemática. A. López Fernández ha contribuido a la redacción del artículo. A. León Aranda ha contribuido a la recogida de datos sistemática en el seguimiento. L. Fernández Ruiz ha contribuido al seguimiento sistemático de los pacientes. I.M. Cruz Valero ha contribuido al diseño y análisis.
Conflicto de interesesNo hay conflicto de intereses.