El control de los factores de riesgo cardiovascular (FRCV) debe realizarse en atención primaria (AP), labor especialmente interesante en los pacientes con enfermedad cardiovascular (ECV) previa. Un seguimiento semestral, acorde a las recomendaciones de las guías de práctica clínica y coincidiendo con la administración de un fármaco inyectable, como es el caso de inclisirán, podría mejorar la eficiencia de la atención sanitaria. El estudio de continuidad asistencial entre cardiología y AP en el paciente con cardiopatía isquémica crónica (CAPRICI) plantea analizar si la implantación de un programa de seguimiento, con visitas semestrales paralelas a la administración de inclisirán en AP, a pacientes con cardiopatía isquémica crónica, permite optimizar el seguimiento y mejorar el control de los FRCV.
MétodosEl estudio CAPRICI es un estudio aleatorizado controlado, prospectivo y multicéntrico, en el que participarán cinco centros de salud (CS) del Área Sanitaria de Santiago de Compostela y Barbanza: A Estrada, Concepción Arenal, Ribeira, Melide y Milladoiro. Se incluirán pacientes con enfermedad coronaria crónica, asociada a otras enfermedades que incrementan el riesgo cardiovascular, con niveles elevados de colesterol unido a lipoproteínas de baja densidad (cLDL) (> 100mg/dl) a pesar del tratamiento convencional con estatinas de alta potencia, asociadas o no a ezetimiba. Se registrarán el número de visitas en los servicios sanitarios, así como el control de los FRCV y los hábitos de vida.
ConclusionesLos resultados de este estudio contribuirán a mejorar el conocimiento sobre la atención a los pacientes de muy alto riesgo cardiovascular, especialmente en la optimización del número de visitas y derivaciones al hospital, así como en el control de sus FRCV.
Identificador Clinicaltrials.gov: NCT06421363
The management of cardiovascular risk factors (CVRF) should be conducted in Primary Care, which is particularly crucial for patients with prior cardiovascular disease. A semi-annual follow-up, aligned with the guidelines of clinical practice and coinciding with the administration of an injectable drug like inclisiran, could enhance healthcare efficiency. The CAPRICI study aims to analyze whether the implementation of a follow-up program, with semi-annual visits parallel to the administration of inclisiran in Primary Care, in patients with chronic ischemic heart disease, allows for optimized follow-up and improved control of CVRF.
MethodsThe CAPRICI study is a randomized, controlled, prospective, multicenter trial involving 5 health centers in the Health Area of Santiago de Compostela and Barbanza: A Estrada, Concepción Arenal, Ribeira, Melide, and Milladoiro. The study will include patients with chronic coronary disease associated with other pathologies that increase cardiovascular risk, with elevated levels of low-density lipoprotein cholesterol (> 100 mg/dl) despite conventional treatment with high-potency statins, with or without ezetimibe. The number of visits to healthcare services, as well as the control of CVRF and lifestyle habits, will be recorded.
ConclusionsThe results of this study will contribute to improving the knowledge about the care of patients at very high cardiovascular risk, particularly in optimizing the number of visits and hospital referrals, as well as in the control of their CVRF.
Clinicaltrials.gov identifier: NCT06421363
El paciente con enfermedad cardiovascular (ECV) constituye uno de los grupos de especial interés en atención primaria (AP) dada su elevada prevalencia1 y su asociación con la mortalidad poblacional2. La historia natural de la ECV describe que el correcto control de los factores de riesgo cardiovascular (FRCV) está asociado a su desarrollo como a mejorar el pronóstico en los pacientes que ya tienen ECV instaurada3.
La labor del médico y enfermera de AP se basa en un control de salud integral periódico en el que, además de orientación sobre cambios en el estilo de vida, se lleve a cabo una evaluación global de salud más allá de la ECV que padece y que debe incluir al conjunto de las comorbilidades4. Por otro lado, en dichos controles se comprueban y corrigen factores de riesgo que han demostrado asociarse con la progresión de la enfermedad, actividades de conciliación de la medicación y se planifica el seguimiento tanto por enfermería como por su médico de AP.
Estas actividades de planificación de la continuidad asistencial, además de promover la estabilidad clínica del paciente, permiten organizar la demanda asistencial en el ámbito de la medicina de AP evitando actos sanitarios que no aporten valor, que condicionan una gran carga asistencial y promueven un gasto sanitario ineficiente.
La cardiopatía isquémica representa la ECV crónica más prevalente en Galicia y se han descrito programas de continuidad asistencial con el objetivo de resolver la demanda en el nivel asistencial adecuado, con programación de los actos sanitarios para su seguimiento y medida de indicadores de actividad que nos permitan identificar oportunidades de mejora. El proceso asistencial del paciente con enfermedad coronaria crónica debe garantizar una respuesta rápida de otros especialistas (en estos pacientes, de forma habitual, el cardiólogo) ante interconsultas por parte de los médicos de AP. En Galicia disponemos de una amplia evidencia del valor de las consultas electrónicas como medio de comunicación entre profesionales sanitarios, reducen la demora en la atención, promueven la accesibilidad a la atención sanitaria, mejoran los resultados en salud y reducen los costes sanitarios5,6.
Inclisirán es un inhibidor de la síntesis de proproteína convertasa subtilisina/kexina tipo 9 (PCSK9) que actúa mediante tecnología de ácido ribonucleico de interferencia para reducir la producción de PCSK9 en el hígado. Al disminuir los niveles de PCSK9, inclisirán aumenta la cantidad de receptores de lipoproteínas de baja densidad (LDL) en la superficie de las células hepáticas, mejorando la eliminación del colesterol unido a lipoproteínas de baja densidad (cLDL) de la sangre y reduciendo significativamente sus niveles. Este fármaco se administra de forma semestral tras una dosis inicial y otra a los tres meses, facilitando el seguimiento clínico y mejorando la adherencia al tratamiento. Los principales efectos secundarios incluyen reacciones en el sitio de inyección, fatiga, dolor de cabeza y síntomas similares a los de un resfriado, así como raras reacciones alérgicas y elevaciones leves de enzimas hepáticas7.
La introducción de inclisirán en la práctica clínica podría ayudar a organizar la continuidad asistencial de los pacientes con ECV crónica, entre los que se encuentran los pacientes tras hospitalización por un síndrome coronario agudo. Su administración semestral, después de una segunda dosis a los tres meses de la primera, podría mejorar el control de uno de los principales determinantes de la progresión de la enfermedad en pacientes con colesterol elevado8 y facilitaría programar su seguimiento integral de salud por parte de su enfermería y médico de AP, que además de evitar actos sanitarios que no aportan valor, mejora su pronóstico y reduce los costes sanitarios.
Este estudio, denominado continuidad asistencial entre cardiología y AP en el paciente con cardiopatía isquémica crónica (CAPRICI), tiene como objetivo principal evaluar la efectividad de un programa de seguimiento que incorpore el tratamiento con inclisirán en pacientes con síndrome coronario crónico. Los objetivos específicos incluyen reducir las consultas no programadas, mejorar el control de los FRCV y evaluar la eficiencia coste-beneficio del tratamiento y seguimiento en la práctica clínica.
MétodosDiseño del estudioEl estudio CAPRICI es un estudio aleatorizado controlado, prospectivo, multicéntrico y de intervención en pacientes con diagnóstico previo de enfermedad coronaria crónica y muy alto riesgo cardiovascular. Es un estudio de carácter multidisciplinar y de ámbito entre niveles asistenciales. Se seleccionarán pacientes de 5 centros de salud (CS) (A Estrada, Concepción Arenal, Ribeira, Melide y Milladoiro) del Área Sanitaria de Santiago de Compostela (SERGAS). Se elegirán un total de 210 pacientes, unos 42 por centro. La selección del estudio será competitiva y se prevé que finalice en mayo de 2025. La población objetivo del estudio son los sujetos con enfermedad coronaria crónica y con médico de familia asignado en uno de los CS participantes.
Definición de la población objetivoEl estudio CAPRICI se centrará en pacientes con muy alto riesgo cardiovascular, definidos como aquellos con enfermedad coronaria crónica y niveles de cLDL >100mg/dL a pesar del tratamiento con estatinas de alta potencia o ezetimiba. Estos pacientes también presentarán al menos una de las siguientes condiciones: diabetes mellitus tipo 2, hipercolesterolemia familiar, enfermedad coronaria recurrente o enfermedad renal crónica según los criterios KDIGO (Kidney Disease: Improving Global Outcomes)9. Esta definición se alinea con las guías de práctica clínica que identifican a estos individuos como de muy alto riesgo debido a su alta probabilidad de eventos cardiovasculares adversos, lo que justifica un seguimiento más intensivo y un control estricto de los factores de riesgo.
Criterios de selecciónLos criterios de inclusión fueron: edad ≥ 18 años; diagnóstico previo de enfermedad coronaria crónica; valores de cLDL >100mg/dl en los 6 meses previos; al menos una de las siguientes enfermedades: a) diabetes mellitus tipo 2; b) hipercolesterolemia familiar; c) enfermedad coronaria recurrente y d) enfermedad renal crónica definida según criterios KDIGO; estar en tratamiento estable en dosis máximas de estatinas (atorvastina 80mg, rosuvastatina 40 o rosuvastatina 20mg, asociadas o no a ezetimibe). Son aceptables pacientes con otras estatinas o dosis inferiores si se ha evidenciado intolerancia clínicamente documentada.
Por otro lado, se consideraron criterios de exclusión los siguientes: pacientes sin estatinas; tratamiento concomitante con iPCSK9; embarazo, lactancia o deseo gestacional por parte de la paciente; pacientes que, a juicio del investigador, no puedan realizar un seguimiento adecuado en el programa de crónicos en la práctica clínica habitual.
Objetivos del estudioEl objetivo principal fue evaluar la eficacia del programa de seguimiento con inclisirán en mejorar la gestión clínica de los pacientes con cardiopatía isquémica crónica. Se focalizó el estudio en: a) reducción de las consultas no programadas y emergencias, tanto en AP como hospitalaria; b) mejora en el control de los FRCV, incluyendo actividad física, dieta, perfiles lipídico y glucémico, presión arterial y función renal; c) disminución de los costes económicos directos asociados al tratamiento de estos pacientes.
Los objetivos secundarios fueron los siguientes: a) determinar la adherencia de los pacientes al tratamiento farmacológico prescrito y su impacto en la salud a largo plazo; b) identificar factores predictivos de alta demanda asistencial y urgencias en esta población y c) investigar las principales causas de hospitalizaciones y mortalidad entre los participantes, proporcionando datos para futuras mejoras en las políticas de salud pública y práctica clínica.
Proceso de inclusión y selección de gruposLos pacientes que cumplan todos los criterios de inclusión y ninguno de exclusión, tras firmar el consentimiento informado, serán incluidos en el seguimiento protocolizado, constituyendo la rama de intervención si aceptan seguir el tratamiento con inclisirán, o la rama de control en centros participantes si no aceptan el tratamiento. Este proceso se denomina «asignación no aleatorizada basada en preferencias», ya que los pacientes son asignados a los grupos de intervención o control en función de su elección.
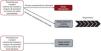
El grupo de control de práctica clínica habitual se obtendrá mediante una «asignación aleatorizada por centro» utilizando un proceso informático que incluye a pacientes que cumplen los mismos criterios en otros centros de atención sanitaria. Las variables serán registradas en una base de datos a partir de la historia clínica electrónica y almacenadas mediante codificación (fig. 1).
SeguimientoLos pacientes seleccionados en los CS participantes, de cualquiera de las dos ramas, serán seguidos durante al menos 27 meses, según el protocolo detallado en la tabla 1, con visitas a los tres meses tras la primera de ellas y cada seis meses, posteriormente, coincidiendo con la administración del fármaco.
Procedimientos
| Tiempo | Visita | Consentimiento informado | Criterios | Historial médico | Hábitos de vida | Exploración física | Pruebas de laboratorio | ECG | Administración de inclisirán | Cambios medicación | Seguimiento de eventos adversos | Variables objetivo |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0 | V0 | X | X | X | X | X | X | X | ||||
| 3 meses | V1 | X | X | X | X | X | X | X | ||||
| 9 meses | V2 | X | X | X | X | X | X | X | ||||
| 15 meses | V3 | X | X | X | X | X | X | X | X | |||
| 21 meses | V4 | X | X | X | X | X | X | X | ||||
| 27 meses | V5 | X | X | X | X | X | X | X | X |
Detalles adicionales:
• Hábitos de vida: evaluación continua de actividad física, tabaco y alcohol en cada visita programada.
• Exploración física: incluye la talla, peso, perímetro abdominal y presión arterial, evaluados en todas las visitas desde V1 en adelante.
Pruebas de laboratorio: incluyen glucemia, HbA1c (si DM), colesterol total, HDL-colesterol, colesterol unido a lipoproteínas de baja densidad, triglicéridos, FGe (CKD-EPI), cociente alb/crea, GOT, GPT, GGT, fosfatasa alcalina y CK, evaluados en la visita inicial y en cada control subsecuente.
CK: creatina cinasa; DM: diabetes mellitus; ECG: electrocardiograma; FGe (CKD-EPI): filtrado glomerular estimado (Chronic Kidney Disease Epidemiology Collaboration); cociente alb/crea: cociente albúmina/creatinina; GOT: glutamato-oxaloacetato transaminasa; GPT: glutamato-piruvato transaminasa; GGT: gamma-glutamil transferasa; HbA1c: hemoglobina glucosilada; V0: visita basal; V1: visita 1; V2: visita 2; V3: visita 3; V4: visita 4; V5: visita 5.
Los pacientes control o de práctica clínica habitual se obtendrán desde la historia clínica electrónica, según los mismos criterios de inclusión y exclusión, registrando las variables necesarias descritas en este mismo protocolo en cada visita de seguimiento (tabla 2).
Delegación de tareas
| Tiempo de seguimiento | Visita | Tareas del médico | Tareas de la enfermera |
|---|---|---|---|
| 0 | V0 | Consentimiento, criterios de inclusión/exclusión, historial médico, pruebas de laboratorio | Administración de inclisirán |
| 3 meses | V1 | Pruebas de laboratorio, seguimiento de eventos adversos | Hábitos de vida, exploración física, administración de inclisirán |
| 9 meses | V2 | Pruebas de laboratorio, seguimiento de eventos adversos | Hábitos de vida, exploración física, administración de inclisirán |
| 15 meses | V3 | Pruebas de laboratorio, seguimiento de eventos adversos | Hábitos de vida, exploración física, administración de inclisirán |
| 21 meses | V4 | Pruebas de laboratorio, seguimiento de eventos adversos | Hábitos de vida, exploración física, administración de inclisirán |
| 27 meses | V5 | Pruebas de laboratorio, seguimiento de eventos adversos | Hábitos de vida, exploración física, administración de inclisirán |
V0: visita basal; V1: visita 1; V2: visita 2; V3: visita 3; V4: visita 4; V5: visita 5.
La base de datos será electrónica y anonimizada. El promotor del estudio será el responsable de la validez y custodia de los datos. Los investigadores de cada centro serán responsables de incluir a los pacientes y recoger las diferentes variables a través de la historia clínica.
El estudio ha sido registrado en ClinicalTrials.gov (NTC462728289) y ha sido aprobado por el Comité de Ética de la investigación con medicamentos de Galicia (CEIm-G) con número de registro 2024/041.
Variables del estudioVariables de resultado principal- a)
Actividad asistencial: número de consultas no programadas en enfermería de AP, número de consultas no programadas en medicina de familia de AP, número de asistencias en puntos de atención continuada de AP, número de consultas hospitalarias telemáticas, número de consultas hospitalarias presenciales y número de asistencias en urgencias hospitalarias.
- b)
Control de factores de riesgo: actividad física, adherencia a la dieta mediterránea, niveles de cLDL, presión arterial, glucemia, hemoglobina glucosilada (HbA1c) (si tiene diagnóstico previo de diabetes mellitus), filtrado glomerular estimado (Chronic Kidney Disease Epidemiology Collaboration [CKD-EPI]) y cociente albúmina-creatinina.
- c)
Costes asociados: análisis de los costos asociados a las variables anteriores.
- a)
Adherencia a la medicación.
- b)
Pronóstico del paciente, incluyendo ingresos hospitalarios y mortalidad.
Para más detalles sobre cómo se registrarán las variables, consulte el anexo (material adicional).
Recogida de datos sobre programas de rehabilitación cardiacaPara abordar de manera integral el tratamiento de los pacientes con cardiopatía isquémica crónica y evitar posibles sesgos de confusión, se incluirá la recogida de datos relacionados con la participación en programas de rehabilitación cardiaca. Los programas de rehabilitación cardiaca, bien diseñados y coordinados con AP, han demostrado beneficios significativos en la morbimortalidad de estos pacientes10.
Las variables relacionadas con los programas de rehabilitación cardiaca que se recogerán incluyen: a) participación en programas de rehabilitación cardiaca: registro de si el paciente está inscrito en un programa de rehabilitación cardiaca; b) frecuencia y duración de la rehabilitación: número de sesiones semanales y duración total del programa; c) adherencia al programa: evaluación de la adherencia del paciente a las sesiones de rehabilitación prescritas; d) componentes del programa: descripción de los componentes específicos del programa, tales como ejercicio físico, educación sobre estilos de vida, y apoyo psicológico; e) resultados de la rehabilitación: mejoras en la capacidad funcional, parámetros de ejercicio y reducción de síntomas.
Estas variables se registrarán en la base de datos del estudio y se analizarán para determinar su impacto en los resultados clínicos y en la eficacia del protocolo de seguimiento propuesto.
Cálculo del tamaño muestralPara asegurar un poder estadístico adecuado en nuestro estudio, se estima el tamaño de muestra necesario para detectar una mejora significativa del 25% en el grupo de intervención comparado con los grupos de control. Basándonos en la proporción esperada de mejora del 50% en los grupos de control y del 75% en el grupo de intervención, se estableció un nivel de significancia del 5% y un poder del estudio del 80%. Dado que el diseño del estudio involucra 3 grupos (grupo de intervención, grupo control en centros participantes y grupo control aleatorizado), se ajustó el tamaño de muestra para mantener el poder estadístico en comparaciones múltiples. Se calculó que cada grupo necesitaría aproximadamente 70 participantes, totalizando 210 sujetos para los 3 grupos. Este tamaño de muestra está diseñado para permitir la detección de diferencias estadísticamente significativas entre los grupos, asumiendo una mínima pérdida de seguimiento y una consistencia en la variabilidad de los datos observados.
Análisis estadísticoEn el análisis estadístico descriptivo de las variables se utilizarán distintos parámetros: media, desviación estándar (DE), mediana, rango intercuartílico (IQR) y cálculo de proporciones.
El análisis de la variable principal se realizará mediante la prueba de la t de Student para muestras pareadas o sus homólogos tests no paramétricos cuando los datos no sigan una distribución normal (U de Mann-Whitney o Kruskall-Wallis). Las variables cualitativas se contrastarán mediante pruebas de la χ2. Para el análisis de costes se incluirán aquellos de consulta y teleconsulta, costes de viaje y del tiempo invertido por el paciente en el desplazamiento al hospital y el coste del tiempo en la lista de espera.
El análisis de las variables secundarias de adherencia a la medicación se calculará mediante la proporción de días cubiertos, según los cálculos descritos en el anexo (material adicional); y para las variables de ingresos y mortalidad se utilizarán curvas de supervivencia de Kaplan-Meier y se estimará un modelo de Cox de riesgos proporcionales ajustados por edad y sexo.
Todos los resultados se presentan con la media y el intervalo de confianza al 95% (IC 95%) y se expondrán con dos decimales, aunque durante el cálculo no se redondeará en ningún caso. Se considerará estadísticamente significativo un valor de p inferior a 0,05. Para el procesamiento y análisis de los datos se utilizará el paquete estadístico SPSS 22.0 para Windows (IBM Corporation, Armonk, Estados Unidos).
DiscusiónEl estudio CAPRICI pretende analizar si protocolizar el seguimiento de los pacientes con enfermedad coronaria, subsidiarios de ser tratados con inclisirán, con la periodicidad de la administración del fármaco, tiene impacto en la reducción de visitas médicas y enfermería además de reducir gastos y tener resultados favorables en el control de los FRCV, así como de ingresos y mortalidad.
El beneficio en el control de cLDL, así como de la lipoproteína (a) (Lp[a]) en pacientes de alto riesgo cardiovascular es bien conocido a partir de los ensayos pivotales del fármaco11–13, y su posible efecto beneficioso en la reducción del riesgo cardiovascular. Sin embargo, es importante destacar que la mayor parte de la Lp(a) presente en el organismo viene determinada genéticamente y varía muy poco con los cambios en la dieta y la mayoría de los tratamientos farmacológicos. La Lp(a) es una lipoproteína similar a la LDL, compuesta por una apolipoproteína B-100 y una apolipoproteína (a), y sus niveles son altamente heredables. Los tratamientos hipolipemiantes convencionales, como las estatinas, no afectan significativamente los niveles de Lp(a). Sin embargo, los inhibidores de PCSK9 y otros tratamientos emergentes han demostrado cierto potencial en su reducción14. En el estudio CAPRICI, se realizará la determinación de los niveles de Lp(a) en los pacientes tratados con inclisirán para evaluar su efecto en la reducción de esta lipoproteína, además de su acción sobre el cLDL. Los pacientes con niveles elevados de Lp(a) tienen un riesgo cardiovascular aumentado, independientemente de los niveles de cLDL. Aunque el control de este último es esencial, los niveles elevados de Lp(a) representan un riesgo residual significativo. Por lo tanto, incluso en pacientes con niveles bajos de LDL controlados por fármacos, la presencia de Lp(a) elevada sigue siendo un factor de riesgo importante que requiere atención y tratamiento15.
Por otro lado, las guías de práctica clínica nos recomiendan un seguimiento semestral de los FRCV mayores, especialmente presión arterial, glucemia y cLDL, que deben tener un control estricto para reducir el riesgo cardiovascular de los pacientes4,16.
El marco financiador actual de nuestro servicio público de salud permite la financiación de inclisirán en pacientes con ECV o hipercolesterolemia familiar a tratamiento con estatinas de alta potencia que no reducen los niveles de cLDL por debajo de 100mg/dl. Nuestro trabajo centra el análisis en un grupo de pacientes con mayor riesgo cardiovascular combinando a la ECV con otra enfermedad como la diabetes mellitus, enfermedad renal o hipercolesterolemia familia, o bien que presente eventos coronarios recurrentes4,16. Además, el inclisirán ofrece una pauta de administración semanal más cómoda para el paciente y que permite implementar paralelamente un seguimiento protocolizado adaptado a las recomendaciones de las guías de práctica clínica17,18.
Proponemos un protocolo de seguimiento que evaluará el control de los FRCV, así como los hábitos de vida y la adherencia al tratamiento. Este enfoque permitirá determinar si dicho seguimiento puede reducir las visitas de los pacientes tanto en AP como en consultas hospitalarias, mejorando así el control de estos factores. Esta estrategia permitirá comprobar la hipótesis de que un correcto seguimiento de los pacientes, basado en la pauta de tratamiento semestral, facilita una estrategia más eficiente y reordenar el seguimiento de los pacientes crónicos.
La pandemia de COVID-19 alteró y rompió de forma importante la «continuidad asistencial» de los pacientes con enfermedades crónicas, especialmente agravada por la sobrecarga asistencial que se ha experimentado en los años posteriores19–21. Como consecuencia, se ha observado un incremento de la mortalidad general durante los años siguientes a la pandemia, asociado además al retraso en la atención sanitaria. Este retraso afectó especialmente las interconsultas realizadas desde AP a atención especializada, lo que significa que los pacientes que requerían una evaluación o intervención especializada no recibieron la atención necesaria de manera oportuna22,23. La pérdida de la continuidad asistencial en pacientes con ECV se asocia a un incremento de su riesgo de muerte, hospitalización por complicaciones relacionadas con su enfermedad coronaria y otras comorbilidades asociadas22,23, incremento de visitas a urgencias y otras visitas sanitarias no programadas, así como un aumento del gasto sanitario. Por tanto, es necesario desarrollar programas de organización de los procesos asistenciales más prevalentes con la enfermería y medicina de AP en el centro que nos permitan recuperar la «continuidad asistencial»24,25.
Los modelos asistenciales basados en la atención protocolizada a los pacientes han mostrado mejor comprensión de su enfermedad por parte de estos e incrementar el grado de control de los FRCV26. Esta atención protocolizada a los pacientes, además de ser una buena estrategia para evitar la inercia terapéutica de los profesionales, puede ser una estrategia adecuada para reducir la falta de adherencia al tratamiento por parte de los pacientes polimedicados como los que serán reclutados en el presente estudio27. La inercia terapéutica se refiere a la tendencia de los profesionales de la salud a no iniciar o intensificar el tratamiento cuando está clínicamente indicado, lo cual puede resultar en un control subóptimo de los FRCV y en peores resultados de salud para los pacientes. Por último, otra ventaja de la atención protocolizada es que puede ayudar a evitar la variabilidad en la atención a los pacientes complejos, en los que existen recomendaciones claras con alto nivel de evidencia con impacto pronóstico favorable desde el punto de vista cardiovascular28.
Las implicaciones prácticas de estos hallazgos son significativas. La implementación de un seguimiento protocolizado tiene el potencial de mejorar significativamente el control de los FRCV en pacientes de muy alto riesgo cardiovascular. Al reducir las visitas no programadas y optimizar el tratamiento de estos pacientes, se pueden lograr mejoras sustanciales en la eficiencia del sistema de salud. Además, la adherencia al tratamiento, que suele ser un desafío en pacientes polimedicados, podría mejorar al establecer un protocolo claro y consistente de seguimiento.
Las direcciones futuras para la investigación incluyen la evaluación a largo plazo de los pacientes tratados con inclisirán para comprender mejor su impacto en la reducción de eventos cardiovasculares mayores y la mortalidad. Además, la exploración de combinaciones terapéuticas que aborden múltiples FRCV simultáneamente podría ofrecer estrategias más robustas para el tratamiento de los pacientes con riesgo cardiovascular elevado. También sería valioso investigar la aplicación de este protocolo en diferentes contextos sanitarios para evaluar su generalizabilidad y adaptabilidad.
ConclusionesEl protocolo propuesto tiene el potencial de mejorar el seguimiento de los pacientes de muy alto riesgo cardiovascular en un contexto de sobrecarga asistencial. La implementación de este protocolo puede reducir las visitas no programadas, optimizar el control de los FRCV y disminuir tanto los ingresos hospitalarios como la mortalidad.
- •
La ECV es una de las principales causas de morbimortalidad a nivel mundial.
- •
El control de los FRCV es crucial para prevenir la progresión de la ECV.
- •
La AP desempeña un papel esencial en el seguimiento y tratamiento de pacientes con ECV crónica.
- •
Inclisirán, un inhibidor de PCSK9, ha demostrado ser efectivo en la reducción de los niveles de colesterol LDL, mejorando el control lipídico en pacientes con alto riesgo cardiovascular.
- •
El estudio CAPRICI evalúa la eficacia de un programa de seguimiento semestral en AP con administración de inclisirán en pacientes con cardiopatía isquémica crónica.
- •
Se propone un modelo de continuidad asistencial entre cardiología y AP, optimizando el control de FRCV y reduciendo las visitas no programadas y emergencias.
- •
La implementación de este protocolo podría mejorar la adherencia y reducir los costos asociados al tratamiento de estos pacientes.
- •
Los resultados de este estudio contribuirán a la optimización de la atención a pacientes con muy alto riesgo cardiovascular, facilitando un enfoque más eficiente y personalizado en su seguimiento.
Este estudio no ha recibido ninguna fuente específica de financiación de agencias del sector público, sector comercial o entidades sin ánimo de lucro. Todos los recursos necesarios para llevar a cabo este estudio han sido proporcionados por los centros participantes y los investigadores involucrados.
Consideraciones éticasEl estudio ha sido registrado en ClinicalTrials.gov (NTC462728289), ha sido aprobado por el Comité de ética de la investigación con medicamentos de Galicia (CEIm-G) y autorizado por la gerencia del área sanitaria.
Se han tenido en cuenta las posibles variables de sexo y género de acuerdo con las directrices SAGER (Sex and Gender Equity in Research Guidelines).
Este estudio cumple con las directrices establecidas por la declaración Strengthening the Reporting of Observational Studies in Epidemiology (STROBE).
Declaración sobre el uso de inteligencia artificialSe declara que en la elaboración del presente manuscrito no se ha utilizado ninguna herramienta de inteligencia artificial o automatizada para generar, editar o revisar el contenido. Todo el trabajo presentado ha sido realizado manualmente por los autores.
Contribución de los autoresS. Cinza-Sanjurjo participó en el diseño del estudio, la redacción del manuscrito y el desarrollo del cálculo del tamaño muestral y análisis estadístico. J. Seijas-Amigo estuvo a cargo de la redacción del manuscrito y el desarrollo del cálculo del tamaño muestral, así como el análisis estadístico. B. Fontela-Sánchez contribuyó en la redacción de secciones específicas del manuscrito. D. Rey-Aldana se encargó del análisis estadístico y la revisión crítica del manuscrito. P. Sempere-Serrano participó en el diseño del protocolo de investigación, la supervisión del estudio y la redacción del manuscrito. P. Mazón-Ramos realizó la revisión bibliográfica y la redacción de secciones del manuscrito. D.G. Mosteiro-Miguéns contribuyó en el diseño del estudio. M. Portela-Romero estuvo involucrado en la coordinación del estudio. N. Sánchez-Varela supervisó el estudio y redactó críticamente el manuscrito. F. Reyes-Santias participó en la redacción del manuscrito. M.T. Ferreiro-Serrano contribuyó en el diseño del estudio. M. Barral-Carregal estuvo involucrada en el diseño del estudio y la revisión crítica del manuscrito. A. Grela-Beiroa participó en la coordinación del estudio. A. Suárez-Dios estuvo a cargo de la revisión crítica del manuscrito. I. Rego-Lijó contribuyó en el diseño del estudio. J.R. González-Juanatey supervisó el estudio en general y revisó críticamente el manuscrito. Todos los autores han leído y aprobado la versión final del manuscrito.
El autor de correspondencia garantiza que todos los autores cumplen con cada una de las características definidas por el International Committee of Medical Journal Editors en los criterios de autoría de los artículos científicos: contribuciones sustanciales al diseño del trabajo o la adquisición, análisis o interpretación de datos; redacción o revisión crítica del contenido intelectual; aprobación final de la versión que se publicará; y acuerdo para asumir responsabilidades sobre todos los aspectos del trabajo y resolver cualquier cuestión relacionada con su precisión e integridad.
Conflicto de interesesNinguno.
Los investigadores recibieron el apoyo de la Fundación Instituto de Investigación Sanitaria de Santiago de Compostela (FIDIS) y de la Red Nacional de Investigación Biomédica en Enfermedades Cardiovasculares (Centro de Investigación Biomédica en Red de Enfermedades Cardiovasculares [CIBERCV]).