Novedades en cardiología: visión del cardiólogo joven
Más datosLa IV edición del Congreso de los Jóvenes Cardiólogos, el CardioMIR, se celebró en Madrid durante los días 22 y 23 de septiembre de 2023, congregando alrededor de 550 jóvenes cardiólogos con el fin de conocer las últimas novedades en el abordaje diagnóstico y terapéutico de la enfermedad cardiovascular. El congreso pretende, además, ser un punto de encuentro de los jóvenes cardiólogos de la Sociedad Española de Cardiología, especialmente residentes, donde compartir experiencias e inquietudes. El objetivo del presente artículo es resumir los principales temas abordados en la IV edición del CardioMIR.
The IV edition of the Congress of Young Cardiologists, CardioMIR, was held in the city of Madrid on September 22 and 23, 2023, bringing together around 550 young cardiologists to learn about the latest developments in the diagnostic approach and therapeutics of cardiovascular disease. The congress also aims to be a meeting point for young cardiologists from the Spanish Society of Cardiology, especially residents, where they can share experiences and concerns. The aim of this article is to summarize of the main topics addressed in the IV edition of CardioMIR.
Uno de los principales objetivos del Grupo de Jóvenes Cardiólogos de la Sociedad Española de Cardiología es promover la formación continuada de sus miembros1. Con ese fin nació en el año 2020 CardioMIR, el Congreso de los Jóvenes Cardiólogos, donde se abordan, desde un punto de vista eminentemente práctico, los aspectos más relevantes y novedosos de la cardiología. Los temas seleccionados pretenden complementar la formación recibida durante la etapa MIR2 e intenta hacer partícipes y protagonistas a todos sus asistentes (residentes, jóvenes cardiólogos y expertos). Tras 3 ediciones marcadas por el éxito de asistencia (más de 500 asistentes en la III edición entre la modalidad presencial y virtual3), la IV edición del CardioMIR no se quedó atrás y cumplió con las expectativas. Celebrado en Madrid, congregó durante los días 22 y 23 de septiembre a más de 550 entusiastas de la cardiología, la mayoría residentes, en un formato dual (presencial y virtual). De esta forma, el CardioMIR, se ha convertido en un referente nacional en la formación en enfermedad cardiovascular (CV). El objetivo del presente artículo es resumir los principales temas abordados en la IV edición del CardioMIR.
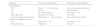
Actualización en prevención cardiovascularOptimización del tratamiento médico en mi paciente con diabetes mellitus tipo 2El tratamiento de la diabetes mellitus tipo 2 (DM2) ha experimentado un importante desarrollo en la última década, principalmente debido a la aparición de 2 nuevas familias de antidiabéticos: los agonistas del péptido similar al glucagón tipo 1 (aGLP-1) y los inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2). Estos fármacos no solo han demostrado mejorar el control glucémico, sino que también ofrecen beneficios adicionales: disminución de la mortalidad CV, disminución de eventos isquémicos e insuficiencia cardiaca (IC), protección renal, y reducción de peso4 (fig. 1 y fig. 2). La combinación de aGLP-1 e iSGLT2 ofrece un enfoque terapéutico sinérgico para los pacientes con DM2, sin incrementar el riesgo de hipoglucemia. Dado su beneficio desde el punto de vista CV, las nuevas guías de práctica clínica5 los sitúan como primera opción terapéutica en los pacientes con DM2 y alto riesgo CV.
Dado el impacto de la asociación de la DM2 y la enfermedad renal crónica (ERC), se deben buscar opciones terapéuticas que no solo no deterioren la función renal, sino que la protejan6. Múltiples estudios han demostrado el beneficio del uso de la finerenona en este contexto7. Actuando como un antagonista no esteroidal selectivo del receptor de mineralocorticoides, ha demostrado beneficios en términos de nefro y cardioprotección, reduciendo tanto la inflamación como la fibrosis y la albuminuria en los pacientes con DM2 y ERC.
El cardiólogo ante la obesidad; una visión prácticaLa obesidad es una pandemia global que trasciende al simple exceso de peso. Su complejidad radica en el aumento de la grasa visceral y epicárdica, así como en la inflamación sistémica. Estas alteraciones están estrechamente relacionadas con el desarrollo de enfermedades CV8. Por ello, los cardiólogos ocupan un lugar esencial en la lucha contra esta problemática, en el que el tratamiento de la obesidad no se limite solo a la pérdida de peso.
Desde el punto de vista nutricional, la dieta mediterránea destaca por sus beneficios en la salud CV. Los estudios PREDIMED9 y CORDIOPREV10 demostraron una reducción del riesgo de eventos CV en individuos que adoptaron esta dieta en comparación con una dieta baja en grasas tanto en prevención primaria como secundaria, respectivamente.
El ejercicio físico, tanto aeróbico como de fuerza, es otro pilar fundamental en el tratamiento y en la prevención de la obesidad y sus complicaciones. Aunque las guías clínicas recomiendan entre 150 y 300 min semanales de ejercicio aeróbico moderado11, un enfoque más personalizado está ganando terreno: la optimización metabólica. Esta perspectiva busca mejorar tanto la cantidad como la calidad del ejercicio, adaptando la intensidad y el tipo de actividad a las necesidades individuales y a las respuestas metabólicas del cuerpo. Mediante la ergoespirometría y las pruebas de lactato, es posible determinar el punto de donde se maximiza la quema de grasa. Realizar ejercicio físico alrededor de este punto no solo potenciaría la quema de grasa, sino que también mejoraría la eficiencia mitocondrial, fundamental para la salud metabólica y CV ofreciendo resultados más efectivos en los pacientes con obesidad, a medio y largo plazo12.
Finalmente, en el ámbito farmacológico, los análogos del GLP1, como semaglutida, liraglutida y dulaglutida, así como futuros medicamentos como cagrilintida-semaglutida y análogos duales (tirzepatida) y triples (retatrutida), están revolucionando el tratamiento de la obesidad. Estos fármacos no solo son efectivos en la reducción de peso, sino que también ofrecen beneficios en el pronóstico CV, regulación lipídica, disminución de la inflamación sistémica y mejora de la clase funcional13–15.
Valoración del riesgo residualEl riesgo CV residual se refiere a la probabilidad de sufrir eventos CV incluso después de haber alcanzado los objetivos terapéuticos recomendados por las guías de práctica clínica. Estos objetivos abordan aspectos como el control de la tensión arterial, el abandono del tabaquismo, la regulación adecuada del metabolismo lipídico y del metabolismo hidrocarbonado y la adopción de un estilo de vida saludable11.
Un aspecto de particular importancia es el riesgo CV lipídico residual, más allá del colesterol unido a las lipoproteínas de baja densidad (LDL)16. Es esencial evaluar las diferentes lipoproteínas y su relación con la adiposidad y los triglicéridos. Las lipoproteínas pequeñas y densas poseen una elevada capacidad aterogénica, lo que implica que pueden contribuir de manera significativa a la ateroesclerosis y, en consecuencia, incrementar el riesgo de eventos CV17. Por ello, es importante no centrarse exclusivamente en el LDL. En su lugar, se deben considerar otros marcadores, como el colesterol no unido a lipoproteínas de alta densidad (HDL) o la determinación de ApoB, que brindan una perspectiva más amplia sobre la estratificación del riesgo ateroesclerótico de un individuo. Los cocientes lipoproteicos, como el cociente LDL/apolipoproteínaB (ApoB) o triglicéridos (TG)/HDL, son también indicativos de este riesgo residual siendo patológicos un cociente LDL/ApoB inferior a 1,3 o un cociente TG/HDL superior a 2, sugiriendo la presencia de lipoproteínas pequeñas y densas.
Finalmente, es relevante mencionar la lipoproteína (a), o Lp(a), que ha sido identificada como un factor de riesgo independiente para la enfermedad CV, y debe solicitarse en nuestros pacientes al menos una vez en la vida. Aunque aún no es modificable, su evaluación proporciona información valiosa sobre el riesgo CV residual de un individuo11.
Actualización en imagen cardiacaTrucos de ecocardiografía en el paciente agudo cardiológicoLa ecocardiografía constituye una herramienta fundamental en el diagnóstico y la monitorización de los pacientes cardiológicos agudos, habiendo demostrado modificar las decisiones de manejo en un elevado porcentaje de pacientes18.
Uno de los principales escenarios críticos en los que la ecocardiografía es de gran utilidad es el shock de causa no filiada. El protocolo Rapid ultrasound for shock and hypotension (RUSH)19 propone realizar una aproximación práctica de las causas del shock centrada en la valoración de la «bomba», el «depósito» y las «cañerías» (tabla 1). Asimismo, la ecocardiografía desempeña un papel central en los pacientes con dispositivos de soporte circulatorio mecánico20, tanto en la selección de los pacientes como en su implante, seguimiento y destete (tabla 2).
Evaluación diagnóstica inicial del shock y la hipotensión mediante ultrasonidos. Protocolo RUSH
| Bomba (pump) | Depósito (tank) | Cañerías (pipes) |
|---|---|---|
| • Ventrículo izquierdo: FEVI, ITVTSVI, alteraciones segmentarias de la contracción• Ventrículo derecho: TAPSE, onda s’, dimensiones• Pericardio: derrame, signos indirectos de taponamiento o constricción | • Vena cava inferior: diámetro• Venas femorales y poplíteas: detección de trombosis venosa profunda• Pleura: derrame, neumotórax• Abdomen: ascitis | • Aorta: aneurisma, disección |
FEVI: fracción de eyección del ventrículo izquierdo; ITVTSVI: integral tiempo velocidad del tracto de salida del ventrículo izquierdo; RUSH: Rapid ultrasound for shock and hypotension; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo.
Escenarios clínicos de la ecocardiografía en el paciente con oxigenación con membrana extracorpórea venoarterial
| Antes del implante | Durante el implante y evolución | Destete |
|---|---|---|
| • Valoración de la FEVI• Detección de la presencia de IAo e IM• Potenciales contraindicaciones/precauciones: disección aórtica, trombo intraventricular, taponamiento cardiaco, comunicación interventricular | • Posicionamiento de las cánulas• Descarga de VI: DTDVI, posición del SIV, ecocontraste espontáneo, apertura de la válvula aórtica, empeoramiento de la IAo o IM• Valoración de la volemia• Detección de complicaciones: derrame pericárdico, trombosis | • Valoración del VI: ITVTSVI, FEVI• Valoración del VD: TAPSE, s’, diámetro basal, posición del SIV• Valoración de las válvulas aórtica y mitral: apertura de la válvula aortica, onda s lateral |
DTDVI: diámetro telediastólico del ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo; IAo: insuficiencia aórtica; IM: insuficiencia mitral; ITVTSVI: integral tiempo velocidad del tracto de salida del ventrículo izquierdo; SIV: septo interventricular; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo; VD: ventrículo derecho; VI: ventrículo izquierdo.
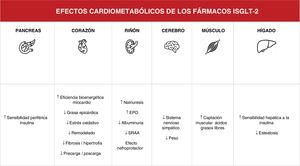
Además de la ecocardiografía, la ecografía pulmonar (lung ultrasound [LUS]) permite realizar el diagnóstico diferencial entre el síndrome de distrés respiratorio, el edema pulmonar y otras causas de insuficiencia respiratoria20. Por otro lado, la evaluación de la congestión venosa mediante ecografía (venous excess ultrasound grading system [VExUS]) apoya los hallazgos de la exploración física21 (fig. 3), pudiendo ayudar a individualizar el tratamiento depletivo22.
Novedades en miocardiopatía hipertróficaUna de las principales novedades en el tratamiento de la miocardiopatía hipertrófica (MCH) obstructiva es el desarrollo de los fármacos inhibidores de la miosina ATPasa cardiaca, que actúan reduciendo la formación de los puentes cruzados de actina-miosina, y con ello la contractilidad miocárdica y mejorando la eficiencia energética23.
El mavacamten es el primer inhibidor alostérico selectivo de la miosina ATPasa cardiaca, que en el ensayo fundamental EXPLORER-HCM24, demostró disminuir el gradiente de obstructivo y mejorar la capacidad de ejercicio en los pacientes con MCH obstructiva sintomática. En un segundo estudio, el VALOR-HCM25, el número de pacientes que cumplían criterio para tratamiento de ablación septal se redujo en el grupo de mavacamten. Así, la guía 2023 de la Sociedad Europea de Cardiología recomienda el empleo de mavacamten en los pacientes con MCH obstructiva que continúan sintomáticos a pesar del tratamiento con bloqueadores beta o calcioantagonistas23. El aficamten es otro inhibidor de la miosina cardiaca en desarrollo, y que, en un estudio en fase 2 (REDWOOD-HCM) ha mostrado reducir el gradiente obstructivo y las cifras de NT-proBNP en los pacientes con MCH obstructiva26. La potencial utilidad de esta estrategia farmacológica en los pacientes con MCH no obstructiva no está establecida, y los ensayos clínicos están actualmente en fase de desarrollo (NCT05582395).
Imagen en el seguimiento del paciente con amiloidosis cardiacaLa realización periódica de pruebas de imagen (ecocardiografía y resonancia magnética cardiaca en la amiloidosis por transtirretina y amiloidosis por cadenas ligeras y gammagrafía DPD en la amiloidosis-TTR) se recomienda en documentos de consenso27, aunque los estudios aún son limitados. En la tabla 3 se resumen algunos de los hallazgos de ecocardiografía y resonancia magnética que podrían permitir identificar a los pacientes con respuesta adecuada o insuficiente al tratamiento. El empeoramiento en el volumen sistólico, el índice cardiaco, el strain longitudinal global (GLS) o la E/e’ mitral podrían permitir identificar precozmente a los pacientes no respondedores al tratamiento. Por otro lado, una respuesta satisfactoria en el tratamiento se asocia con una mejoría en el GLS y ratio del strain ápex/base a 12 meses27. Sin embargo, el carácter predictivo de estos parámetros aún no está claramente establecido, y deben interpretarse de una forma integrada con otras variables clínicas y analíticas28.
Parámetros de imagen en el seguimiento de la amiloidosis cardiaca
| Parámetro | Pacientes respondedores | Pacientes no respondedores |
|---|---|---|
| Ecocardiografía | ||
| FEVI | Mejoría >20% en 4 años | Ausencia de mejoría o deterioro |
| GLS | Mejoría | Empeoramiento |
| E/e’ | Sin cambio/mejoría | Incremento >20 |
| Strain ápex-base | Reducción en un año | Sin cambio |
| Grosor del septo interventricular | Reducción 1-2mm en 3-4 años | Sin cambio/empeoramiento |
| Resonancia magnética cardiaca | ||
| VEC | Reducción >5% | Incremento >5% |
| Masa ventricular | Reducción | Aumento |
FEVI: fracción de eyección del ventrículo izquierdo; GLS: strain longitudinal global; VEC: volumen extracelular.
Uno de los documentos más esperados del reciente Congreso Europeo de Cardiología 2023 es la actualización de la guía de práctica clínica sobre IC publicada en 2021. Este hecho evidencia la necesidad de actualización constante dentro de esta enfermedad tan prevalente29. Entre las principales novedades destaca el posicionamiento de los iSGLT2 en todo el espectro de la IC, tanto en los pacientes con fracción de eyección del ventrículo izquierdo (FEVI) reducida o conservada (I-A), gracias a los estudios EMPEROR-Preserved y DELIVER30, donde se demostraba un significativo beneficio en el número de descompensaciones en los pacientes con FEVI>40%. Esto hace replantear el abordaje terapéutico inicial de todos los pacientes con IC, desde el primer momento diagnóstico, independientemente del nivel asistencial (señalando la importancia del diagnóstico precoz en atención primaria), simplificando el abordaje farmacológico hasta la realización de valoraciones o técnicas más avanzadas (ecocardiograma o resonancia cardiaca), que permitan tipificar el fenotipo de dicha enfermedad.
Otro de los aspectos destacados de esta guía respecto al tratamiento farmacológico de la IC, es el ajuste de las dosis de fármacos. Las recomendaciones para iniciar el ya conocido tratamiento cuádruple, cuanto antes y de manera combinada, pueden chocar con dificultades habituales en la práctica clínica diaria: poblaciones de edades muy avanzadas, múltiples comorbilidades, seguimiento no protocolizado… por tanto, son de gran relevancia los hallazgos del estudio STRONG-HF31, donde se compararon una estrategia intensiva de ajuste de dosis de fármacos (idealmente en las primeras 2 semanas) frente al seguimiento convencional. El ajuste a dosis máximas toleradas de manera precoz demostró unos beneficios muy significativos a solo 180 días, reduciendo la mortalidad por todas las causas y nuevas descompensaciones por IC.
¿Qué debemos hacer en los pacientes sintomáticos más allá de la primera línea de tratamiento?A pesar de los grandes avances en el tratamiento neurohormonal de la IC, sigue siendo el principal motivo de ingreso en los mayores de 65 años. Por ello, el abordaje de las vías fisiopatológicas como la activación de la guanilatociclasa soluble, mediado a través de la molécula vericiguat (estimulador oral) permitiría mejorar esta vía con sus correspondientes beneficios cardiacos, vasculares o renales32. Por eso, este fármaco se une al tratamiento de los pacientes con IC con FEVI reducida, especialmente en aquellos con múltiples descompensaciones por IC en el último año33. Probablemente, el efecto más beneficioso en los pacientes con IC se haya visto con los programas de rehabilitación cardiaca, que mejoran calidad de vida y reducen hospitalizaciones. De manera muy similar, y una de las novedades más esperadas en los últimos años, el reciente estudio STEP-HF34 confirma las buenas impresiones de los análogos GLP1 en los pacientes con sobrepeso e IC (FEVI conservada en este estudio). La importancia de la obesidad y su correcto tratamiento multidisciplinar será uno de los pilares que incorporar en nuestro día a día.
Trucos «renales» para cardiólogos con interés en la insuficiencia cardiacaLa práctica clínica diaria nos ha llevado a focalizar el interés en la estrecha relación riñón y corazón. El abordaje de la IC no puede dejar de lado la interdependencia de estos órganos, especialmente si hablamos de congestión y su tratamiento. Por ello, es importante conocer las distintas combinaciones terapéuticas para tratar la congestión, como demostraron los estudios ADVOR35 con acetazolamida y el nacional CLOROTIC36 con hidroclorotiazida, ambos con resultados satisfactorios a la hora de tratar la descompensación cardiaca, mejorando la respuesta al tratamiento diurético convencional.
Otro de los aspectos compartidos entre especialidades sería el manejo de la hiperpotasemia, limitación habitual al ajustar la posología u optimizar el tratamiento neurohormonal de la IC. La aparición de los nuevos quelantes orales del potasio, asociados a un beneficio clínico y buena tolerancia, los posicionan como nuevas herramientas al ajustar las dosis en el tratamiento neurohormonal en los pacientes con ERC37,38.
La complejidad del paciente cardiorrenal explica la necesidad de contar con unidades cardiorrenales en nuestro medio, que amplien nuestro conocimiento sobre los diferentes fenotipos de pacientes y el mejor tratamiento que podamos aportar para optimizar la atención de estos enfermos39.
Actualización en cardiopatía isquémica y estructuralImplante de válvula aórtica transcatéter en los pacientes de bajo riesgoDado su enfoque mínimamente invasivo, el implante percutáneo de válvula aórtica (TAVI) se ha convertido en el principal tratamiento de la estenosis aórtica grave sintomática en los pacientes mayores de 75 años40. Esta indicación se podría ampliar en un futuro cercano a los pacientes más jóvenes con un riesgo quirúrgico bajo. Diversos estudios han demostrado que el TAVI puede ser una alternativa válida a la sustitución quirúrgica en los pacientes con estenosis aórtica grave de bajo riesgo quirúrgico41,42. Sin embargo, estos resultados deben tomarse con cautela al tratarse de cohortes pequeñas y con ausencia de seguimiento a largo plazo43. En la tabla 4 se enumeran los pros y contras del TAVI en los pacientes de bajo riesgo quirúrgico. Se necesitarán más estudios aleatorizados que tamaño muestral más grandes y que incluyan las prótesis valvulares de última generación, en ambos grupos —TAVI y sustitución quirúrgica—, para conocer el verdadero impacto de esta técnica percutánea en los pacientes con estenosis aórtica grave de bajo riesgo.
TAVI en los pacientes con bajo riesgo quirúrgico
| Consideraciones para TAVI en los pacientes con bajo riesgo quirúrgico. |
|---|
| • Ausencia de estudios aleatorizados con seguimiento a largo plazo (10 años) |
| • Tasa de necesidad de marcapasos definitivo elevada (>10%) |
| • Impacto de la fuga paravalvular |
| • Futuro acceso coronario en caso de necesidad de intervencionismo coronario |
| • Historia natural e impacto de trombosis valvular subclínica |
| • Factibilidad de reintervención en caso de degeneración protésica |
TAVI: implante percutáneo de válvula aórtica.
El desarrollo de nuevas técnicas y dispositivos junto con la mejora de la selección de los pacientes han permitido ampliar las indicaciones del tratamiento percutáneo de valvulopatías mitral y tricuspídea —especialmente la insuficiencia mitral y tricuspídea— en la última década. En el caso de la valvulopatía mitral, la principal indicación en la actualidad se encuentra en el tratamiento percutáneo de la insuficiencia mitral secundaria mediante el uso de los dispositivos borde a borde, apoyado en los resultados del estudio COAPT51. Sin embargo, con el incremento de la experiencia, su uso se amplía en los pacientes con insuficiencia mitral primaria con un riesgo quirúrgico prohibitivo44. Para obtener el máximo beneficio de esta técnica en este complejo escenario, todos los pacientes deben derivarse a centros de referencia donde los comités multidisciplinares (heart team) deber evaluar individualizadamente cada caso para confirmar la gravedad de la valvulopatía y el riesgo quirúrgico prohibitivo y valorar la factibilidad de la reparación percutánea. En aquellos casos no aptos para reparación percutánea, se puede valorar la posibilidad de recambio valvular percutáneo45.
Por otro lado, el tratamiento percutáneo de la insuficiencia tricuspídea grave sintomática se ha asociado a una mejoría clínica46. Entre las diferentes opciones terapeúticas, destacan los dispositivos borde a borde diseñados específicamente para su uso en posición tricuspídea (TriClip, Abbott Vascular, EE. UU.), la anuloplastia percutánea con el dispositivo Cardioband (Edwards Lifesciences, EE. UU.) y las válvulas heterotópicas como el TricValve (P&F Products & Features, Alemania) que ha demostrado un adecuado perfil de eficacia y seguridad47–49. La elección de un tipo u otro de dispositivo dependerá principalmente de la anatomía tricuspídea y la calidad de la imagen ecocardiográfica para guiar el procedimiento.
Papel de la revascularización percutánea en los pacientes con disfunción ventricularHasta hace poco, se desconocía el papel de la revascularización percutánea en los pacientes con disfunción ventricular grave. La publicación del estudio REVIVED-BCIS2 ha permitido superar esta situación al comparar el impacto del intervencionismo coronario percutáneo (ICP) con el tratamiento médico en los pacientes con disfunción ventricular50. Se aleatorizó a más de 700 pacientes y, tras un seguimiento de 41 meses, no se evidenció diferencias en el objetivo primario (muerte por cualquier causa o rehospitalización por IC) entre los 2 grupos. Sin embargo, los resultados de este estudio se deben tratar con cautela. Llama la atención la baja carga de enfermedad coronaria de los pacientes incluidos, lo que indicaría que el origen de la disfunción ventricular, en un porcentaje significativo de los pacientes, se puede deber a una miocardiopatía subyacente junto con enfermedad coronaria. Esto, junto con el papel cada vez más discutido del concepto de «viabilidad cardiaca» y un seguimiento a corto plazo, puede explicar la ausencia de diferencias encontradas entre los 2 grupos.
Actualización en arritmiasAbordaje integral de la fibrilación auricular: no todo es el control de ritmo o frecuencia cardiacaLa fibrilación auricular (FA) se ha relacionado de forma estrecha con hábitos de vida y comorbilidades que producen cambios estructurales en la aurícula (fibrosis, hipertrofia, inflamación, estrés oxidativo, etc.), provocando una verdadera miocardiopatía auricular51. El adecuado tratamiento de estas comorbilidades y el empleo de fármacos no antiarrítmicos que modifican este sustrato arrítmico —upstream therapies— son clave en la prevención de la FA y en su control cuando ha aparecido (tabla 5).
Grupos farmacológicos no antiarrítmicos con potencial papel en la prevención primaria y secundaria de la fibrilación auricular
| Grupo farmacológico | Resultados |
|---|---|
| BSRAA (IECA, ARA-II) | Prevención primaria: estudios preclínicos52 y observacionales53 indican que el tratamiento con BSRAA podría reducir la incidencia de FA de novoPrevención secundaria: resultados contradictorios, con un ECA que no muestra reducción de la recurrencia de FA53,54 |
| Antagonistas del receptor de mineralocorticoides | Prevención primaria: reducción de la aparición de FA denovo en los pacientes con IC con FEVI reducida55Prevención secundaria: un metanálisis de estudios observacionales mostró una reducción en la recurrencia de FA, pero no de FA postoperatoria56 |
| Bloqueadores beta | Prevención secundaria: algunos estudios observacionales muestran reducción de la recurrencia de FA. Sin embargo, la evidencia es contradictoria57 |
| Sacubitrilo-valsartán | Prevención primaria: no reduce incidencia de FA denovo en los pacientes con IC con FEVI reducida58Prevención secundaria: potencial mejoría del remodelado auricular y de la recurrencia de FA tras ablación de FA en comparación con valsartán59 |
ARA-II: antagonistas del receptor de la angiotensina II; BSRAA: bloqueantes del sistema renina angiotensina; ECA: ensayo clínico aleatorizado; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de angiotensina.
En este sentido, el ensayo aleatorizado RACE 360 demostró que un abordaje intensivo de los factores de riesgo CV mejoraba el tiempo en ritmo sinusal en los pacientes con FA persistente. La tabla 4 resume los principales grupos farmacológicos que podrían tener un papel en la prevención primaria y secundaria de la FA. Además, resulta prioritario el control, tanto farmacológico como no farmacológico, de comorbilidades asociadas a la FA, como la obesidad61 o el síndrome de apnea hipopnea del sueño62. En algunos pacientes, la inclusión en programas de rehabilitación cardiaca podría mejorar el control y los eventos adversos en los pacientes con FA63.
Anticoagulación en el paciente mayorLa prevalencia de la FA aumenta con la edad, y la edad es un predictor independiente de eventos adversos en los pacientes con FA, formando parte de las escalas habitualmente empleadas para predecir eventos isquémicos (CHA2DS2VASc) y hemorrágicos (HAS-BLED)64. A pesar de que la evidencia que demuestra el beneficio de anticoagular a los pacientes mayores superan los potenciales riesgos derivados de la fragilidad, comorbilidad y mayor riesgo de sangrado65, los pacientes mayores con FA reciben con menor frecuencia tratamiento anticoagulante66. Además, resulta imprescindible que se prescriba una dosis adecuada a la ficha técnica, ya que recibir una dosis inferior a la indicada es menos efectivo en la prevención de eventos isquémicos y asocia más mortalidad67. En la tabla 6 se recogen algunas consideraciones especiales del tratamiento anticoagulante en el paciente mayor.
Consideraciones especiales en el paciente mayor anticoagulado
| Anticoagulación en el paciente mayor |
|---|
| • Valorar riesgo/beneficio de anticoagular (generalmente el beneficio es mayor)• Ajustar dosis según criterios de ficha técnica• Monitorizar la función hepática y renal• Tratamiento adecuado de comorbilidades (p. ej., hipertensión arterial)• Medidas para la prevención de caídas• Evitar la polifarmacia y valorar las interacciones farmacológicas• Priorizar pautas de administración sencillas• Asegurar INR en rango en los pacientes con antagonistas de la vitamina K. Si no es posible, sustituir por anticoagulantes de acción directa |
La prevalencia de FA en los pacientes que van a ser sometidos a un procedimiento de intervencionismo percutáneo es de aproximadamente el 10-15%. En estos pacientes resulta esencial evaluar el riesgo trombótico y el riesgo hemorrágico, y establecer una duración de la triple terapia antitrombótica adecuada para cada caso68. Diferentes estudios aleatorizados con antagonistas de la vitamina K69 y anticoagulantes de acción directa70–73 han comparado estrategias de doble y triple tratamiento antitrombótico (tabla 6), y muestran una reducción del riesgo de complicaciones hemorrágicas sin aumento de eventos isquémicos con estrategias de tratamiento antitrombótico doble (con al menos una semana de tratamiento triple).
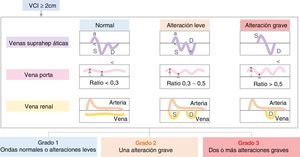
Las guías de práctica clínica de la Sociedad Europea de Cardiología proponen distintos esquemas de duración del tratamiento antitrombótico triple y doble74 (fig. 4) en función del riesgo trombótico y hemorrágico de cada paciente. En la mayoría de los pacientes, se recomienda una semana de tratamiento triple, con una duración variable entre 1, 3, 6 y 12 meses de anticoagulación e inhibidor de P2Y12. El inhibidor de P2Y12 más frecuentemente empleado en los ensayos clínicos en combinación con el ácido acetilsalicílico y anticoagulación oral es el clopidogrel, por lo que se aconseja priorizar su uso frente al de otros antiagregantes por su menor riesgo hemorrágico74.
Esquema de duración del tratamiento antitrombótico en los pacientes con fibrilación auricular e intervencionismo coronario percutáneo en función del riesgo isquémico y hemorrágico. ACO: anticoagulación oral (anticoagulantes de acción directa o antagonistas de la vitamina K); DTA: doble tratamiento antitrombótico (anticoagulación y antiagregación simple, generalmente clopidogrel); FA: fibrilación auricular; ICP: intervencionismo coronario percutáneo; TTA: triple tratamiento antitrombótico (anticoagulación y doble antiagregación con ácido acetilsalicílico e inhibidor de la P2Y12, generalmente clopidogrel).
La estimulación sin cables ha surgido en los últimos años como una alternativa a la estimulación transvenosa. Los escenarios clínicos donde estos dispositivos pueden ser especialmente relevantes son aquellos con dificultades de acceso vascular, pacientes con antecedentes de infección de la bolsa o del dispositivo o de alto riesgo, así como en casos de fractura del cable.
Los principales ensayos clínicos publicados hasta la fecha incluyen dispositivos de estimulación sin cables monocamerales75,76, monocamerales con sensado auricular77 y bicamerales78 (tabla 7). En términos generales, estos dispositivos han mostrado buenos resultados en términos de eficacia y seguridad, con una reducción del riesgo de complicaciones asociadas a los marcapasos convencionales descrito en cohortes históricas y con adecuada capacidad de detección y umbral de estimulación. Este tipo de estimulación presenta algunas limitaciones e interrogantes por resolver, como son la posibilidad de una eventual extracción, su durabilidad y resultados a largo plazo. Además, hasta la fecha no hay ensayos aleatorizados frente a los dispositivos de estimulación transvenosa que confirmen la reducción en el riesgo de complicaciones.
Principales estudios no aleatorizados de dispositivos de estimulación sin cables
| Estudio | N | Dispositivo | Estimulación | Seguridada(%) | Eficaciab(%) | Sincronía AVc(%) |
|---|---|---|---|---|---|---|
| LEADLESS II75 | 200 | LP Aveir (Abbott, EE. UU.) | Monocameral (VD) | 96 | 95,9 | — |
| Micra76 | 725 | Micra (Medtronic, EE. UU.) | Monocameral (VD) | 96 | 98,3 | — |
| MARVEL 277 | 75 | Micra-V (acelerómetro ventricular; Medtronic, EE. UU.) | Monocameral (VD) con sensado auricular | 100 | 94,3 | |
| Aveir DR i2i78 | 300 | Aveir DR i2i (Abbott, EE. UU.) | Bicameral (AD/VD) | 90,3 | 90,2 | 97,3 |
AD: aurícula derecha; AV: auriculoventricular; VD: ventrículo derecho.
La tormenta arrítmica, entendida como 3 o más eventos ventriculares sostenidos en menos de 24 h que requieran intervención para su control, es siempre un reto terapéutico. El manejo tradicional con fármacos antiarrítmicos (amiodarona y bloqueadores beta) como primera opción terapéutica y la ablación cardiaca como segunda opción terapéutica en caso de recurrencias está cada vez más en entredicho79. Diferentes estudios han demostrado el beneficio de una ablación cardiaca precoz como primer recurso80,81.
Para finalizar, debemos recordar el uso del soporte circulatorio mecánico (principalmente mediante el uso de oxigenadores extracorpóreos de membrana) en los pacientes con shock cardiogénico secundario a tormenta arrítmica (nivel de recomendación IIb en las actuales guías europeas), como puente a la ablación cardiaca79.
ConclusionesDado el impacto de la enfermedad CV, es necesario conocer las últimas novedades en su tratamiento con el fin de trasladar ese beneficio a nuestros pacientes. El IV Congreso de los Jóvenes Cardiólogos de la Sociedad Española de Cardiología abordó las principales novedades en el campo de la enfermedad CV, y continúa su crecimiento como punto de encuentro del presente y futuro de la cardiología.
FinanciaciónLos autores declaran no haber recibido financiación para la realización de este trabajo.
AutoríasLos autores que envían el manuscrito aceptan la plena responsabilidad de su contenido tal y como lo define el International Committee of Medical Journal Editors. Todos los autores han contribuido de forma similar a este artículo.
Conflicto de interesesP.L. Cepas-Guillén declara honorarios por conferencias de AstraZeneca, Almirall, Daiichi Sankyo, Amgen y Novo Nordisk, y apoyo para asistir a reuniones o viajes de AstraZeneca y Pfizer. A. Laffond declara apoyo para asistir a reuniones o viajes de Bayer y Novartis. J. Borrego Rodríguez declara honorarios por conferencias de AstraZeneca, Novartis, Novo Nordisk, Amarin, Lilly, Viatris y Adamed, y apoyo para asistir a reuniones o viajes de Novo Nordisk. D. Gonzalez-Calle declara honorarios por conferencias de NovoNordisk, AstraZeneca, Bayer y Daiichi Sankyo.