La miocarditis eosinofílica (ME) es una entidad infrecuente, con una presentación clínica variable, que consiste en la inflamación e infiltración de eosinófilos en el músculo cardiaco y que se acompaña frecuentemente de eosinofilia en sangre periférica1. La ME es una causa inusual de insuficiencia cardiaca que presenta una elevada morbimortalidad con el retraso diagnóstico, por lo cual es importante la sospecha clínica y confirmación diagnóstica precoz2. Este informe de caso clínico busca concienciar a los profesionales sanitarios sobre la presencia de procesos patológicos agudos y reversibles en el miocardio que nos deben hacer actuar rápidamente para disminuir la mortalidad y morbilidad asociadas a la referida entidad.
Se presenta el caso clínico de un paciente de sexo masculino de 58 años, con antecedentes personales de diabetes mellitus. En un control rutinario, 2meses antes del proceso actual, se detectó eosinofilia en sangre periférica, y se encontraba pendiente de completar estudio etiológico. Acudió al servicio de urgencias por 4 días de disnea progresiva hasta hacerse de mínimos esfuerzos, dolor torácico con irradiación interescapular y con empeoramiento en posición de decúbito supino. Asimismo, asociaba ortopnea y disnea paroxística nocturna. En la exploración física, presentó presión arterial de 96/68mmHg, frecuencia cardiaca de 123 latidos por minuto y saturación de oxígeno de 88%. A la auscultación presentó ruidos cardiacos taquicárdicos, regulares y sin soplos; en el pulmón, crepitantes húmedos en ambos campos. El electrocardiograma mostró una taquicardia sinusal, ondas Q en DII, DIII y AVF, con una falta de progresión de primer vector en precordiales. Radiografía de tórax con cardiomegalia e infiltrados alveolares bilaterales compatible con edema agudo de pulmón. Se realizó una analítica en la que destacó una leucocitosis de 30.500/μL con una hipereosinofilia marcada de 10.980/μL (36%), elevación del propéptido natriurético cerebral y las enzimas de daño miocárdico (troponinas).
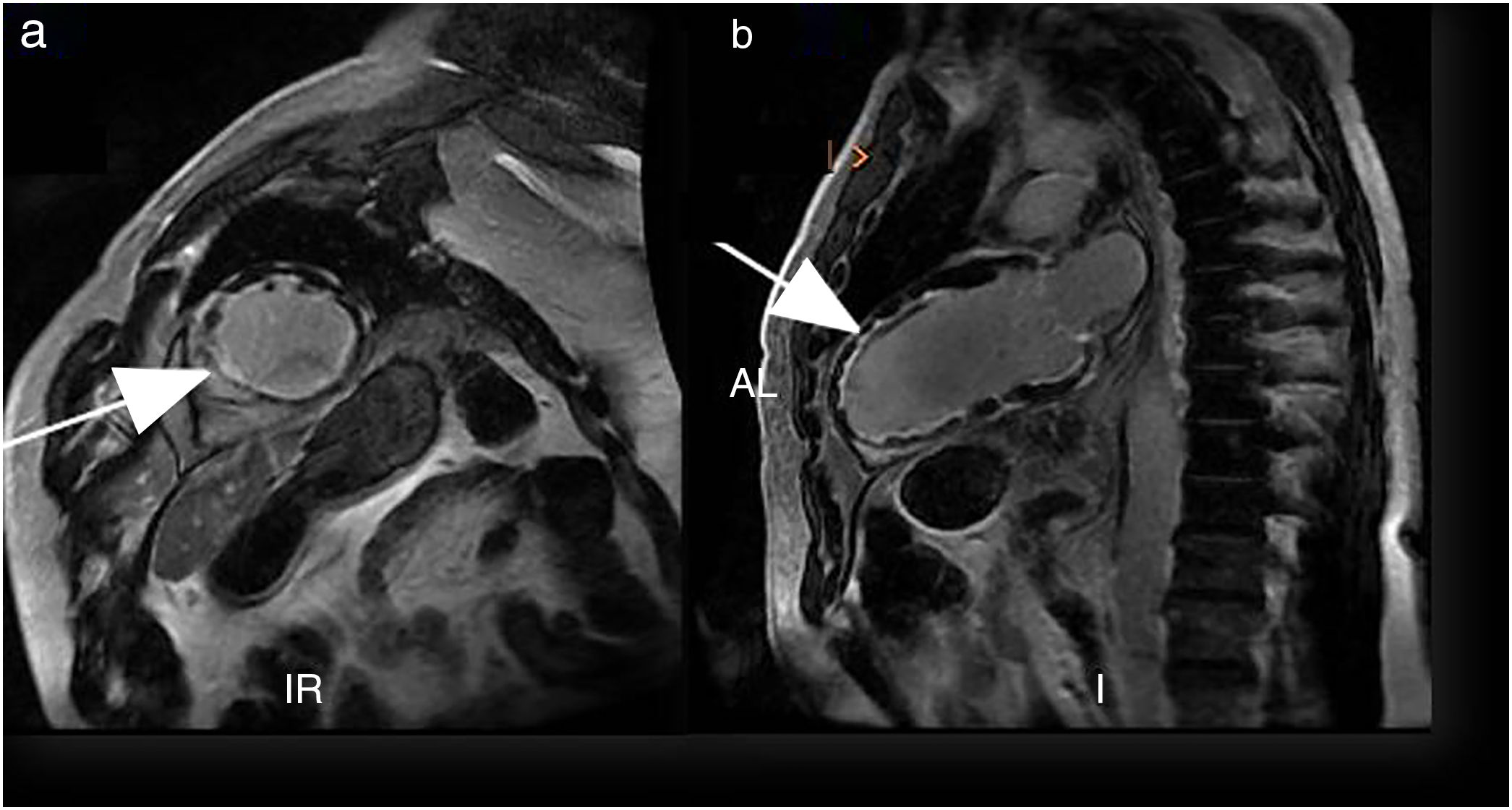
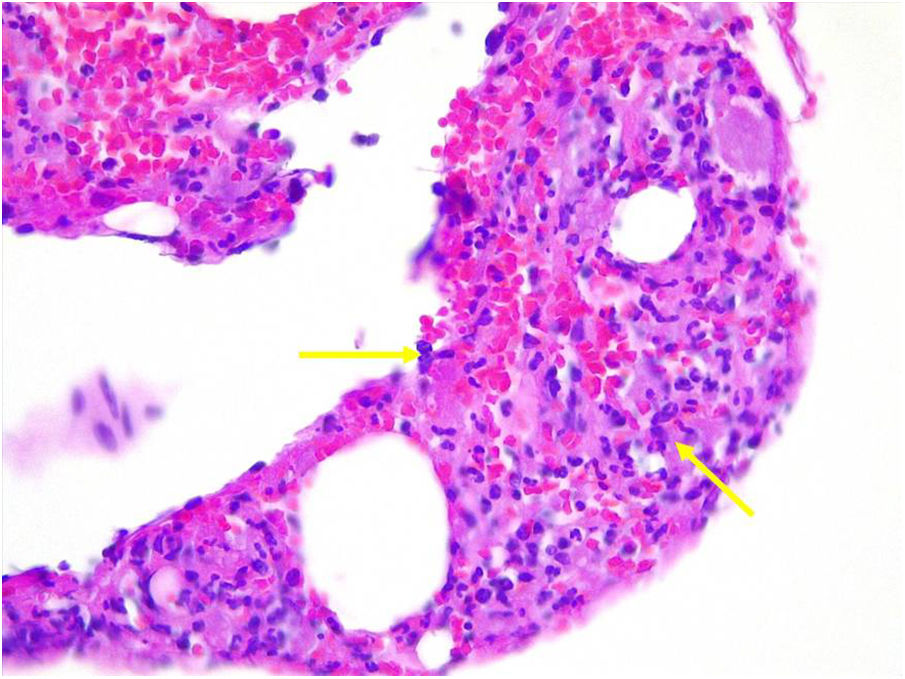
Se trasladó a la unidad coronaria, donde precisó medidas de soporte vital avanzado, fármacos vasoactivos e implante de balón de contrapulsación aórtica. El ecocardiograma mostró hipocinesia difusa de predominio en segmentos septal, medial y apical, disfunción ventricular grave con una fracción de eyección del ventrículo izquierdo (FEVI) <30% (en el estudio rutinario por la eosinofilia se realizó un ecocardiograma 2semanas antes del ingreso que mostró FEVI de 67%). Una cardiorresonancia magnética evidenció en las secuencias de realce tardío la presencia de captación de contraste subendocárdico del 25% del grosor de la pared y difuso por todas las caras ventriculares, con predominio transmural septoinferior medio, hallazgos compatibles con ME (fig. 1a y b). La coronariografía cardiaca no evidenció alteraciones vasculares sugestivas de origen isquémico y la biopsia endomiocárdica mostró el músculo miocárdico con fibrosis focal y presencia de abundantes eosinófilos (fig. 2). Para completar el estudio de la hipereosinofilia grave con compromiso de órgano diana, se realizó un aspirado de médula ósea en el que se observaron abundantes eosinófilos (64% de la celularidad total), sin células neoplásicas, parásitos ni otras alteraciones morfológicas.
Cardiorresonancia magnética. Eje axial corto (a) y eje axial largo (b). En las secuencias de realce tardío se aprecia la presencia de captación de contraste subendocárdico del 25% del grosor de la pared y difuso por todas las caras ventriculares, con predominio transmural septoinferior medio; hallazgos compatibles con miocarditis eosinofílica.
Con diagnóstico de síndrome hipereosinofílico (SHE) idiopático y ME secundaria, se inició tratamiento con corticoides (prednisona a dosis de 1 mg/kg al día). A los 4 días presentó mejoría clínica, analítica y ecocardiográfica (FEVI 44%), por lo cual se trasladó a planta convencional y se le dio el alta hospitalaria tras 2 semanas de estabilidad clínica.
A los 30 días del alta hospitalaria, reconsultó por clínica de insuficiencia cardiaca con FEVI (40%), a pesar del tratamiento óptimo de insuficiencia cardiaca y corticoides. Durante el ingreso presentó mejoría con tratamiento depletivo, se le dio de alta posteriormente y mantuvo una FEVI alrededor del 45%.
Los siguientes meses permaneció estable sin requerir nuevos ingresos y toleró una reducción lenta y progresiva de la corticoterapia hasta continuar con dosis de mantenimiento de 10-20 mg de prednisona al día, con una FEVI similar a la del alta en ecocardiograma de control realizado a los 6 meses.
La ME corresponde al tejido miocárdico inflamado con un gran componente de infiltración por eosinófilos, lo cual le da su nombre histopatológico. Este patrón anatomopatológico puede ser visto en diversas entidades, entre las que la más frecuente es la miocarditis por hipersensibilidad, seguida del SHE, como nuestro caso2. Por otro lado, se define como hipereosinofilia la detección de eosinófilos en sangre periférica superior a 1.500/μL en 2 determinaciones en un intervalo mayor de un mes o la hipereosinofilia en una biopsia de órgano diana. Se conoce como SHE cuando existe daño estructural o funcional orgánico no justificado por otras causas. Los tejidos que normalmente se ven afectados son la piel, los pulmones y el tracto gastrointestinal. Sin embargo, con menor frecuencia pueden producirse afecciones en el miocardio y generar una forma de miocarditis, como ocurrió en nuestro caso3.
La primera descripción de afección cardiaca fue hecha por Loeffler en 1936, y en estudios recientes se describe una incidencia hasta de un 20% en los pacientes con SHE2.
Fisiopatológicamente, la ME tiene 3 etapas. En primer lugar, ocurre una miocarditis o necrosis aguda debida a la infiltración del miocardio por eosinófilos, que da lugar a clínica de síndrome coronario agudo o insuficiencia cardiaca. En segundo lugar, puede suceder una trombosis con riesgo de complicaciones embólicas. Finalmente, el estadio fibrótico puede causar valvulopatías que, a menudo, requieren cirugía2-4.
No existen datos concluyentes sobre prevalencia y características epidemiológicas de la ME. En una revisión sistemática en la que se incluyó a 179 pacientes, se observó una edad media de 41 años, con prevalencia similar en ambos sexos. El 47,4% fueron caucásicos. La presentación clínica es variable: desde casos asintomáticos hasta formas con miocarditis aguda fulminante o miocardiopatía restrictiva crónica. Habitualmente existe compromiso de la FEVI: en la revisión sistemática la media es de 35%, como en nuestro caso1. El diagnóstico debe sospecharse en pacientes con clínica de miocarditis o insuficiencia cardiaca. Asimismo, es frecuente la hipereosinofilia en sangre periférica, aunque en algunos casos puede estar ausente, lo cual puede motivar un retraso en el diagnóstico2,3. La cardiorresonancia puede usarse como soporte diagnóstico a través de la visualización de infiltración del miocito, inflamación y edema, aunque estos cambios no siempre están presentes. El gold standard es la biopsia endomiocárdica1-4. El objetivo diagnóstico es, además, determinar la causa subyacente de la hipereosinofilia, ya que de ello dependerá la elección y la efectividad del tratamiento. La ME puede desarrollarse en el contexto de hipereosinofilia reactiva (enfermedades inflamatorias, infecciones parasitarias, reacciones adversas a fármacos), neoplásicas (desórdenes mieloides clonales) o, como en nuestro caso, de un SHE idiopático4.
El tratamiento de la ME depende del compromiso hemodinámico y de la presentación clínica. En caso de insuficiencia cardiaca con FEVI reducida, se requiere tratamiento según las guías de práctica clínica y puede requerirse inicialmente medicación inotrópica y soporte mecánico circulatorio4,5. El tratamiento para contrarrestar el efecto de los eosinófilos es gradual: el primer escalón son los corticoides (prednisona de 0,5 a 1 mg/kg inicialmente y de 5 a 10 mg/día de mantenimiento), con respuesta en el 85% de los casos. En aquellos que no respondan al primer escalón, se han usado terapias citorreductoras con hidroxiurea e interferón-α, u otros inmunosupresores, como la ciclosporina1-5. Existen estudios que describen una normalización de la FEVI en pacientes con ME sin fibrosis al instaurar precozmente un tratamiento adecuado. No obstante, una vez establecido el daño miocárdico, este será irreversible y generará, por ejemplo, miocardiopatía dilatada e insuficiencia cardiaca crónica6. Por otro lado, la mortalidad asociada a la enfermedad objeto de estudio es alta y depende del retraso en el diagnóstico: existen cohortes con hasta una 22,3% de muerte intrahospitalaria4.
Consideramos como hipótesis que la no recuperación de la FEVI y la persistencia de clínica de insuficiencia cardiaca del caso presentado se deben al hecho de la presencia de áreas de fibrosis en la biopsia miocárdica, ya que esta provoca un daño irreversible estructural a pesar del óptimo tratamiento.
Como conclusión, nuestro caso clínico es sobre una entidad poco frecuente, como es la ME, con una presentación clínica consistente en insuficiencia cardiaca aguda con compromiso de la FEVI y shock cardiogénico. Según nuestra revisión, es importante considerar este diagnóstico en el contexto de un paciente con insuficiencia cardiaca aguda una vez descartadas las causas más comunes, ya que su potencial reversibilidad tiene implicaciones terapéuticas y pronósticas.