La endocarditis infecciosa (EI) es una enfermedad de mal pronóstico que, a pesar de las mejoras en el manejo diagnóstico y terapéutico, está asociada a gran mortalidad y complicaciones graves1,2. Su incidencia ha aumentado en el periodo 2003-2014 en España (2,72 a 3,14/100.000 personas/año) con menor presencia de valvulopatía reumática, aunque los pacientes suelen tener más edad, más valvulopatía degenerativa, más válvulas protésicas y dispositivos intracardiacos. La mortalidad intrahospitalaria es del 20,4% en series recientes y hasta un 23% de los casos precisan cirugía3.
Se presenta el caso de un varón inmunocompetente de 34 años con endocarditis sobre tubo valvulado aórtico tras cirugía de Bentall. El paciente tuvo una estenosis aórtica grave en la infancia por válvula aórtica bicúspide que se intervino mediante operación de Ross en 2001. En 2007 se intervino nuevamente con cirugía de Bentall tras desarrollar estenosis aórtica grave del homoinjerto y dilatación de raíz aórtica.
En el seguimiento se detectó degeneración del homoinjerto pulmonar con estenosis pulmonar grave, pero el paciente permaneció asintomático hasta finales de 2018. En ese momento experimentó un cuadro clínico de episodios febriles de hasta 39°C de predominio vespertino, de semanas de evolución y sin otra sintomatología asociada, que cedían con tratamiento antibiótico pautado por su médico de atención primaria, pero tenían recurrencias tras finalizar el tratamiento. No presentaba clínica sugestiva de origen en otro foco infeccioso y no había sufrido manipulaciones dentarias, urológicas, gastrointestinales ni contacto con animales. Dada la clínica y la presencia de una cardiopatía predisponente para endocarditis, se ingresó al paciente para completar el estudio.
Tras iniciar antibioterapia empírica con ampicilina y gentamicina, el paciente se encontraba asintomático, sin nuevos episodios febriles. Inicialmente, la hemoglobina fue 14,1g/dl, leucocitos 4.550/μl, velocidad de sedimentación globular (VSG) 117mm/h y la proteína C reactiva (PCR) 20,78mg/l. Hemocultivos negativos. Las serologías para Coxiella, Brucella, Borrelia, Mycoplasma, Legionella y hongos (Aspergillus) fueron negativas. Los ANA (anticuerpos antinucleares), anticuerpos anti-ADN (anti-ácido desoxirribonucleico) y factor reumatoide, negativos. En las ecocardiografías transtorácica y transesofágica no se observaron imágenes que sugirieran vegetaciones, abscesos, seudoaneurisma, fístulas ni nueva dehiscencia del homoinjerto ni del tubo valvulado aórtico. La PCR se negativizó tras la antibioterapia y los ecocardiogramas de control se mantenían sin imágenes compatibles con endocarditis.
Tras los resultados negativos en las pruebas y la alta sospecha clínica de EI, se decidió realizar una tomografía por emisión de positrones/tomografía computarizada con 18F-fluorodesoxiglucosa (PET/TC con 18F-FDG) de cuerpo entero. En la PET/TC con 18F-FDG se observó un intenso hipermetabolismo periprotésico circundando la válvula mitral y un incremento focal de actividad metabólica en la pared anterior de la aorta ascendente con relación al tubo valvulado aórtico compatible con una endocarditis (fig. 1A,B). Además, se realizó TC craneal y toraco-abdominal y no se detectaron eventos embólicos ni foco séptico. Estos hallazgos apoyaron el diagnóstico de endocarditis como criterio mayor junto a 2 criterios menores ya presentes (fiebre>38°C y enfermedad cardiaca predisponente), aunque sin llegar a cumplir los criterios de una endocarditis definida según las guías4.
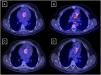
A y B: imágenes obtenidas de la PET/TC con 18F-FDG pocos días después del inicio de antibioterapia empírica. C y D: la misma prueba de control tras 4 semanas de antibioterapia. El panel A muestra hipermetabolismo periprotésico circundando la válvula mitral; el panel B, un incremento de la actividad metabólica en la aorta ascendente con relación al tubo valvulado aórtico. Los paneles C y D muestran persistencia del hipermetabolismo, pero de menor intensidad respecto a los previos.
Por tanto, se decidió continuar la antibioterapia empírica. En el seguimiento, el paciente se encontraba afebril y con buenos resultados analíticos y ecocardiográficos de control. A las 4 semanas se realizó una PET/TC con 18F-FDG de control que detectó la persistencia de hipermetabolismo periprotésico, pero de menor intensidad respecto al estudio previo (fig. 1C,D). El tratamiento antibiótico se finalizó tras completar 6 semanas y, al estar asintomático con normalización de reactantes de fase aguda y sin nuevos episodios febriles durante 2 días, se extrajeron hemocultivos de control y se decidió el alta hospitalaria.
Sin embargo, el paciente volvió a ingresar al día siguiente del alta con fiebre de hasta 39°C, astenia, poliartralgias y cefalea. Respondió favorablemente a la misma antibioterapia empírica previa. Los hemocultivos al ingreso fueron negativos y el ecocardiograma tampoco mostró cambios respecto a los previos. Ante la recidiva de endocarditis con hemocultivos negativos y tras discusión por el equipo multidisciplinario, se decidió tratamiento quirúrgico. Durante la intervención se observaron señales de infección local en la zona del tubo valvulado aórtico y el homoinjerto pulmonar calcificado (fig. 2), por lo que se sustituyeron el homoinjerto pulmonar y el tubo valvulado aórtico por 2 nuevos homoinjertos. En las primeras horas del posoperatorio el paciente presentó un aumento del débito en el drenaje pericárdico, por lo que tuvo que ser reintervenido, y se detectó un sangrado de una arteria epicárdica en la cara anterior del ventrículo derecho que se suturó con éxito. Tras esto, el paciente presentó buena evolución clínica y analítica, ecocardiograma con ambos homoinjertos normofuncionantes y cultivos negativos del material retirado de la cirugía. A las 6 semanas del segundo ingreso, y tras completar un nuevo ciclo de antibioterapia, se dio el alta al paciente. En la revisión de los 2 meses permanecía asintomático, sin nuevos episodios febriles y con ecocardiografías transesofágica y transtorácica con homoinjertos normofuncionantes.
En la imagen izquierda se muestra el campo quirúrgico tras una esternotomía media. El tubo valvulado aórtico (flecha azul) es separado fácilmente de un material de aspecto friable (flecha amarilla) compatible con infección local. En la imagen derecha se identifica el homoinjerto pulmonar degenerado y calcificado. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Este caso clínico permite resaltar la importancia de la PET/TC con 18F-FDG en el diagnóstico de EI, ya que en las últimas guías sobre EI de la Sociedad Europea de Cardiología (ESC) (2015) la detección de actividad anómala alrededor de la válvula protésica, cuando la prótesis o el dispositivo se implantó hace más de 3 meses, se incluyó como criterio mayor de las pruebas de imagen para el diagnóstico de EI4. Esto es especialmente relevante en pacientes con material protésico que dificulta su diagnóstico por ecocardiografía transtorácica y transesofágica, por lo que debido al aumento de implante de prótesis y dispositivos intracardiacos esta prueba puede ser de utilidad en el futuro en el diagnóstico de endocarditis. También puede ser una herramienta útil para monitorizar la respuesta al tratamiento antibiótico, aunque actualmente no se disponga de datos suficientes para dicha recomendación.
Este artículo presenta algunas limitaciones. Según el protocolo de nuestro centro, cuando se sospecha EI con pruebas complementarias negativas y alta sospecha clínica, se realiza, en primer lugar, una PET/TC con 18F-FDG. Si la prueba no fuera muy sugestiva y persistiera sospecha clínica, el siguiente paso sería la tomografía por emisión monofotónica (SPECT) marcada con leucocitos. Otra limitación fue la ausencia de una nueva PET/TC con 18F-FDG de control tras la cirugía, aunque su especificidad es menor en los primeros meses tras la cirugía.